|
|
morfologia de meduloepitelioma e ependimoblastoma. 5. CD34, Ki67, p53 |
|
|
|
morfologia de meduloepitelioma e ependimoblastoma. 5. CD34, Ki67, p53 |
|
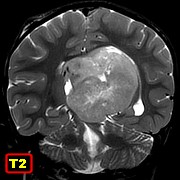
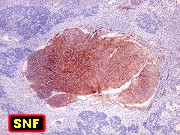
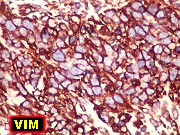
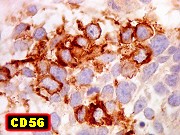
| Fem. 2 a 10 m. Clique para TC, RM, HE, Masson, IH - GFAP, SNF, MAP2, vimentina, nestina (texto), AE1AE3, 1A4, CD56, CD99, S100, HMB45, INI1, CD34, Ki67, p53. Texto |
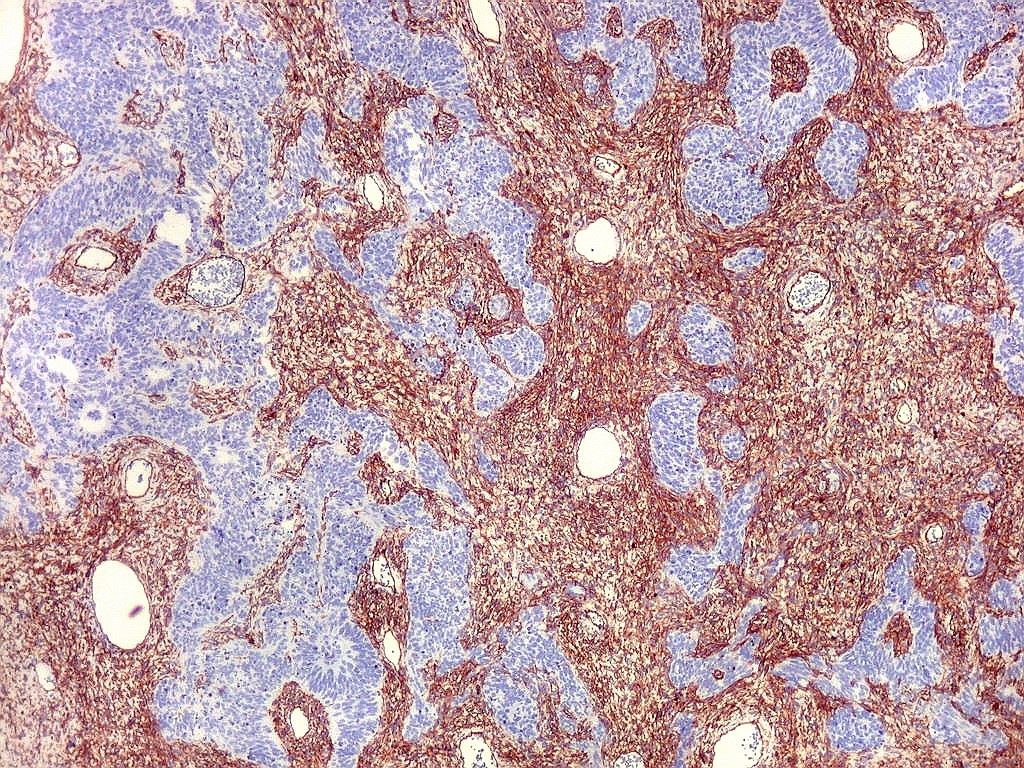
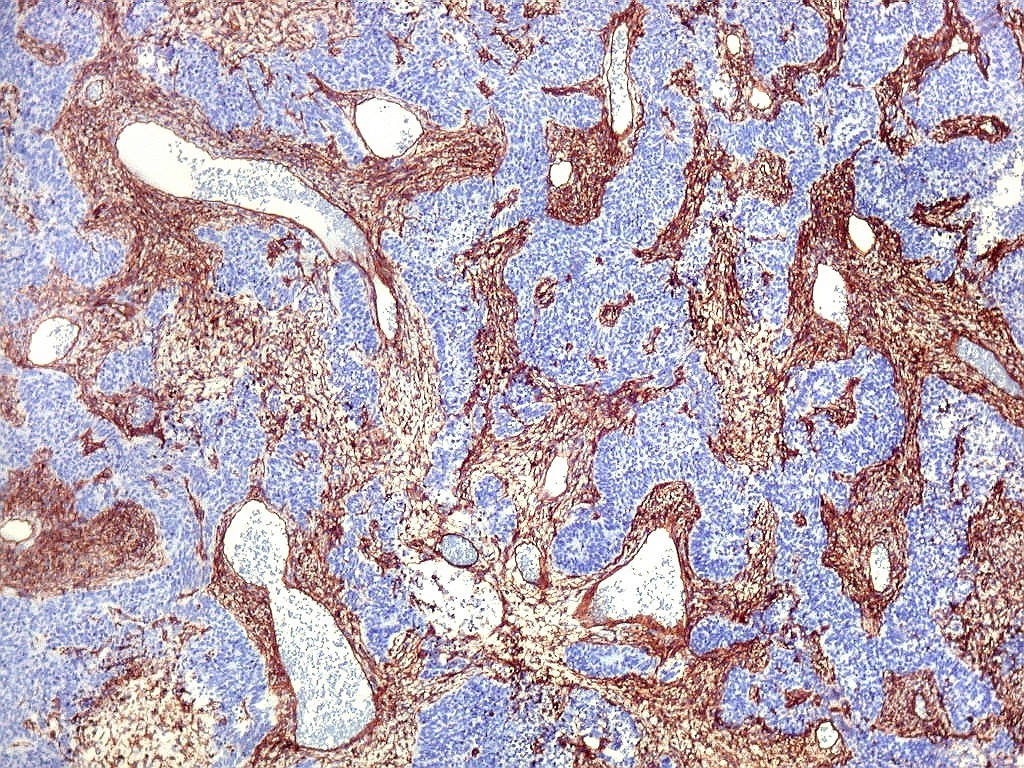
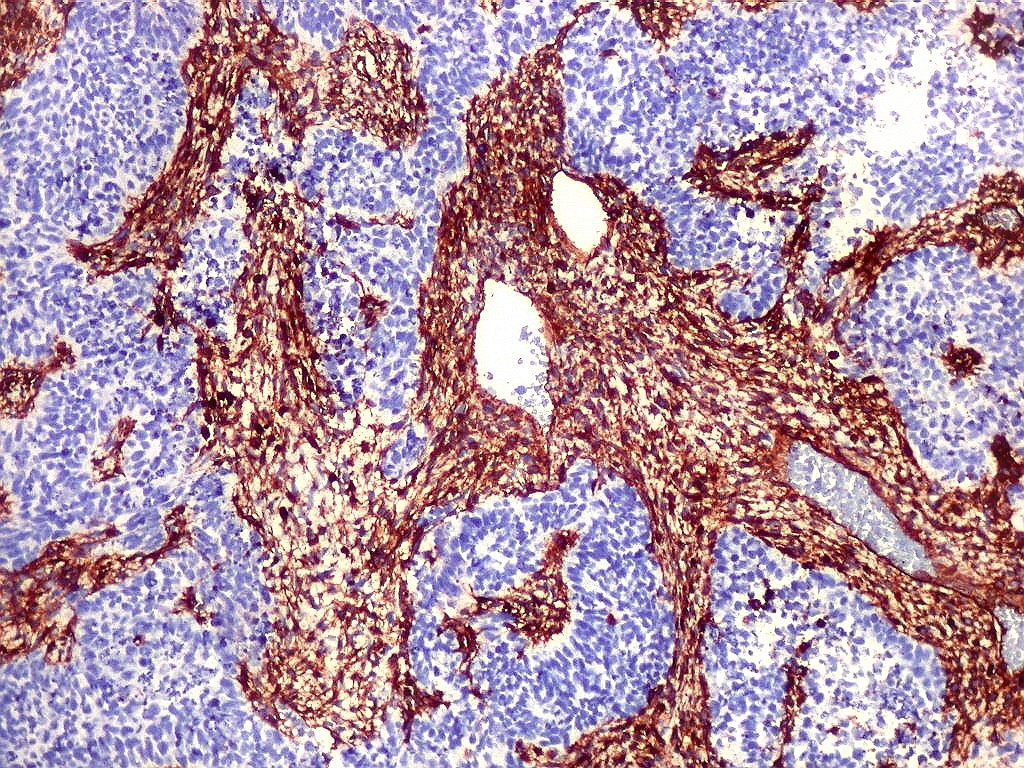
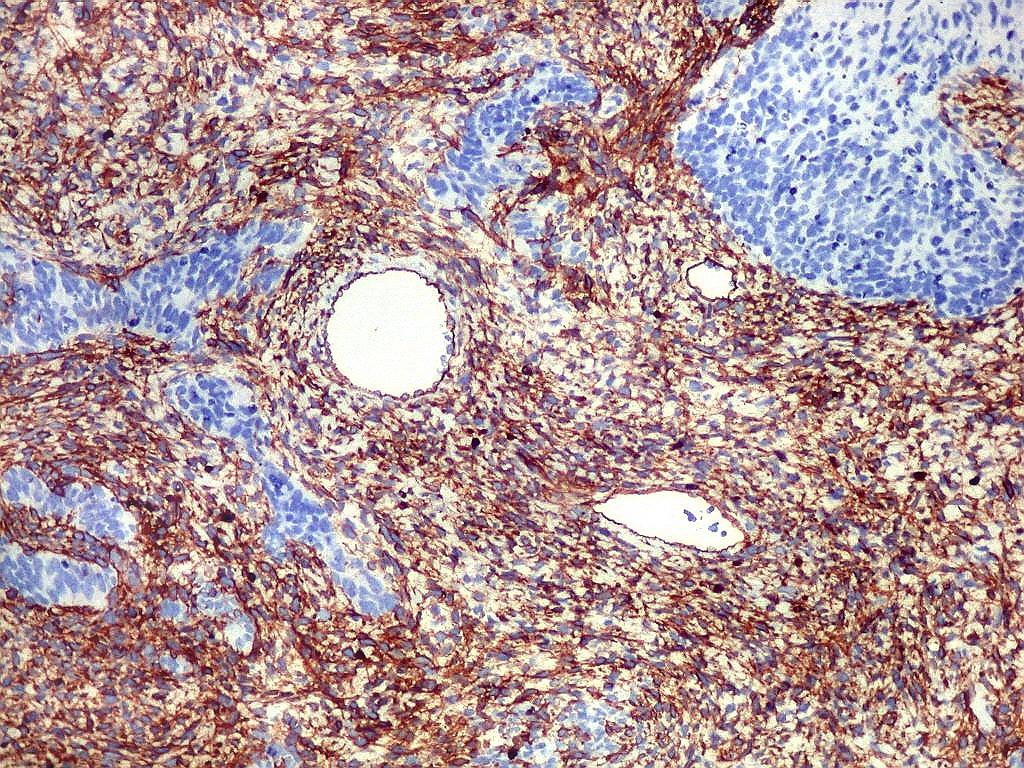
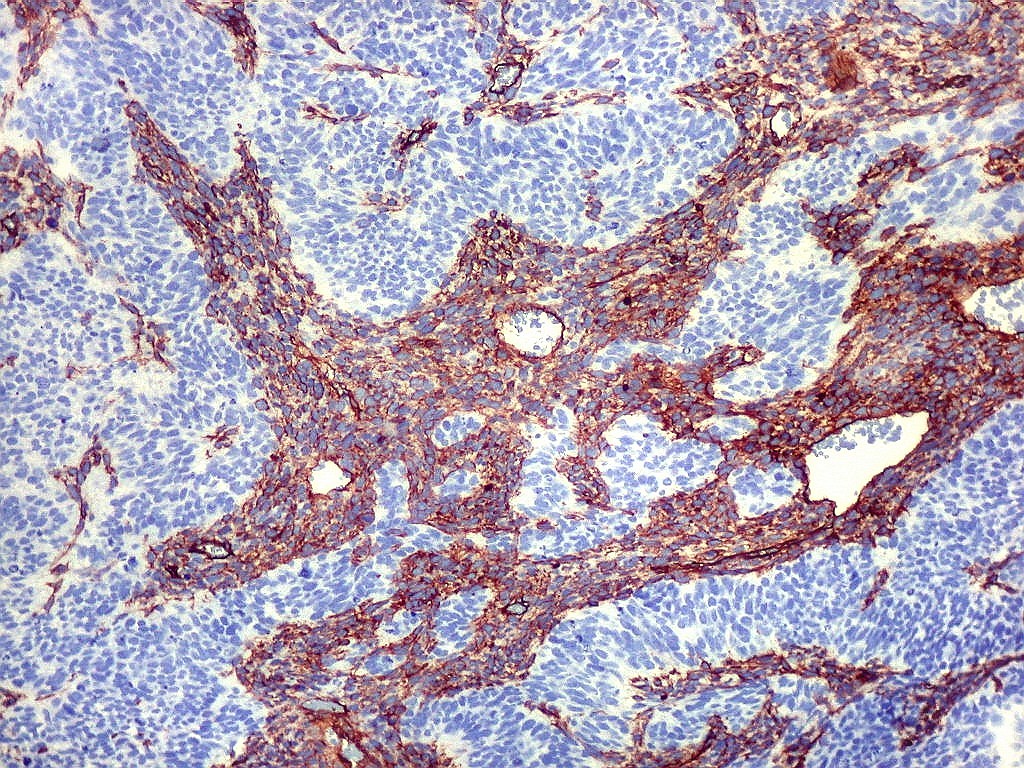
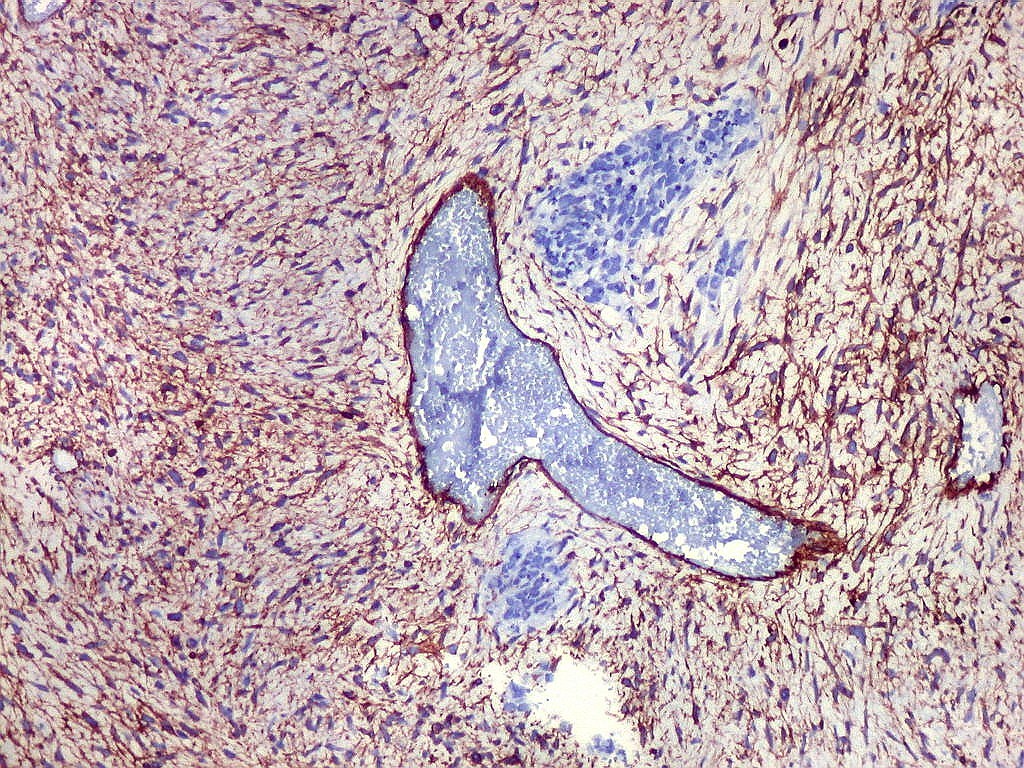
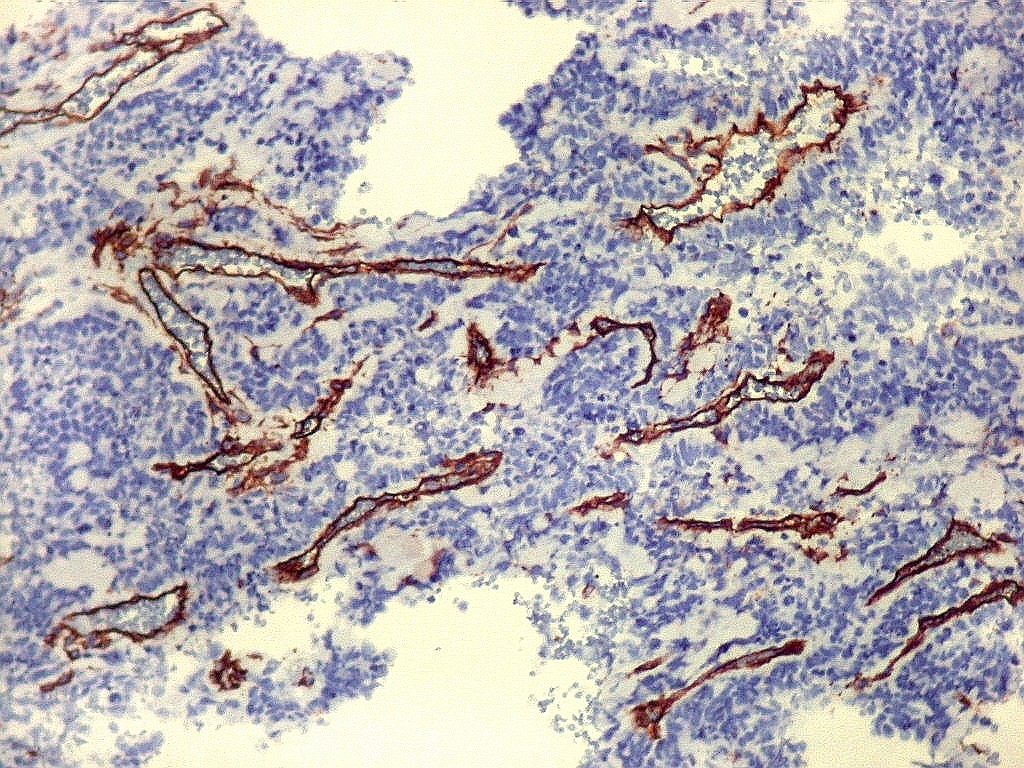
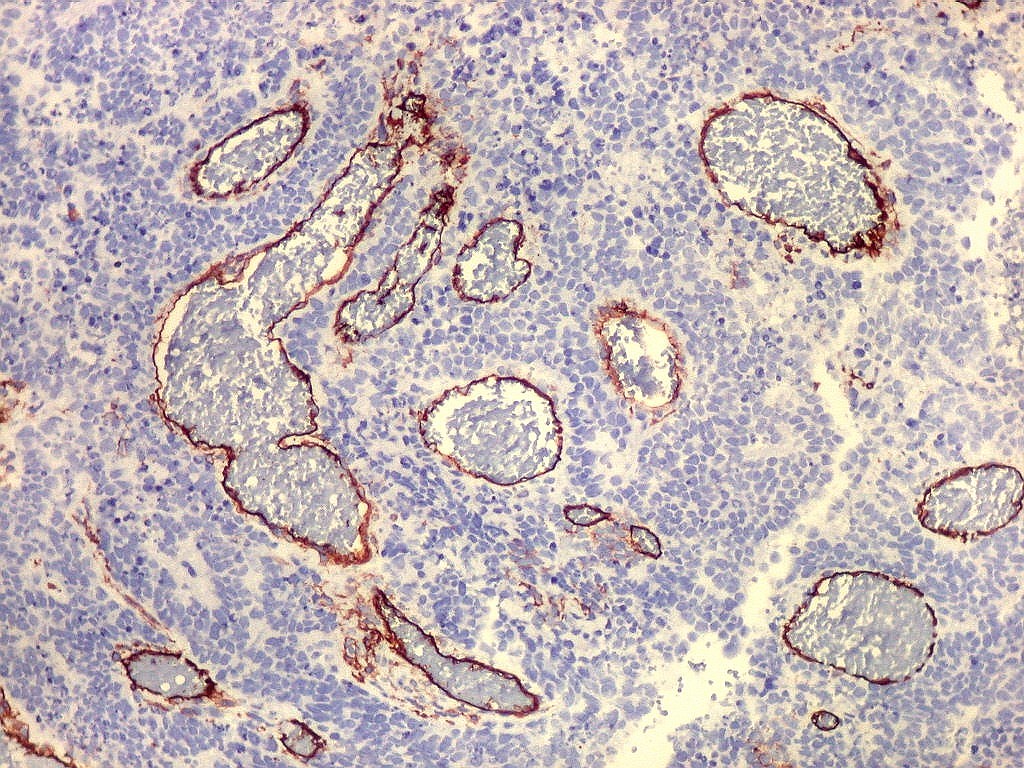
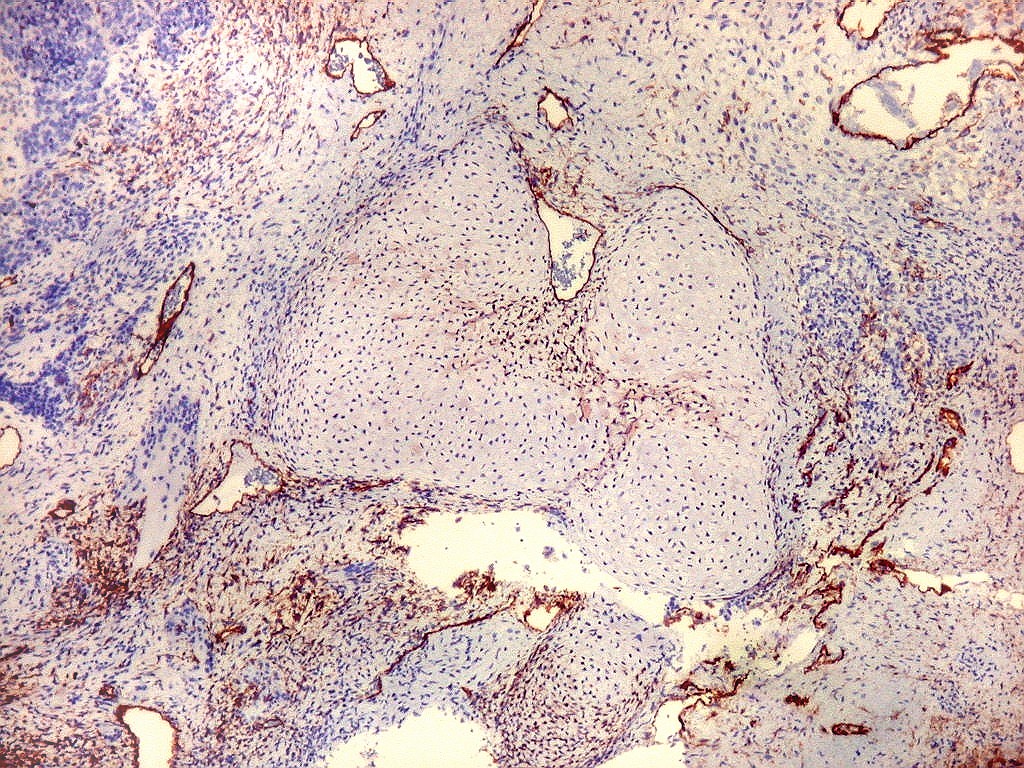
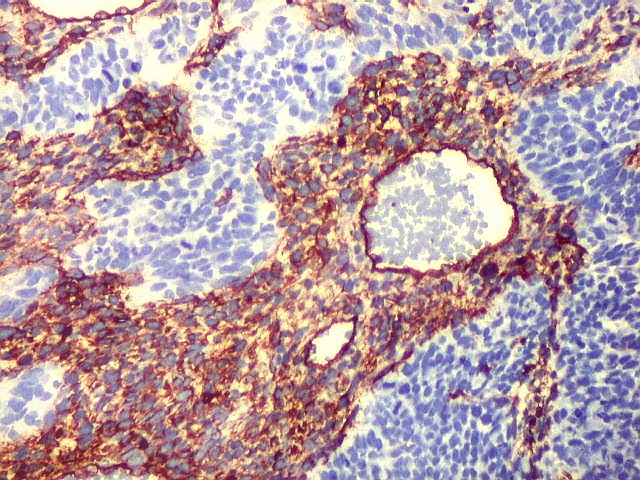
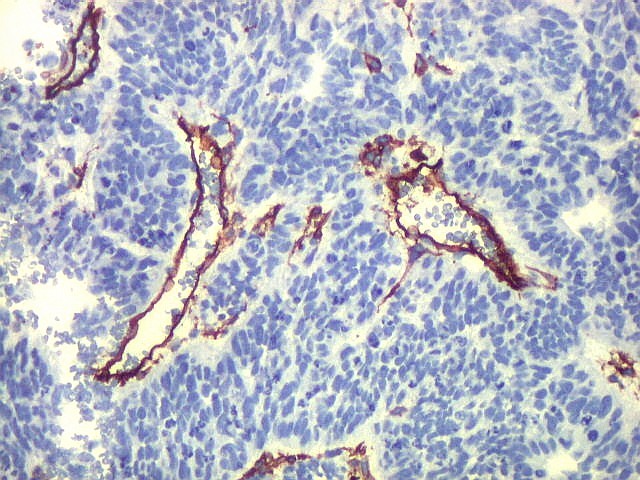
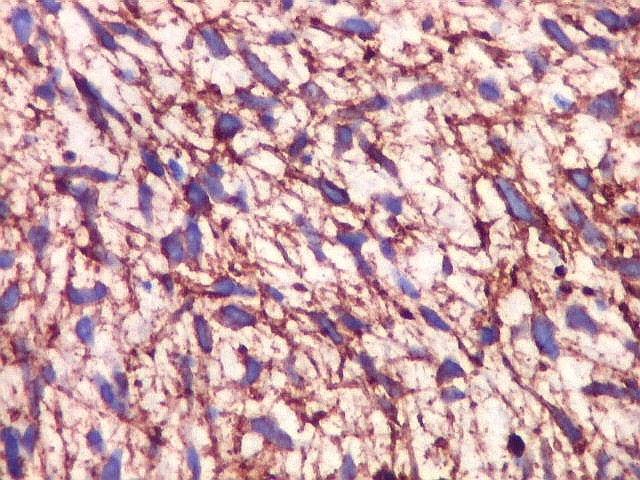
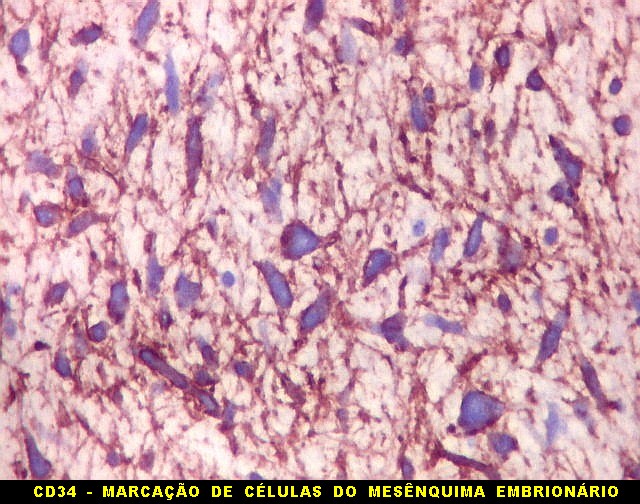
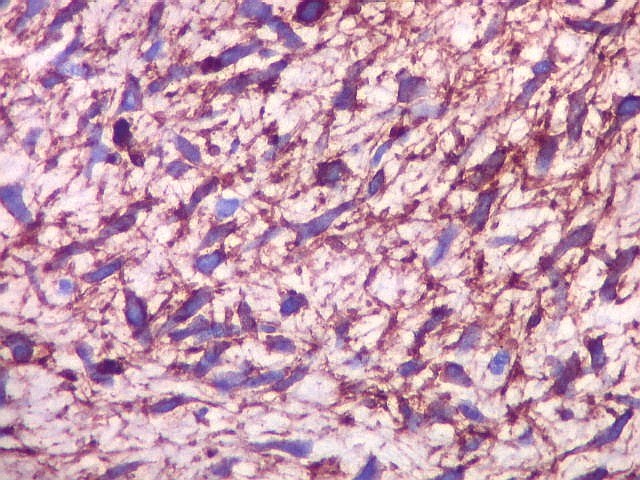
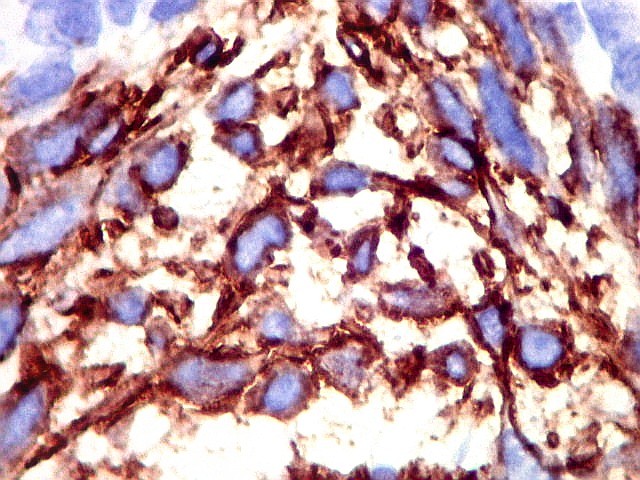
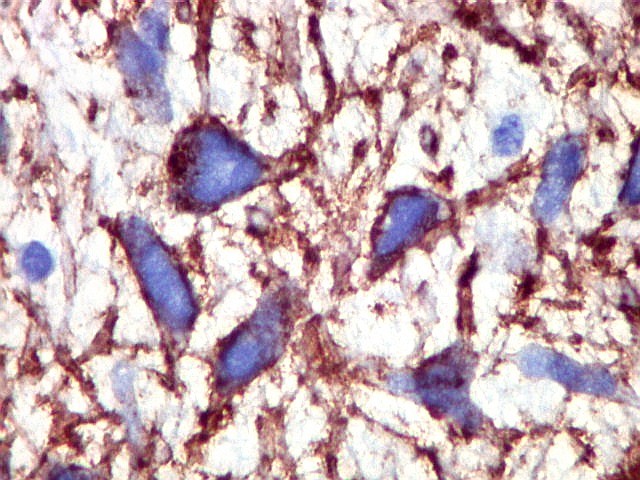
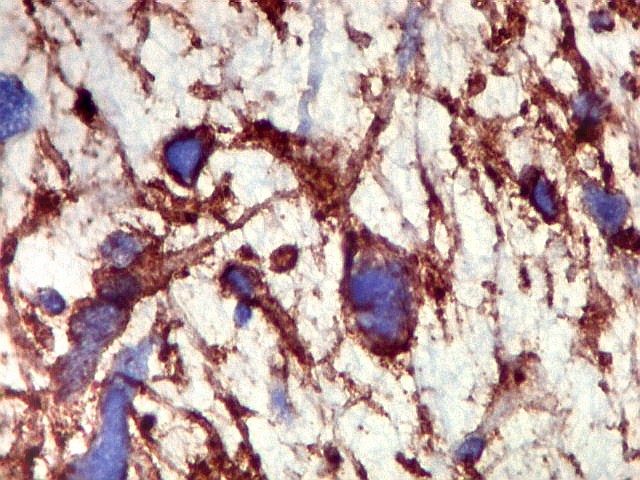
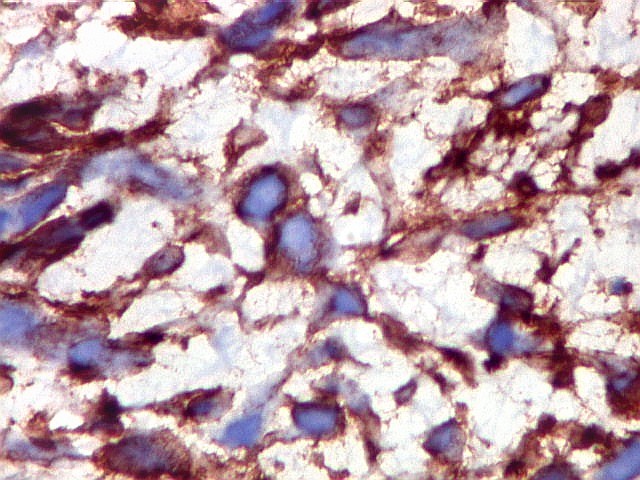
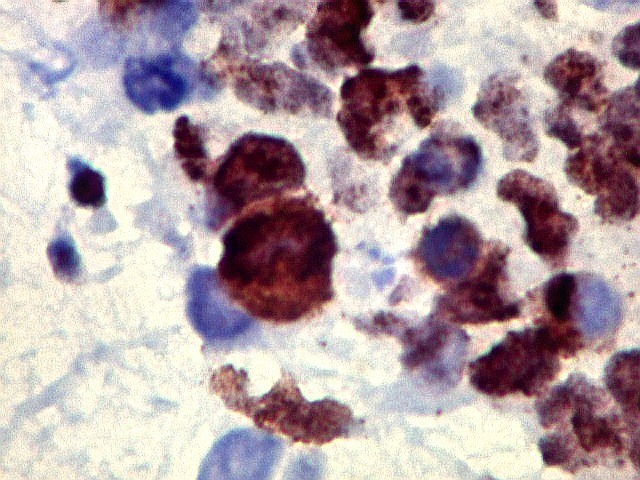
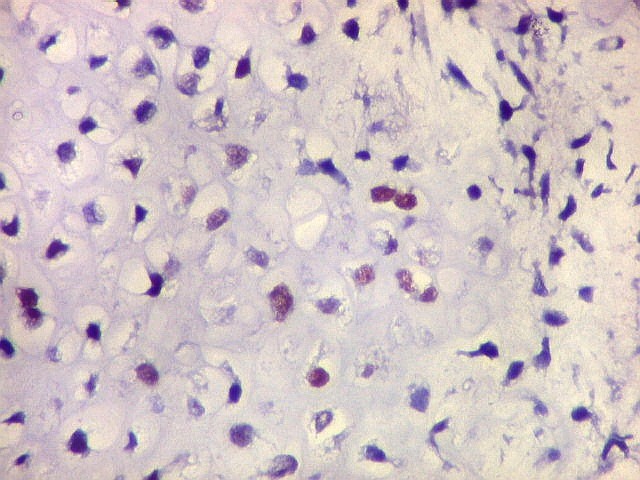
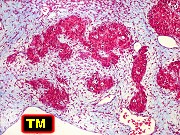
| CD34. CD34 é um antígeno oncofetal (para textos (1)(2) e outros detalhes, clique). Aqui, observou-se marcação intensa e homogênea das células do mesênquima embrionário, além da positividade habitual no endotélio vascular. As células do neuroepitélio não marcaram. Em outros exemplos de PNETs postados aqui, observamos positividade para CD34 somente em vasos (1)(4)(6)(7)(8) mas também, em outros casos, na membrana de células neoplásicas (2)(3)(5). |
 |
 |
 |
 |
 |
 |
 |
 |
 |
 |
 |
 |
 |
 |
 |
 |
 |
 |
 |
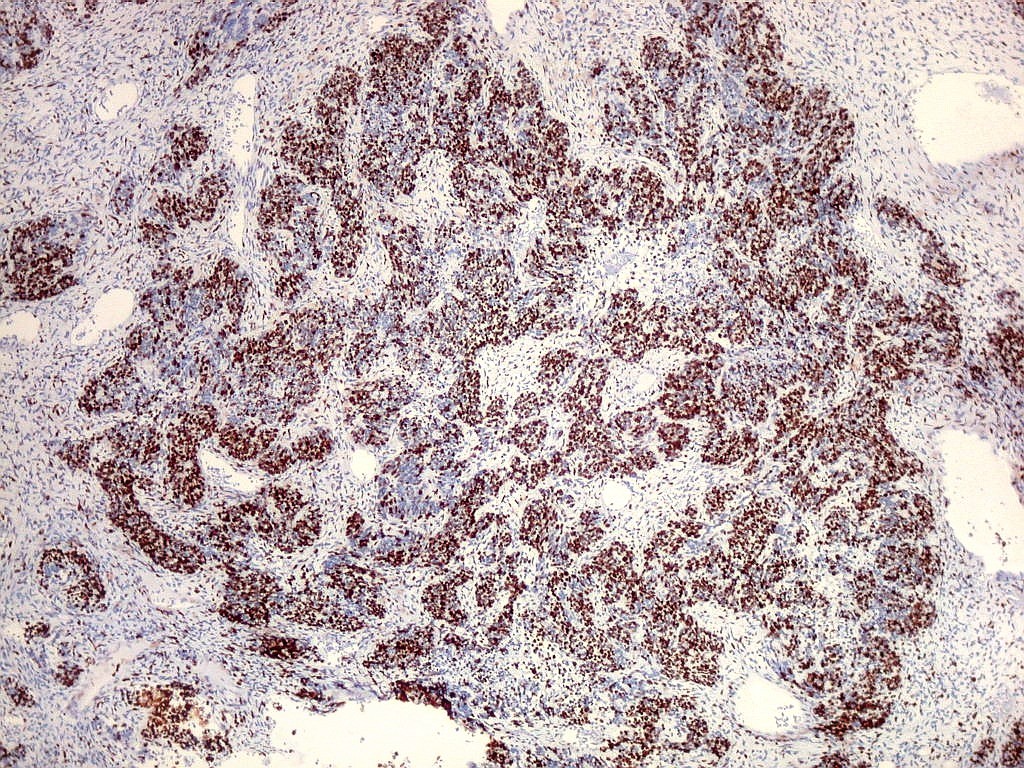
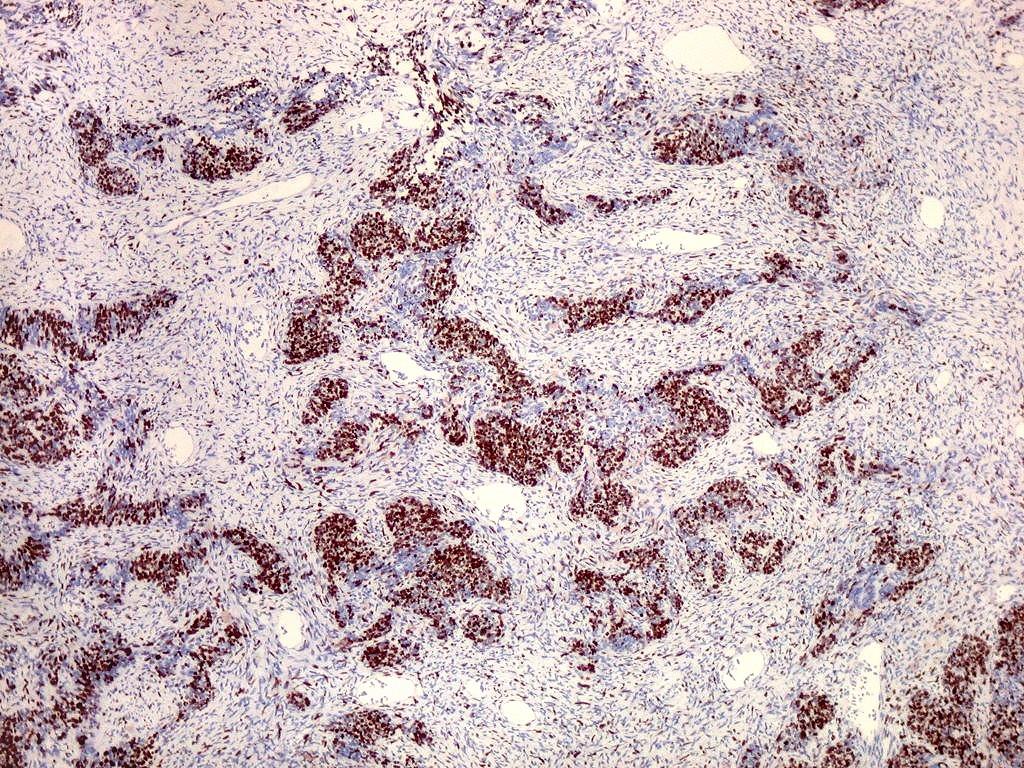
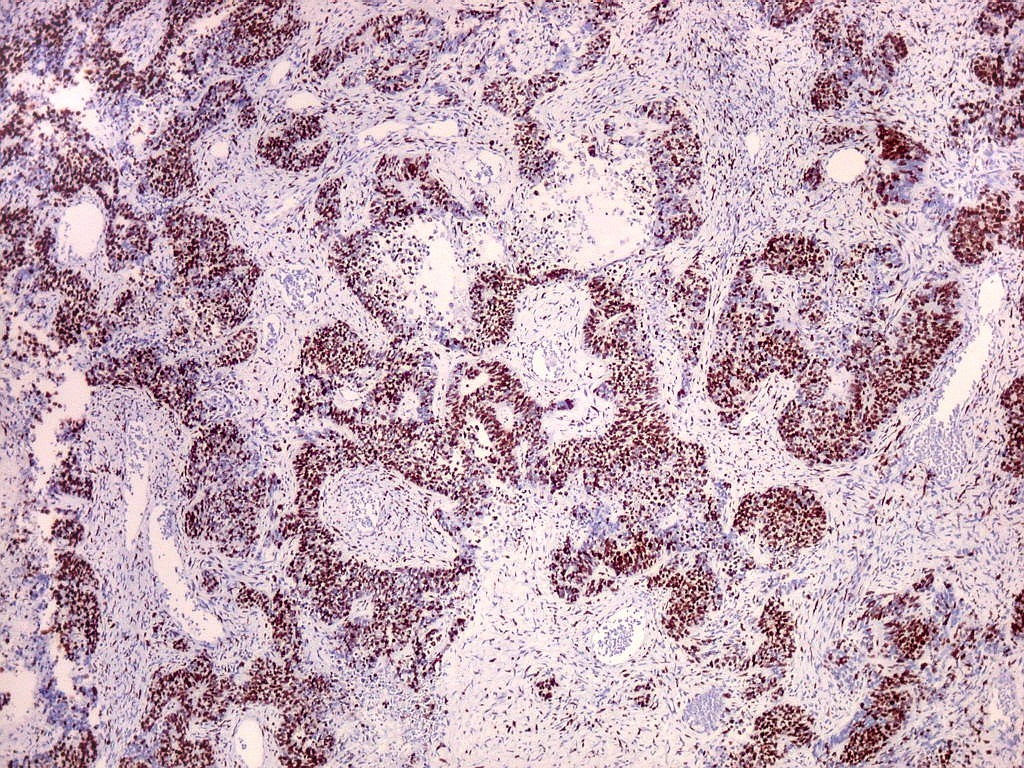
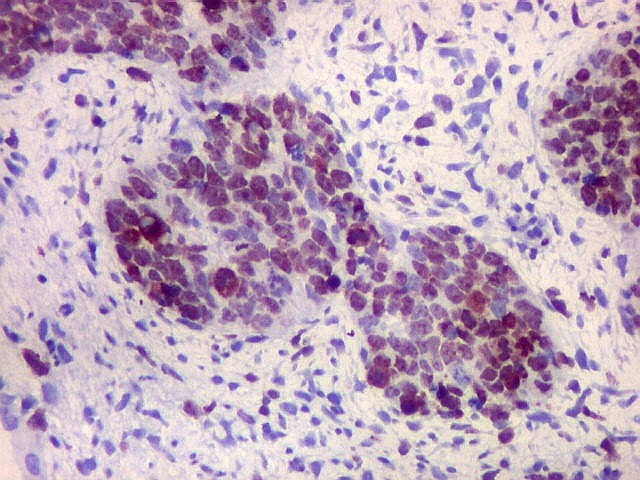
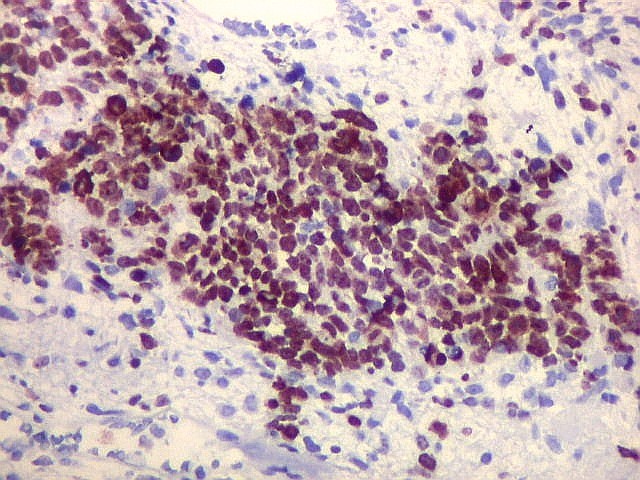
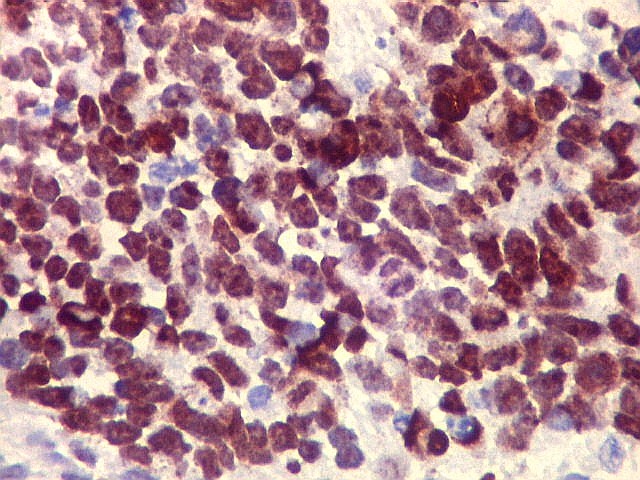
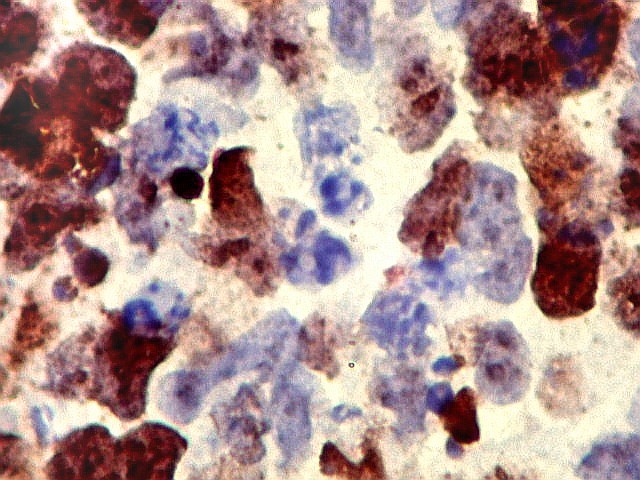
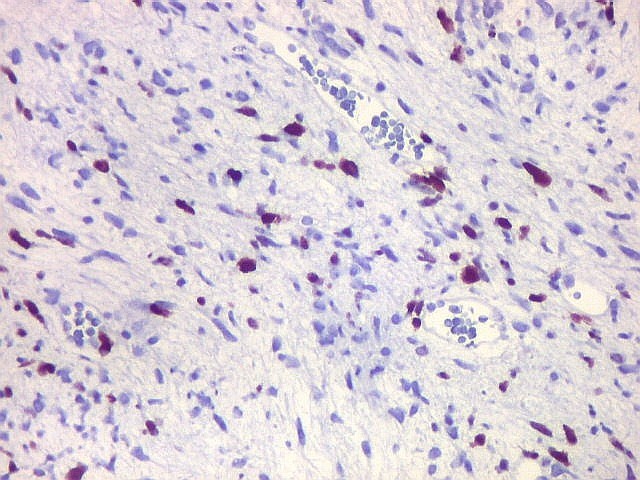
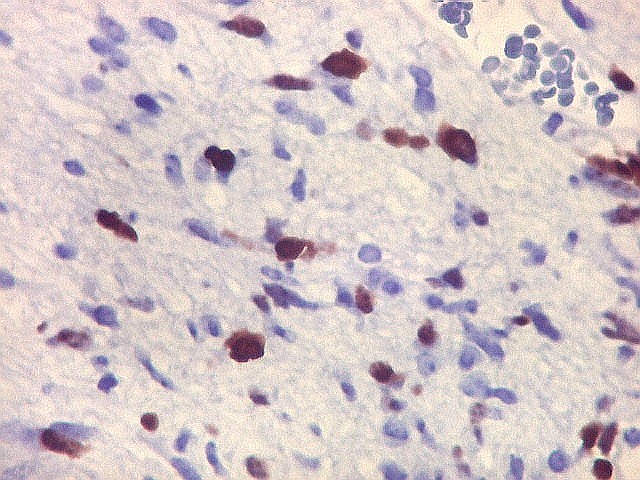
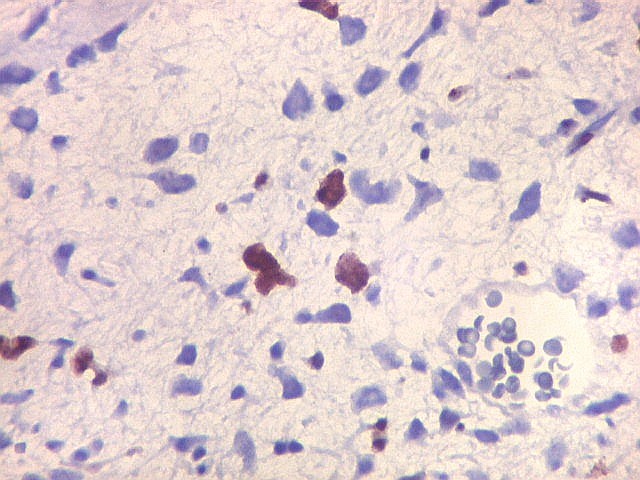
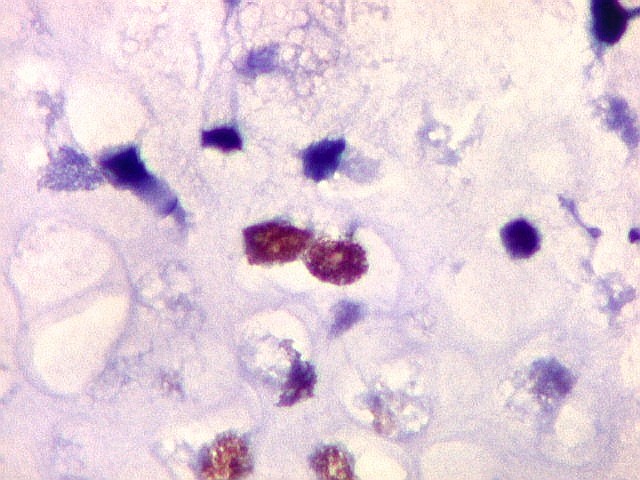
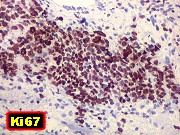
| Ki67. O marcador de proliferação celular Ki67 foi fortemente positivo no neuroepitélio, com áreas excedendo 80%, em concordância com o alto índice mitótico encontrado nestas regiões. No mesênquima embrionário e no fragmento de cartilagem, a positividade foi mais modesta, da ordem de 10 a 20%. Os achados estão em linha com o crescimento rapidamente progressivo do tumor. |
 |
 |
 |
 |
 |
 |
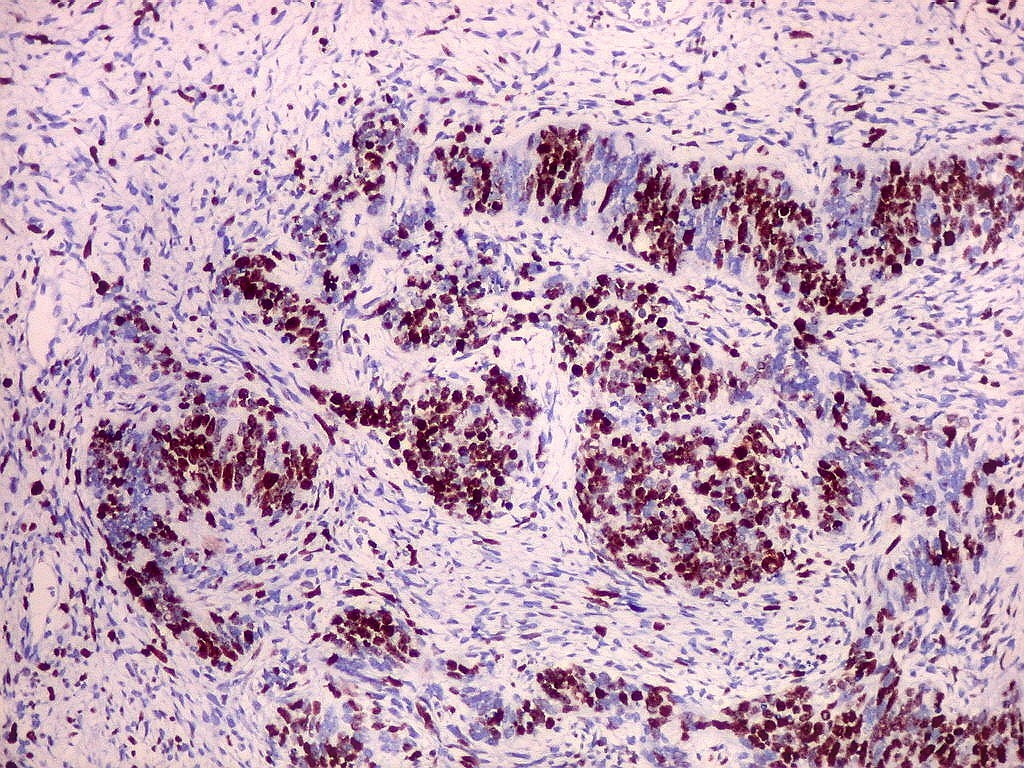
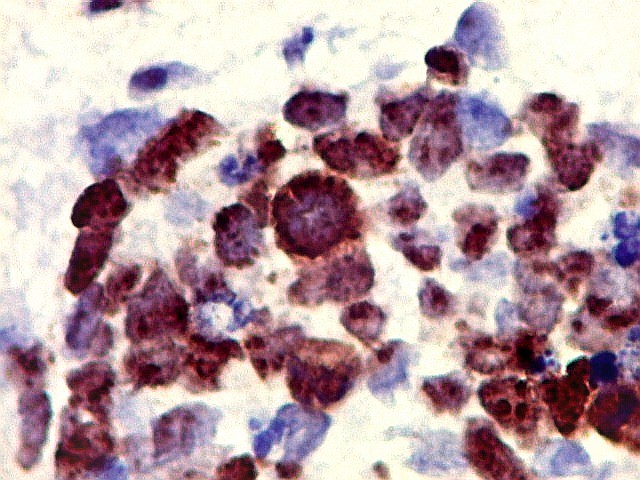
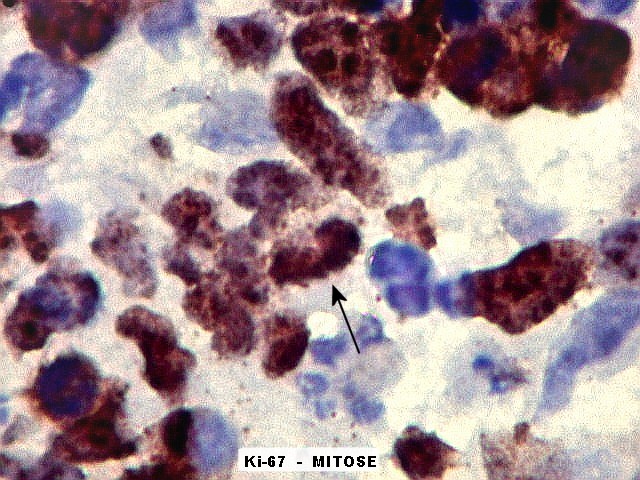
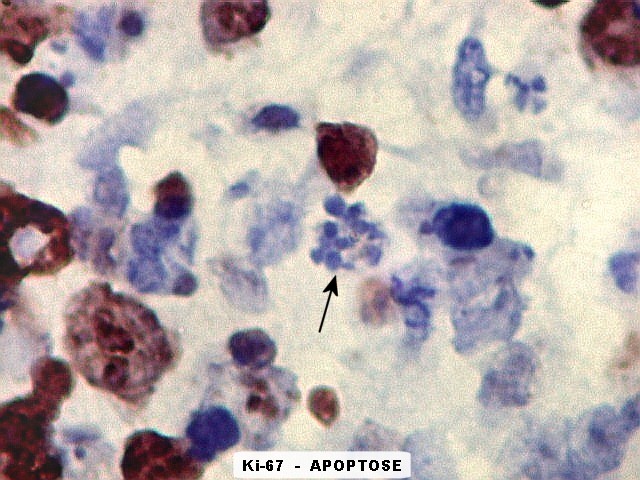
| Ki67. Neuroepitélio. Notar que cromossomos em mitose marcam, células em apoptose são negativas. | |
 |
 |
 |
 |
 |
 |
 |
 |
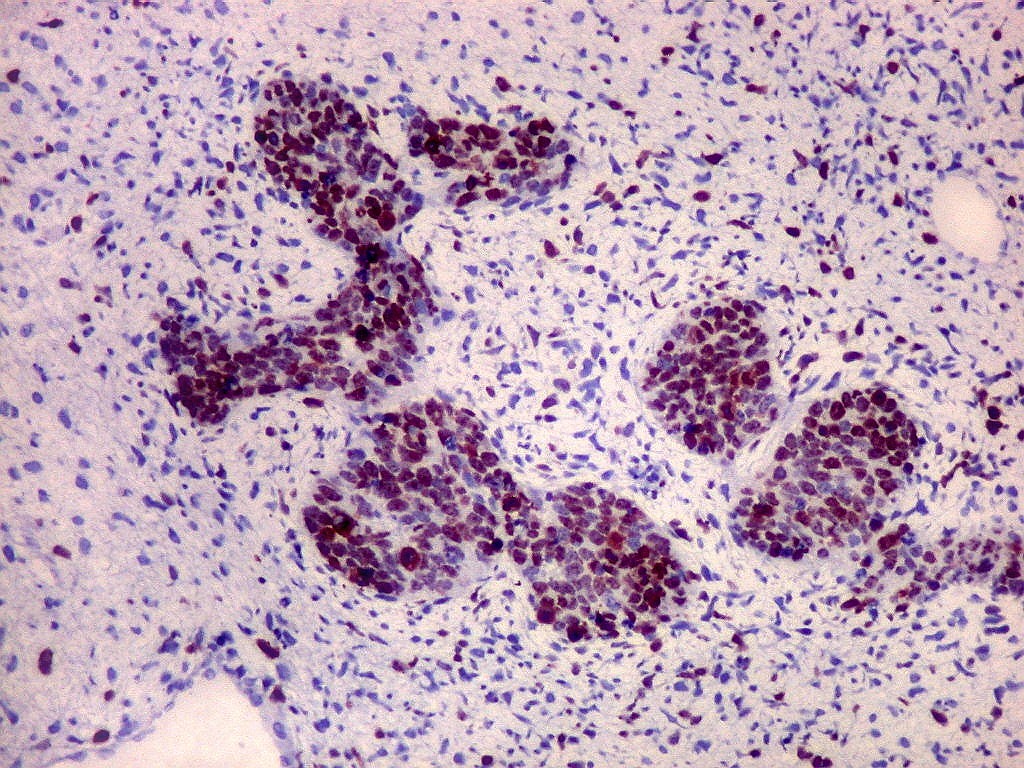
| Ki67. Mesênquima. | |
 |
 |
 |
 |
 |
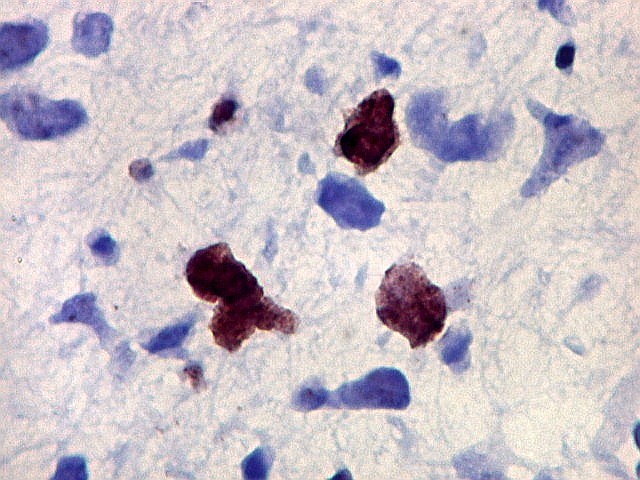 |
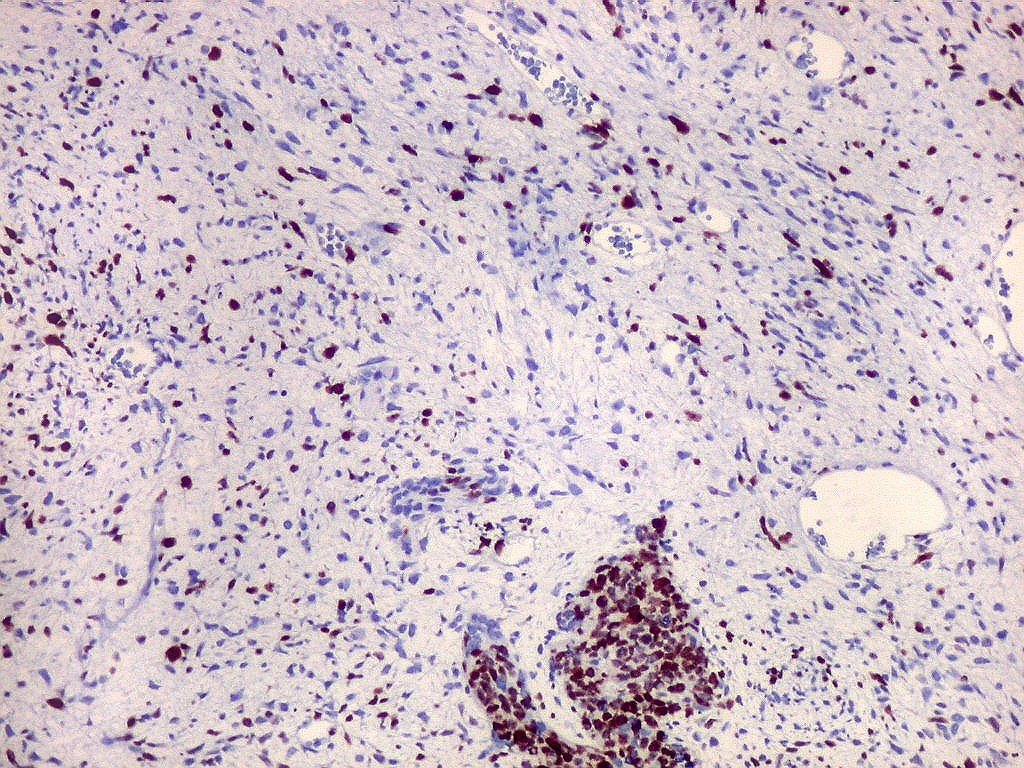
| Ki67. Cartilagem. | |
 |
 |
 |
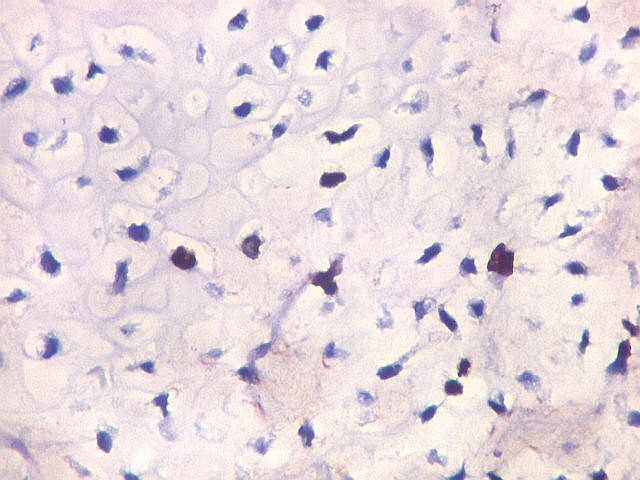 |
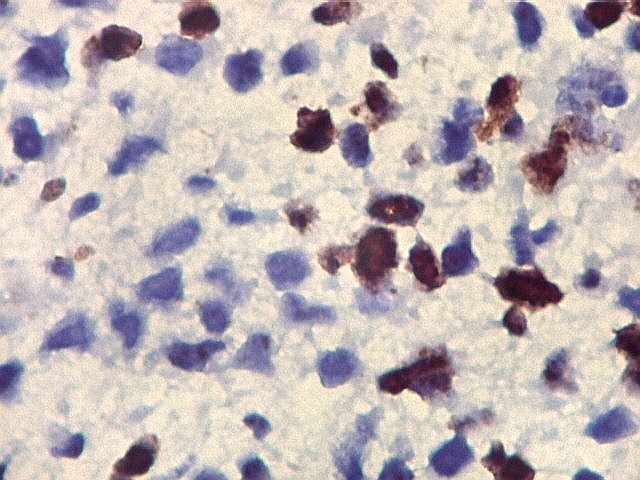
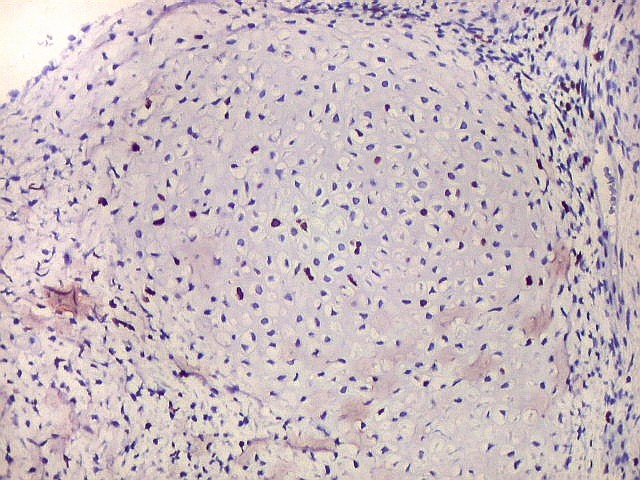
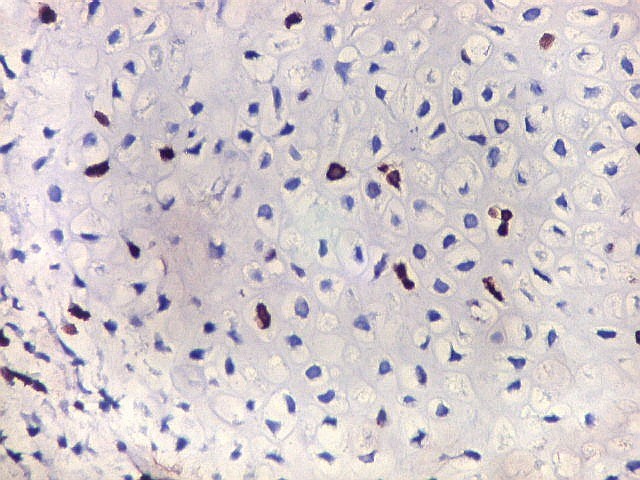
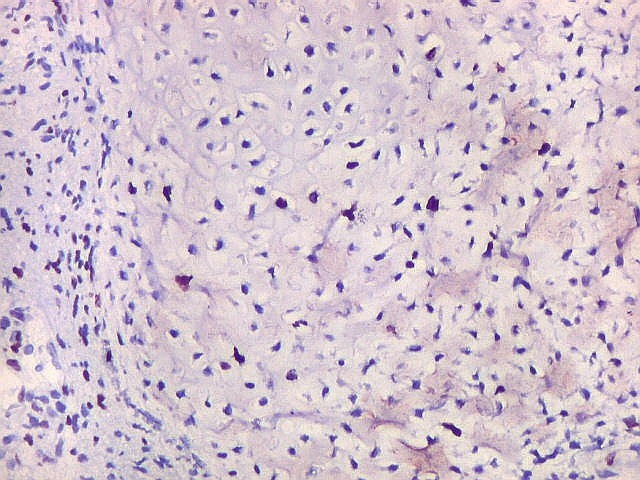
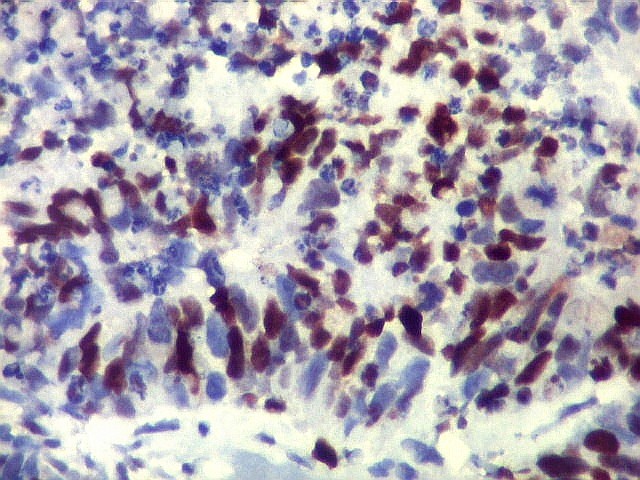
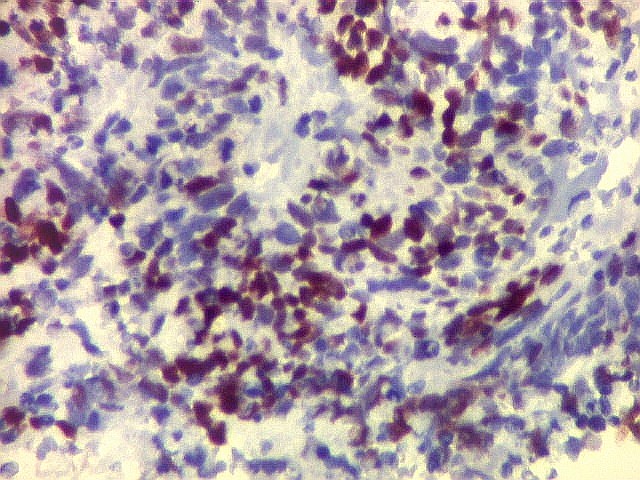
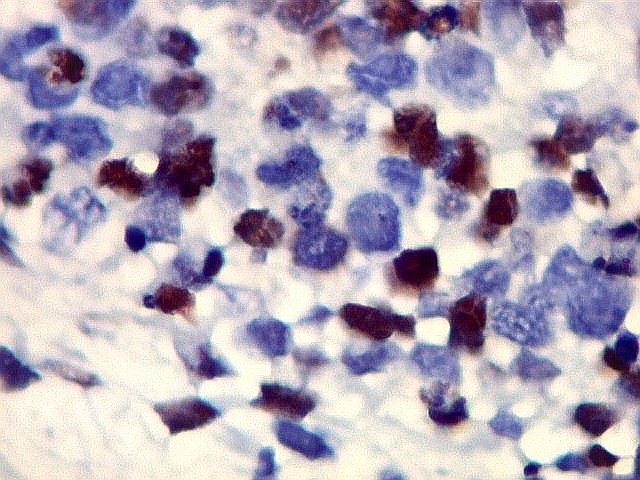
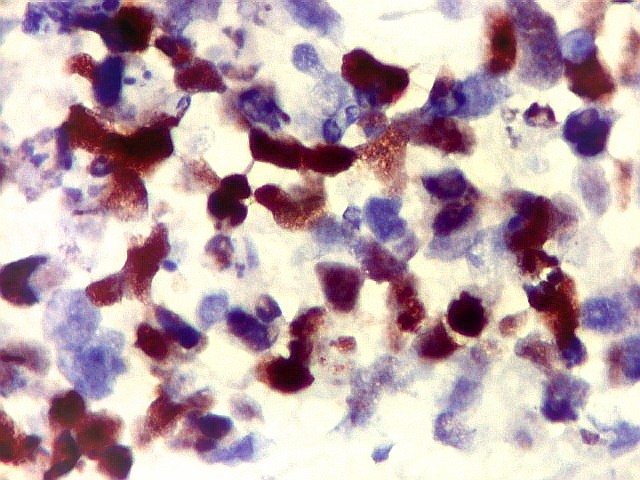
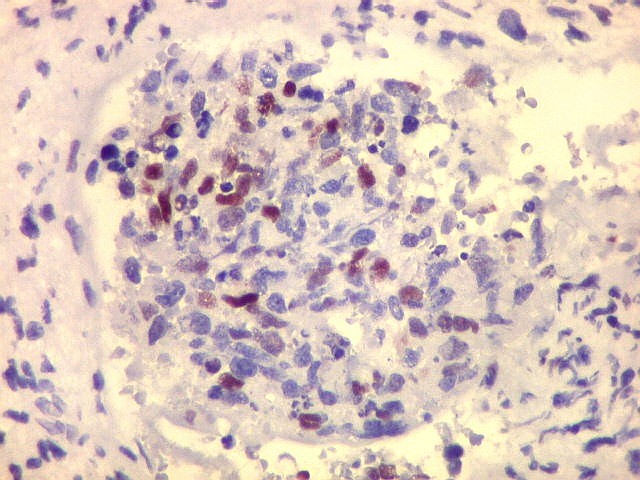
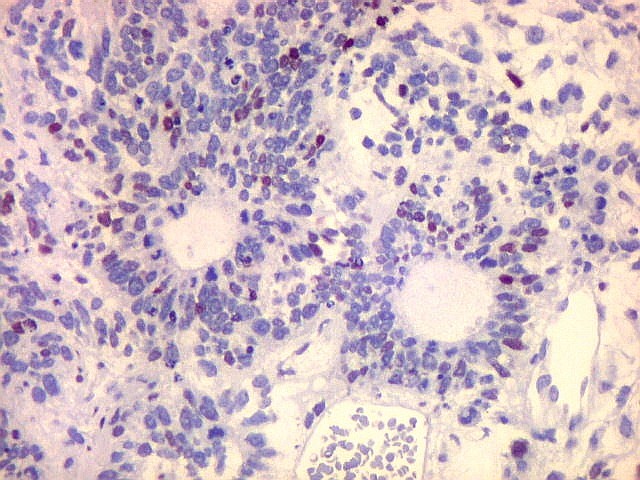
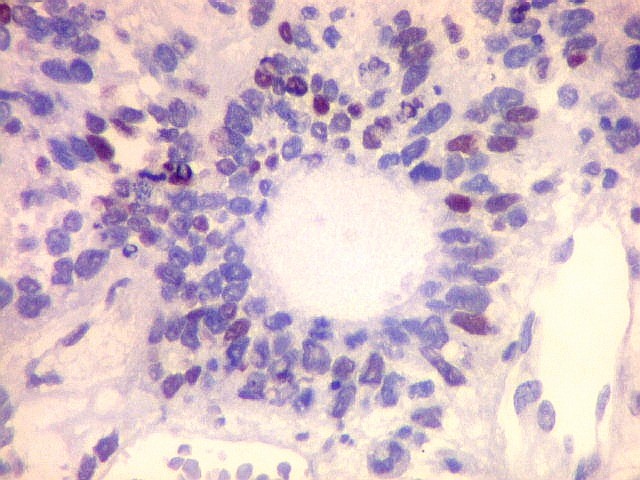
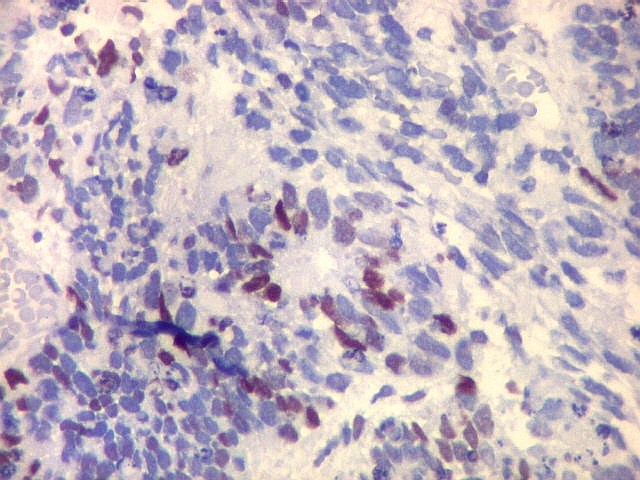
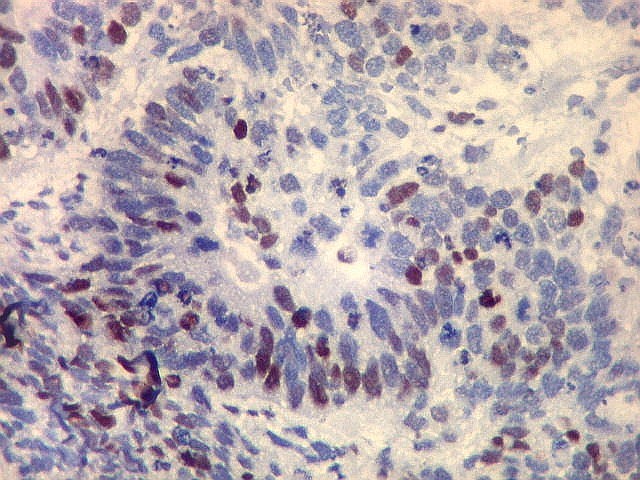
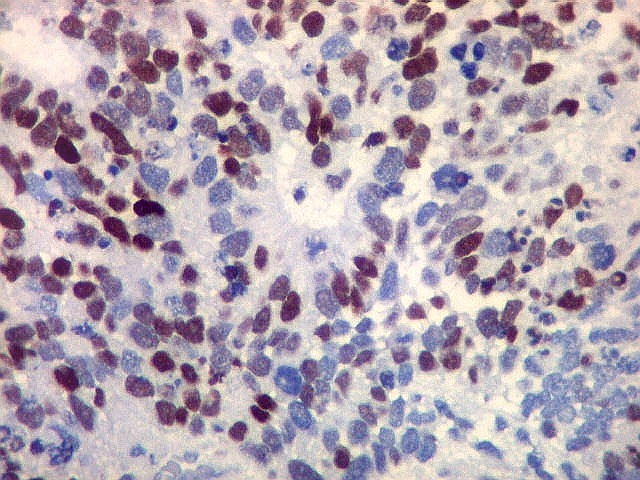
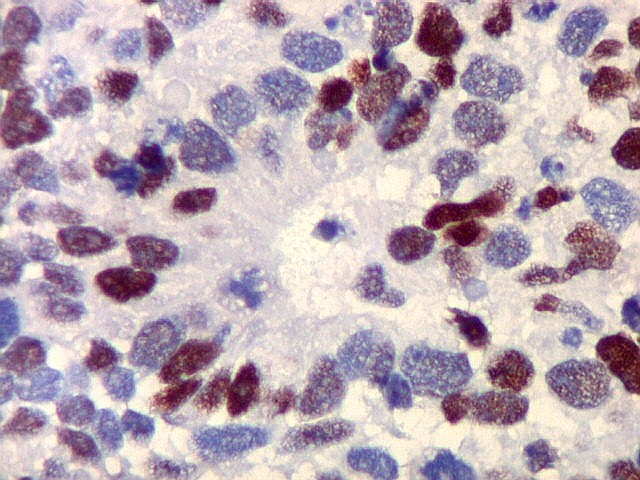
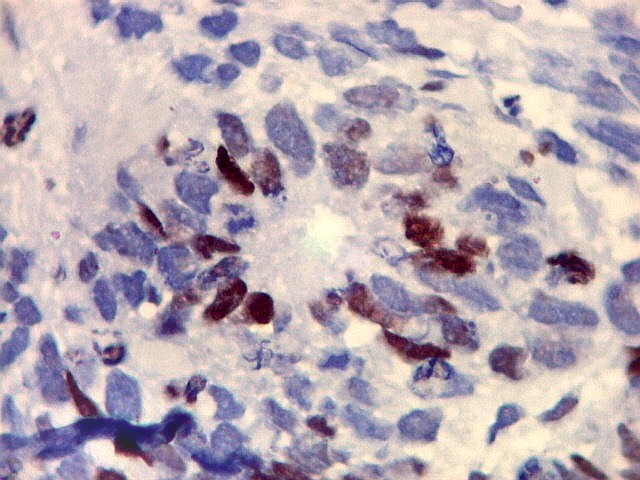
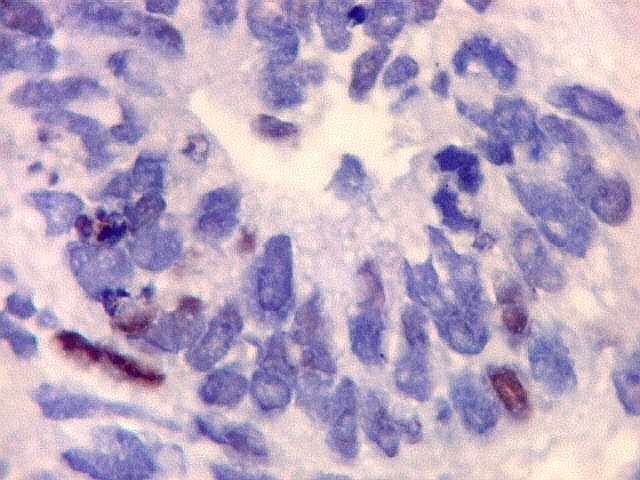
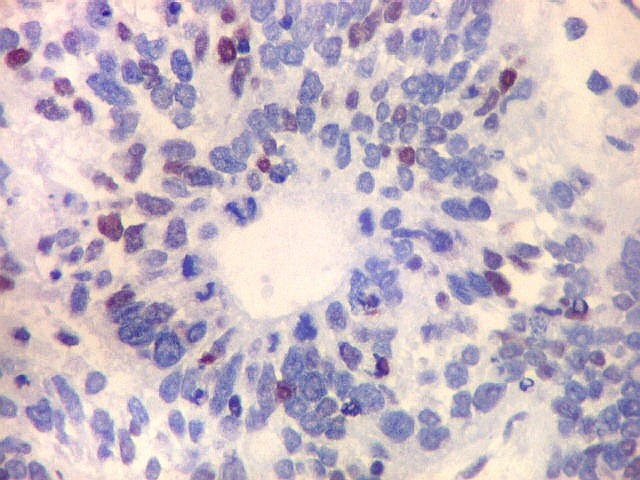
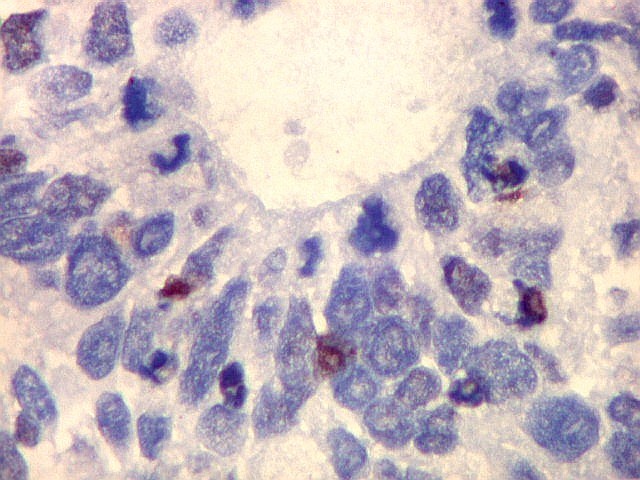
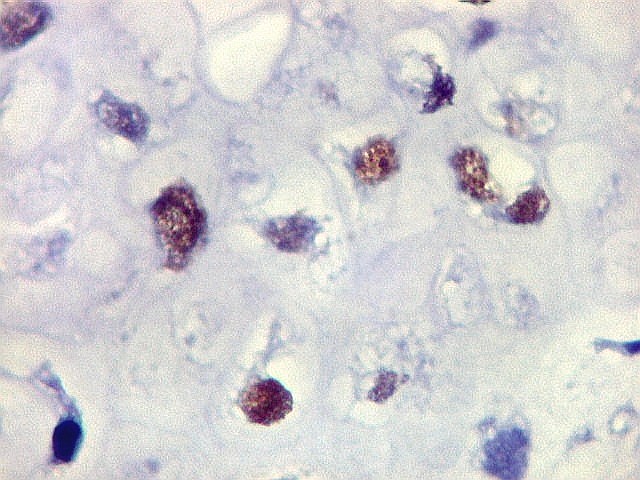
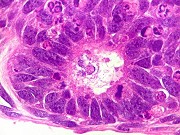
| p53. Este importante gene supressor tumoral localizado no braço curto do cromossomo 17 é essencial na manutenção da viabilidade do genoma, identificando mutações do DNA que podem resultar em tumores (considerado o 'guardião do genoma'). A proteína normal codificada pelo gene é lábil, sendo continuamente sintetizada e degradada. Mutações levam à produção de uma proteína anômala estável que se acumula e é detectada por imunohistoquímica. Esta proteína não é hábil para impedir o desenvolvimento de células cancerosas, nem para induzir apoptose das células mutadas. Neste PNET com rosetas multicamadas, há alta proporção de células p53 positivas. Para amplo texto sobre p53, consultar https://en.wikipedia.org/wiki/P53 |
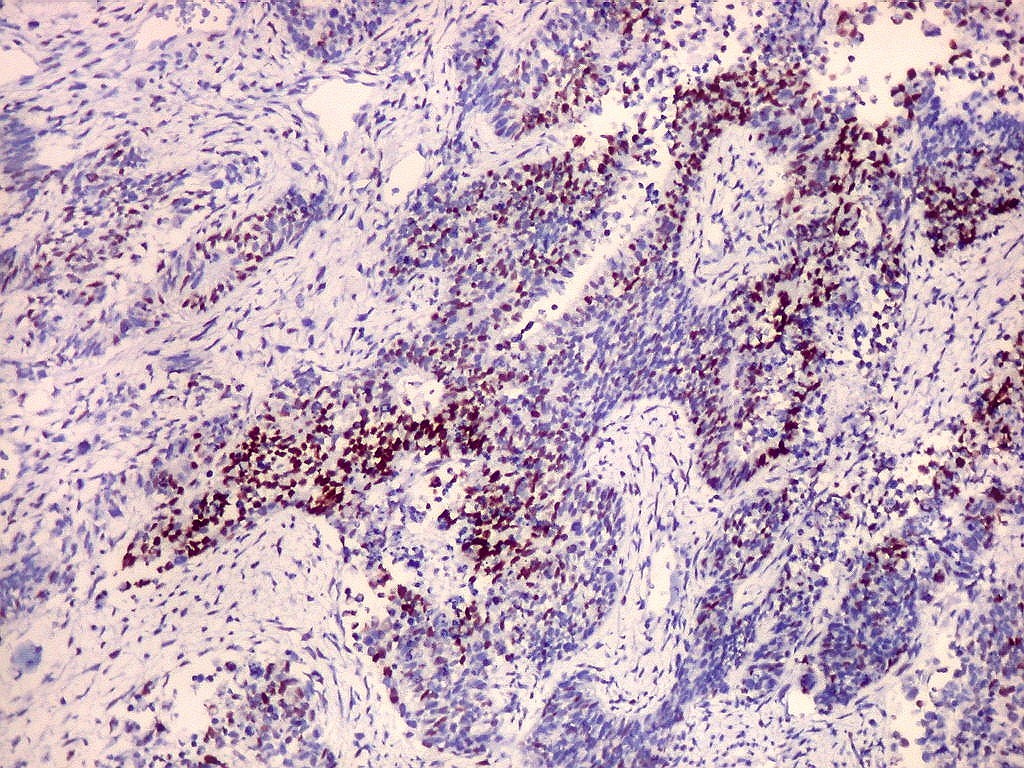 |
| p53. Neuroepitélio. | |
 |
 |
 |
 |
 |
 |
 |
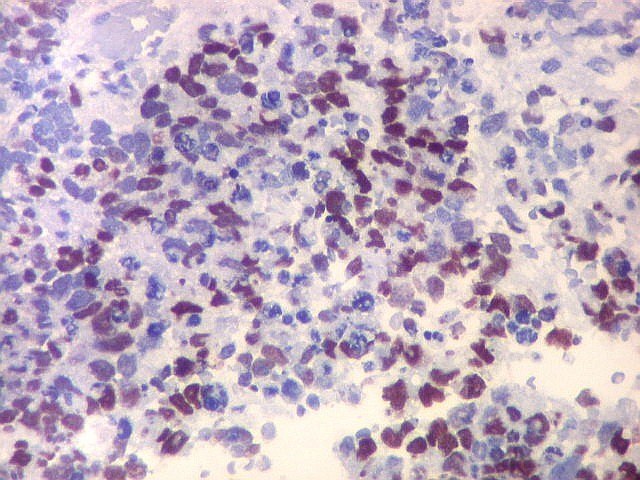 |
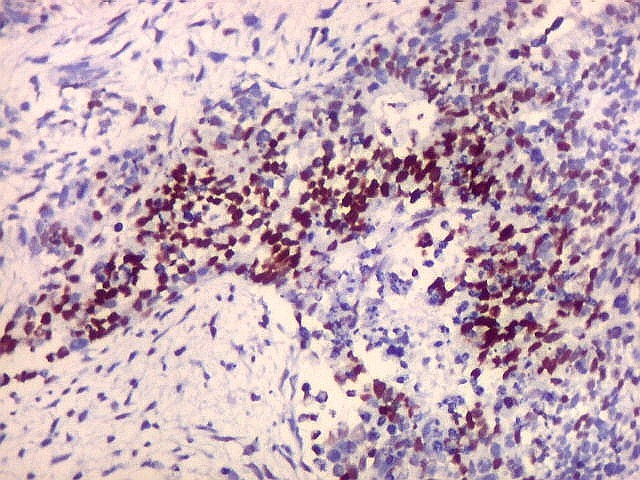
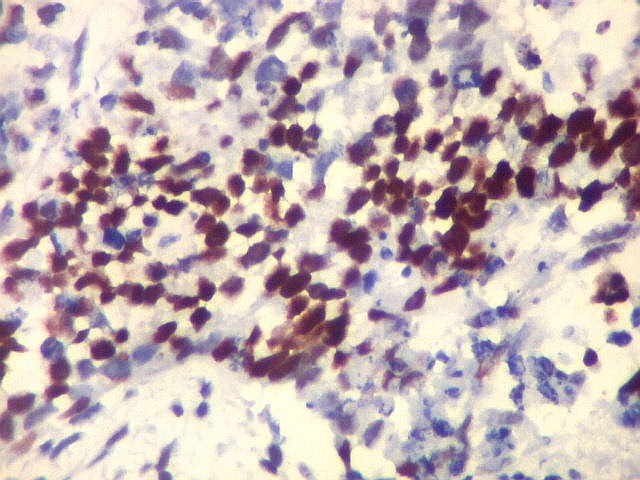
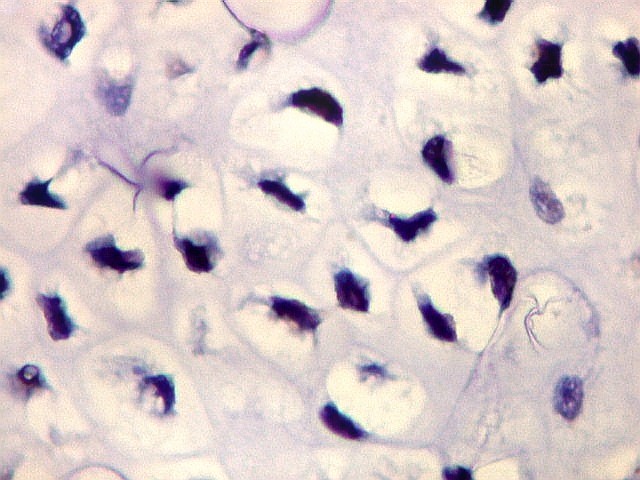
| p53. Rosetas. | |
 |
 |
 |
 |
 |
 |
 |
 |
 |
 |
| p53. Cartilagem. | |
 |
 |
 |
 |
| Anticorpos negativos. Cromogranina, neurofilamento, NeuN, EMA, HHF-35, Melan A. |
| Tumor embrionário
com rosetas multicamadas
- OMS 2016.
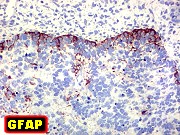
Definição. Tumor embrionário agressivo do sistema nervoso central com rosetas multiestratificadas e alterações (incluindo amplificação e fusões) no locus C19MC no cromossomo 19q13.42. Pode ocorrer no cérebro, cerebelo ou tronco cerebral e incluir vasto espectro histológico, com áreas de neurópilo neoplásico. Engloba tumores antes classificados como tumor embrionário com neurópilo abundante e rosetas verdadeiras, ependimoblastoma e meduloepitelioma. Contudo, qualquer tumor embrionário com as alterações genéticas acima qualifica para esta designação, mesmo sem as feições histopatológicas características. Todos estes tumores são graduados IV pela OMS. Idade. Quase todos casos < 4 anos, Na grande maioria < 2 anos, Igual distribuição entre sexos. Localização. Hemisférios cerebrais em 70%, maior envolvimento frontal e parieto-temporal. Podem envolver mais de um lobo e ambos hemisférios. Cerebelo e/ou tronco em 30%. Há tendência a disseminação leptomeníngea, e descreve-se invasão de tecidos moles extracranianos e metástases à distância. Microscopia. Rosetas são feição característica destes tumores. São multiestratificadas, com lúmen patente e mitoses, que tendem a ser mais numerosas próximas à luz. Descrevem-se 3 padrões morfológicos, antigamente vistos como categorias nosológicas distintas, mas que são hoje considerados ou pontos em um espectro contínuo, ou diferenciação divergente em uma entidade única. Isto devido ao caráter comum das alterações moleculares. a) Tumor embrionário com neurópilo abundante e rosetas verdadeiras. Este padrão mostra arquitetura bifásica, com agrupamentos densos de células pequenas com núcleos redondos ou poligonais, citoplasma escasso de limites imprecisos. Estes estão dispersos em grandes áreas paucicelulares de aspecto fibrilar ou semelhante a neurópilo, às vezes em arranjo fascicular, contendo células neurocíticas ou ganglionares. As áreas hipercelulares contêm numerosas mitoses e corpos apoptóticos e abrigam freqüentemente as rosetas multicamadas. b) Ependimoblastoma. Neste padrão há aglomerados e faixas de células pouco diferenciadas com rosetas multicamadas, mas não tem a matriz semelhante a neurópilo nem células ganglionares encontradas no tipo acima. c) Meduloepitelioma. Este padrão caracteristicamente apresenta-se como massa cerebral bem delimitada em crianças jovens. Apresenta arranjos papilares, trabecular ou tubulares de epitélio neoplásico pseudoestratificado, com membrana limitante externa PAS + e marcada por colágeno IV, lembrando o tubo neural primitivo. Não há cílios ou blefaroplastos na superfície luminal destes túbulos. Mitoses são abundantes, tendendo a serem localizadas próximas à superfície luminal. Zonas fora das estruturas papilares ou tubulares mostram vastos campos de células pouco diferenciadas com núcleos hipercromáticos e alta proporção núcleo-citoplasma. Pode conter grupos de rosetas multicamadas. As células tumorais variam desde células embrionárias a neurônios e astrócitos maduros. Raramente o tumor pode demonstrar diferenciação mesenquimal ou pigmento melânico. Poucos tumores após tratamento podem mostrar maturação neuronal ou glioastrocitária lembrando um tumor glioneuronal de baixo grau. Outros tumores mostram perda das feições histológicas chaves do tumor embrionário com rosetas multicamadas e podem parecer outros tumores embrionários. Imunofenótipo. O componente neuroepitelial primitivo do tumor embrionário rosetas multicamadas é intensamente reativo para nestina e vimentina. Áreas de pequenas células e rosetas verdadeiras podem mostrar expressão local de citoqueratinas, EMA e CD99, mas são geralmente negativos para marcadores neuronais e gliais. Áreas semelhantes a neurópilo marcam-se fortemente para sinaptofisina, neurofilamento, e NeuN. GFAP marca células isoladas lembrando astrócitos reativos. Há forte e difusa reação nuclear para INI1, afastando ATRT. Ki-67 varia entre 20 e 80%, com maior expressão nas áreas altamente celulares. Origem. População celular primitiva na zona subventricular. Prognóstico. São tumores de rápido crescimento, agressivos, com tendência a recidiva local e disseminação pelo neuroeixo, relatando-se inclusive metástases fora do sistema nervoso central. Tempos de sobrevida são em média de 12 meses após combinação de terapias. Em casos muito raros com longa sobrevida observou-se diferenciação neuronal pós-tratamento, indicando melhor prognóstico. Ver caso neste site : imagem (1)(2), patologia (1)(2). Fonte.
Korshunov A, et al. Embryonal tumour with multilayered rosettes,
C19MC-altered. In WHO Classification of Tumours
of the Central Nervous System. 4th Revised Ed. Louis DN, et
al, editors. International Agency for Research on Cancer, Lyon, 2016.
pp 201-4.
|
| Agradecimentos. Caso do Centro Infantil Boldrini, Campinas, SP. Preparações histopatológicas e imunohistoquímicas pelos técnicos do Laboratório de Patologia do Centro Boldrini - Srs. Aparecido Paulo de Moraes e Irineu Mantovanelli Neto. |
| Para mais imagens deste caso e texto: | |||
| RM | HE | Masson | IH - GFAP |
 |
 |
 |
 |
| IH - sinaptofisina, MAP2 | IH - vimentina, nestina, AE1AE3, 1A4 | IH - CD56, CD99, S100, HMB45, INI1 | IH - CD34, Ki67, p53 |
 |
 |
 |
 |
| Textos sobre PNETs supratentoriais (1) (2) | Tumor embrionário com rosetas em multicamadas (1) (2) | Ependimoblastomas | Pineoblastomas (1) (2) | Características de imagem dos PNETs |
| Neuropatologia
- Graduação |
Neuropatologia -
Estudos de casos |
Neuroimagem
- Graduação |
Neuroimagem -
Estudos de Casos |
Roteiro
de aulas |
Textos
de apoio |
Correlação
Neuropatologia - Neuroimagem |
| Índice alfabético - Neuro | Adições recentes | Banco de imagens - Neuro | Textos ilustrados | Neuromuscular | Patologia - outros aparelhos | Pages in English |
|
|