|
|
|
|
|
|
|
|
| Masc. 36 a. Clique para RM, HE, destaques da imunohistoquímica, GFAP, vimentina, S-100, NF, CD34, CD99, 1A4, Ki67, p53. |
| Destaques da imunohistoquímica. | ||
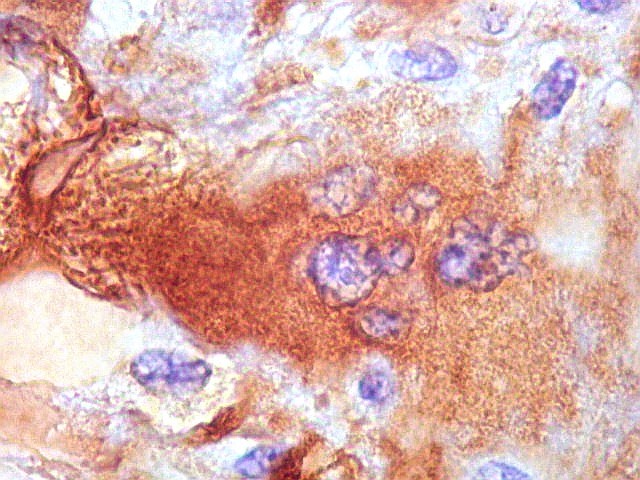
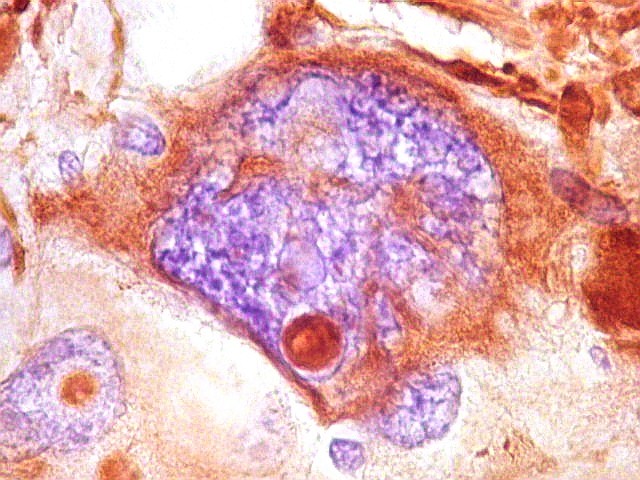
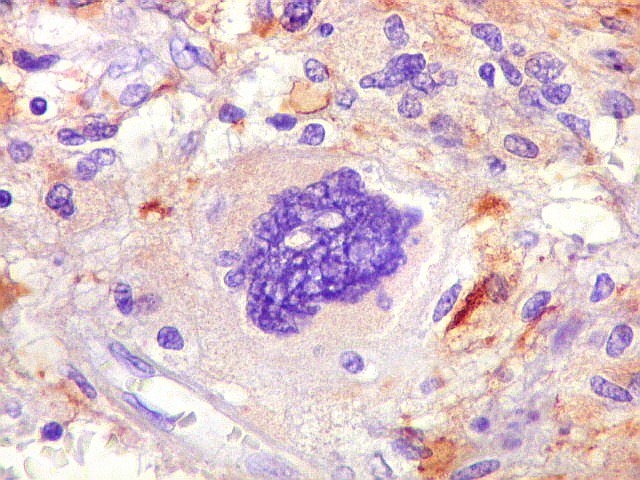
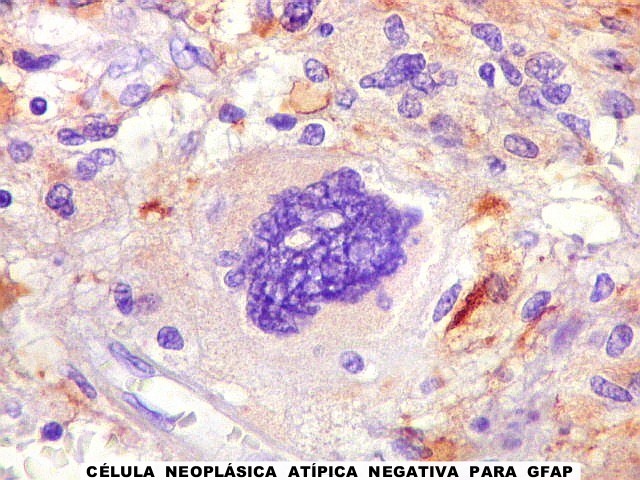
| GFAP. Células atípicas positivas | Pseudoinclusões intranucleares | Células atípicas negativas |
 |
 |
 |
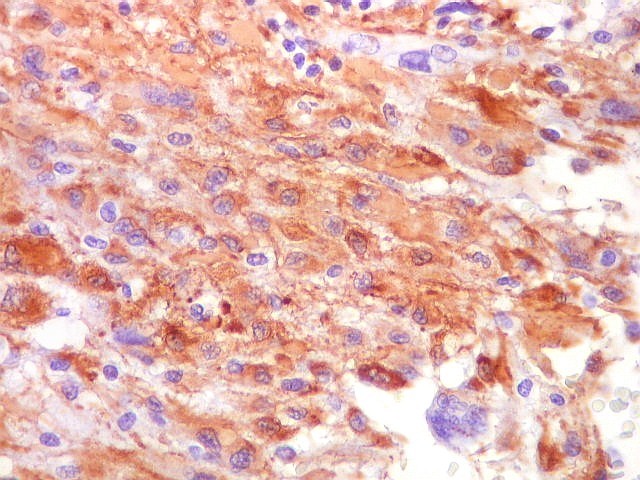
| Células menores lembrando oligodendrócitos | Mitoses raras, atípicas | Vasos - escassa proliferação endotelial, ocasional obstrução da luz |
 |
 |
 |
| VIM. Células atípicas positivas | Pseudoinclusões intranucleares | Células atípicas negativas |
 |
 |
 |
| Células menores (aqui com citoplasma claro) lembrando oligodendrócitos | Mitoses raras, atípicas | Vasos - raro exemplo de pseudoglomérulo |
 |
 |
 |
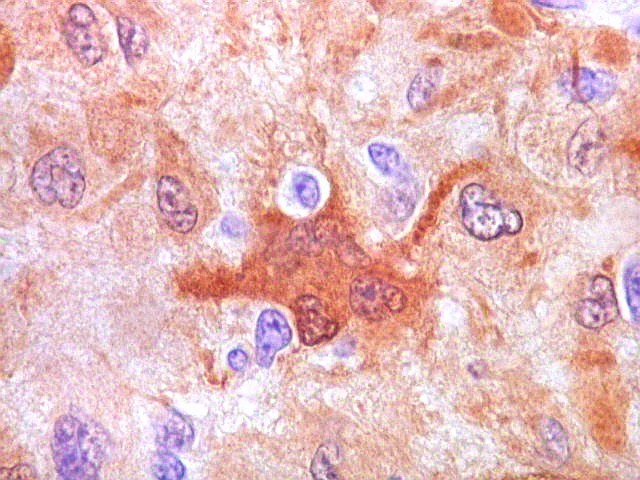
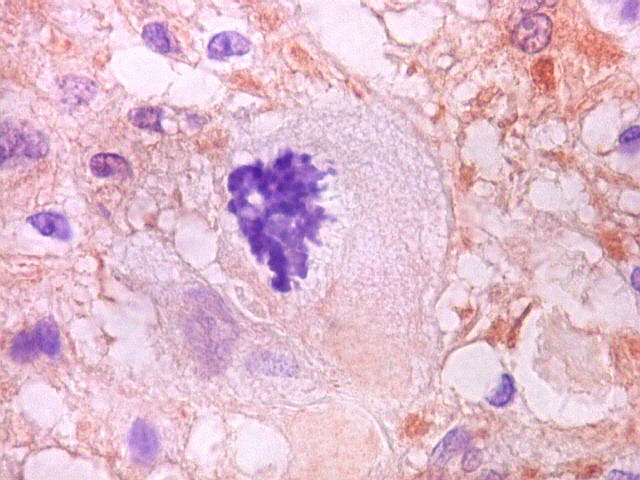
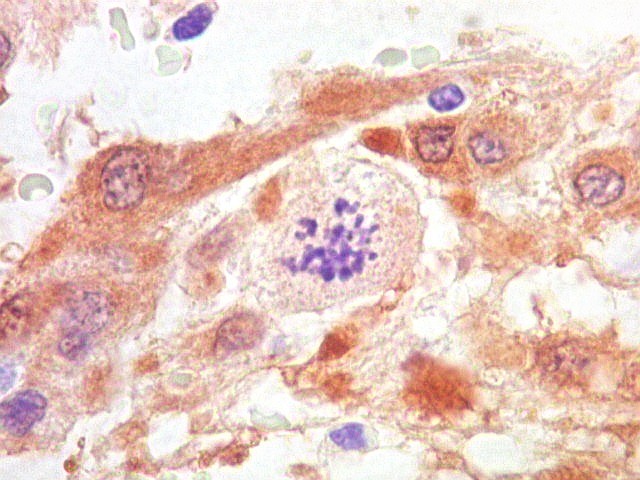
| S-100. Células atípicas positivas | Células atípicas negativas | Mitoses raras, atípicas |
 |
 |
 |
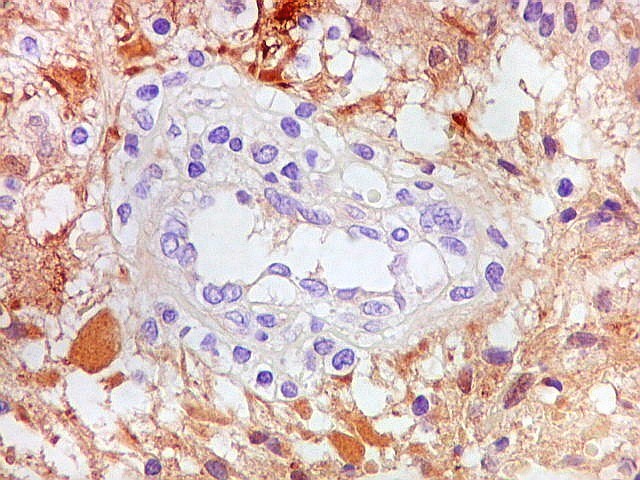
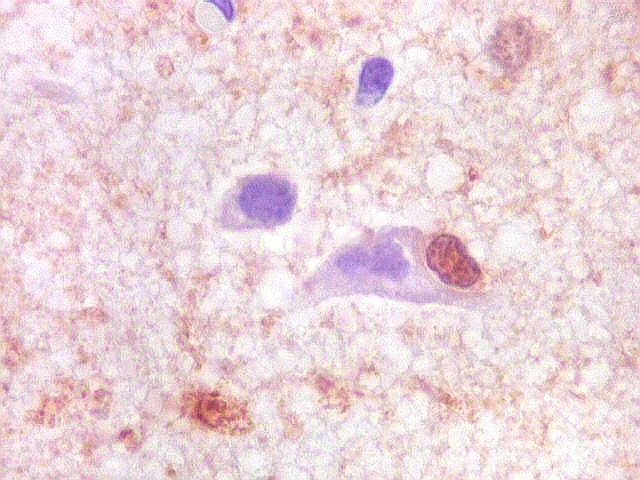
| Vasos - escassa proliferação endotelial, ocasional obstrução da luz | Córtex cerebral normal, controle interno. Positividade em astrócitos (inclusive nuclear), negativo em neurônios | NF. Negativo no tumor. Ausência de caráter infiltrativo |
 |
 |
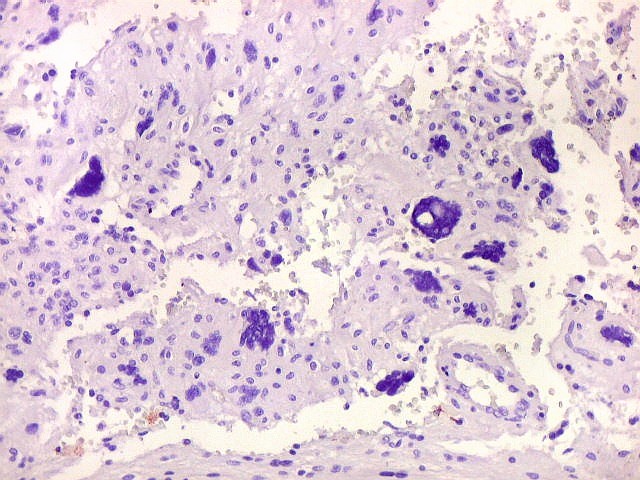 |
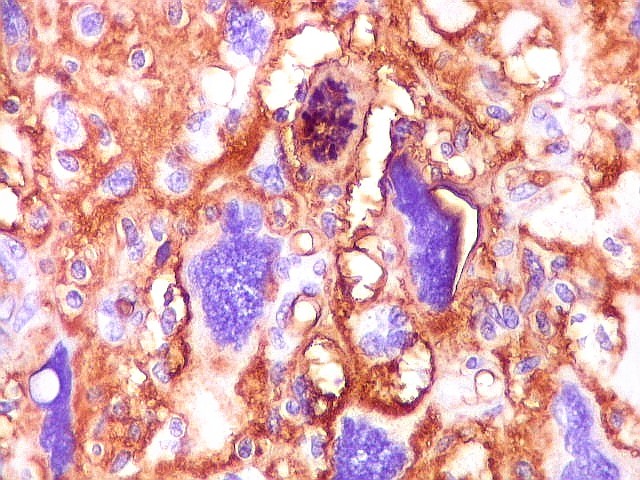
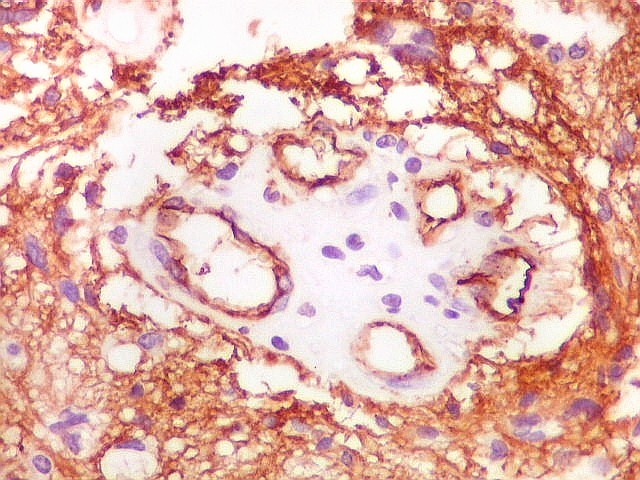
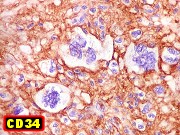
| CD34. Positivo universalmente em padrão membrana em células neoplásicas | CD34. Vasos. Córtex cerebral normal | CD99. Positivo universalmente em padrão membrana em células neoplásicas |
 |
 |
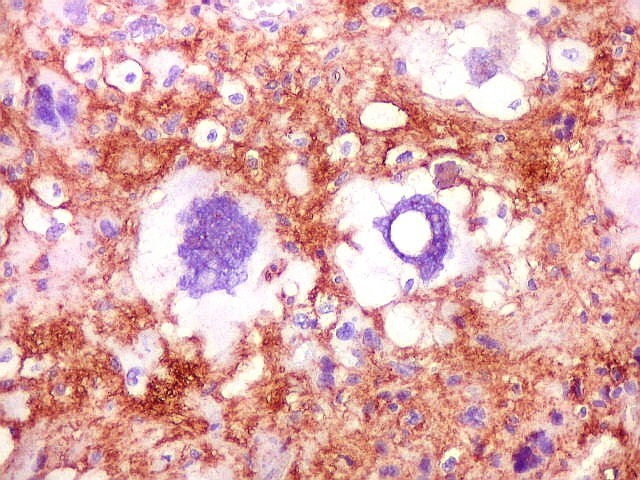 |
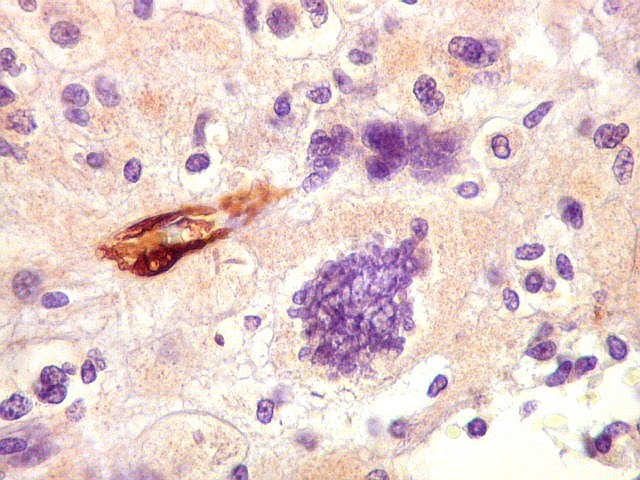
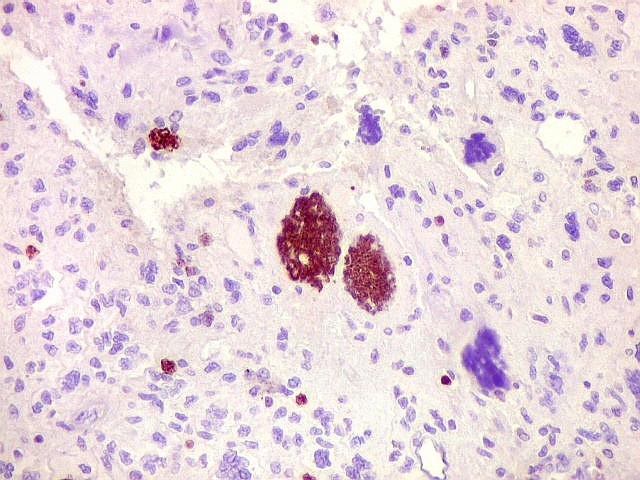
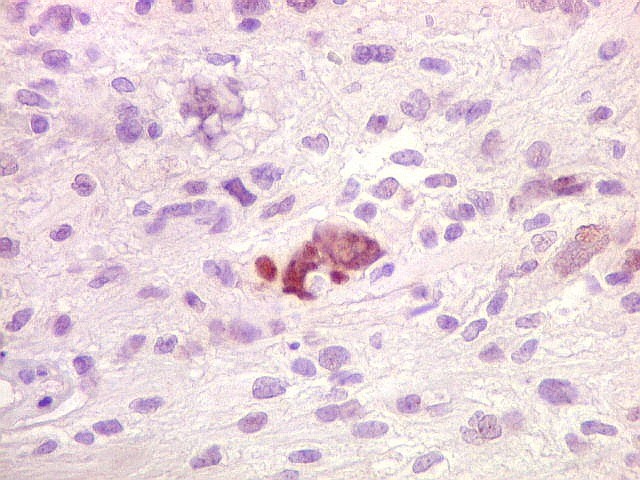
| 1A4. Positivo nos vasos, negativo nas células neoplásicas | Ki-67. Positividade em cerca de 3 a 5% dos núcleos das células neoplásicas. | p53. Positivo só em raríssimos núcleos |
 |
 |
 |
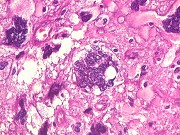
| Destaques da histologia HE. | ||
|
|
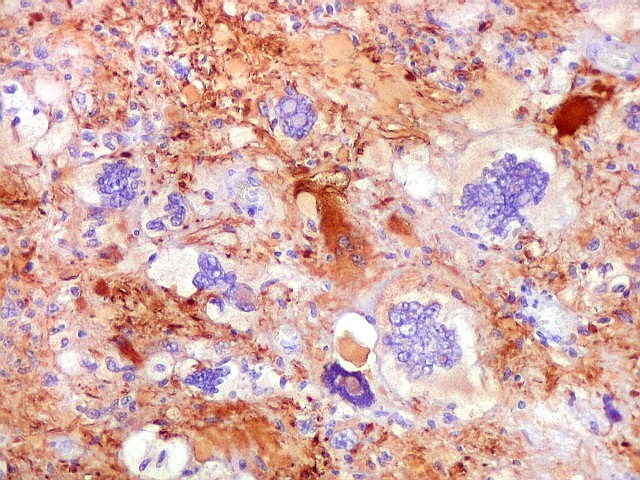
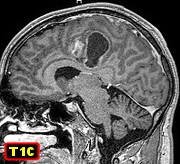
| GFAP. Positividade para GFAP (proteína glial ácida fibrilar, ou glial fibrillary acidic protein, um filamento intermediário próprio de astrócitos) atesta o tumor como de linhagem astrocitária, portanto um astrocitoma. O caráter bem delimitado da lesão na RM, sólido-cístico, com impregnação na parte sólida e parede do cisto, escasso edema perilesional e pouco efeito de massa são compatíveis com xantoastrocitoma pleomórfico. No GFAP, chama atenção o caráter variável da positividade, com células marcadas e não marcadas lado a lado. O mesmo ocorre com vimentina e S-100. | |
 |
 |
 |
 |
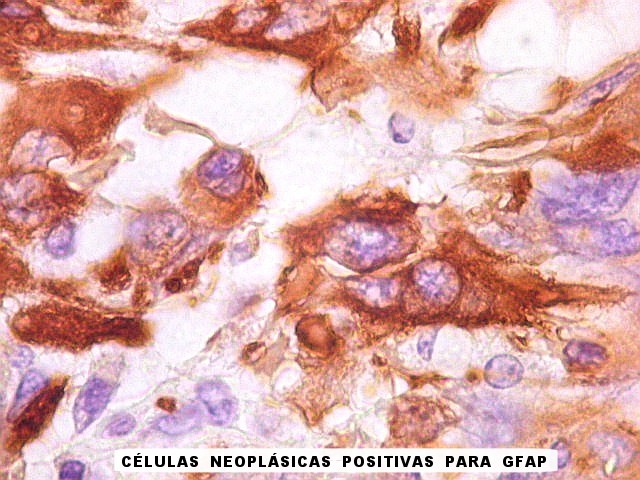
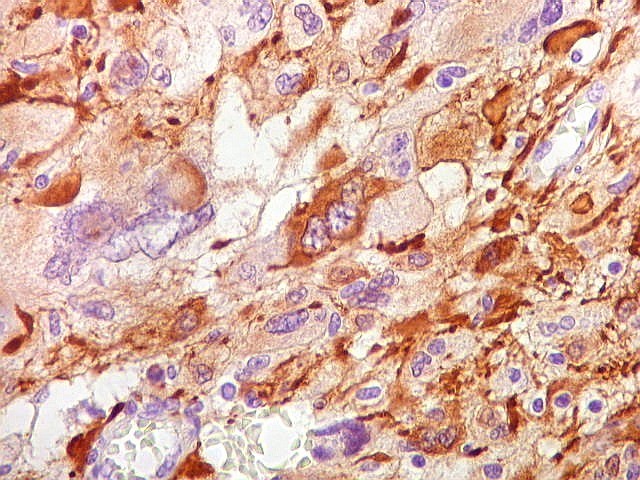
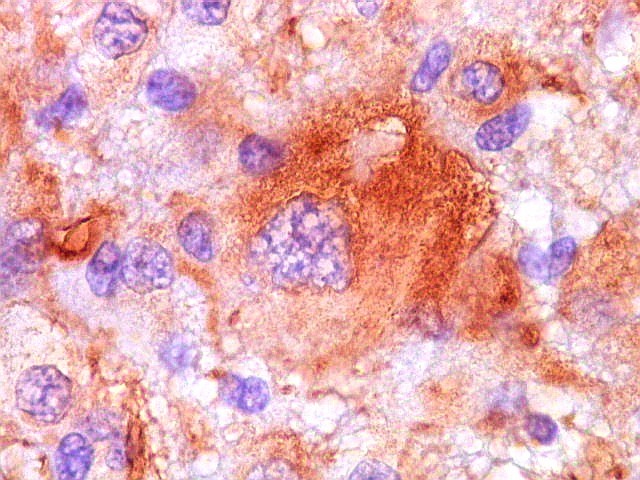
| GFAP. Células atípicas positivas. | |
 |
 |
 |
 |
 |
 |
 |
 |
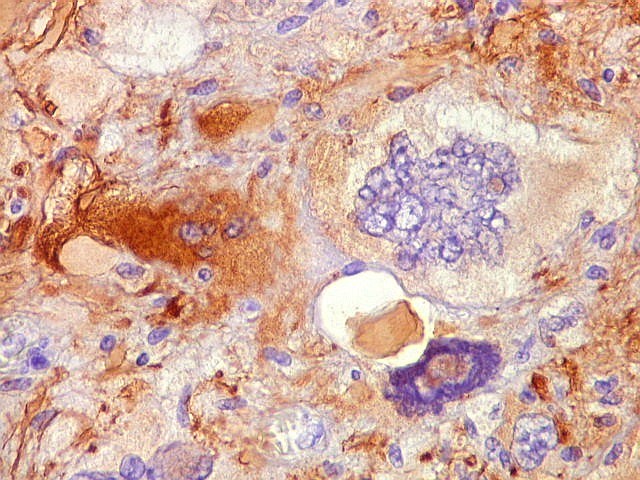
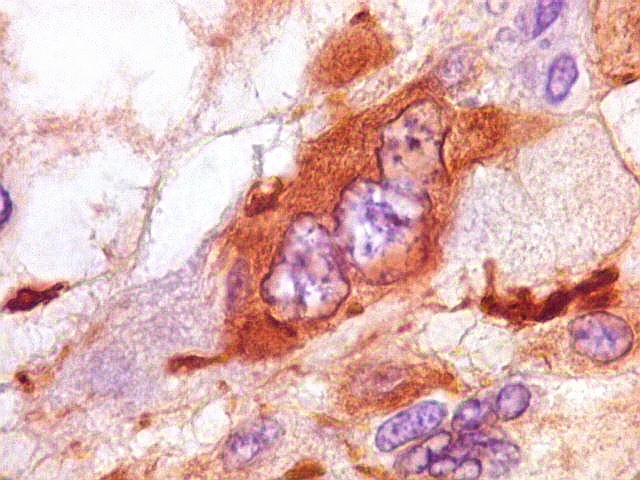
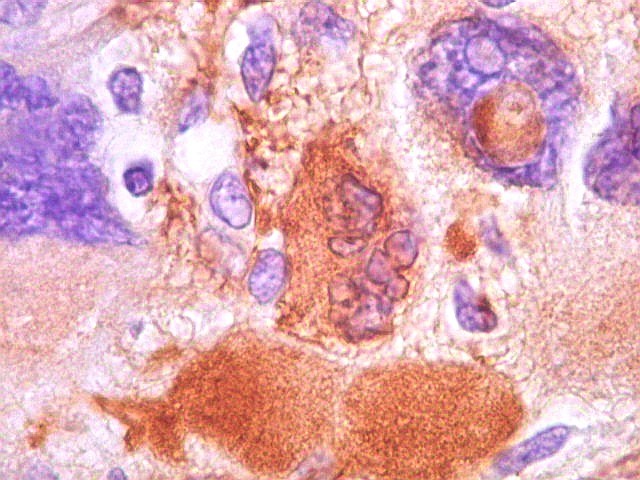
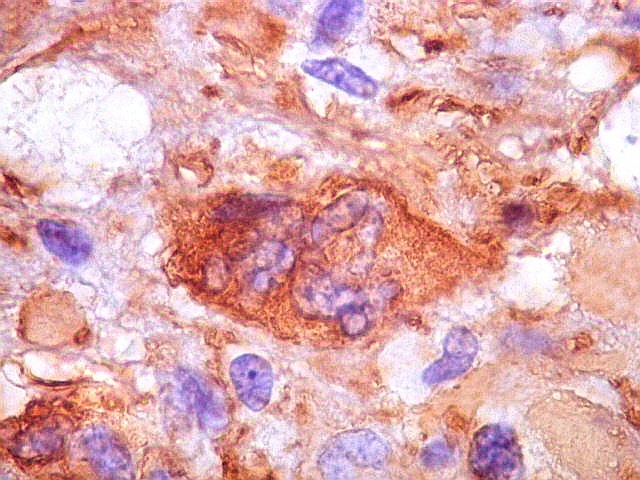
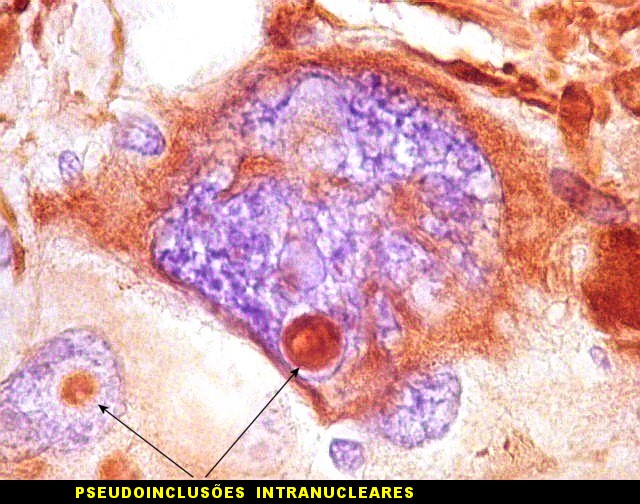
| GFAP.
Pseudoinclusões.
Estas formações que parecem intranucleares são positivas para GFAP, demonstrando sua natureza citoplasmática. A continuidade entre a pseudoinclusão e o citoplasma está fora do plano de corte. Ver também VIM. |
 |
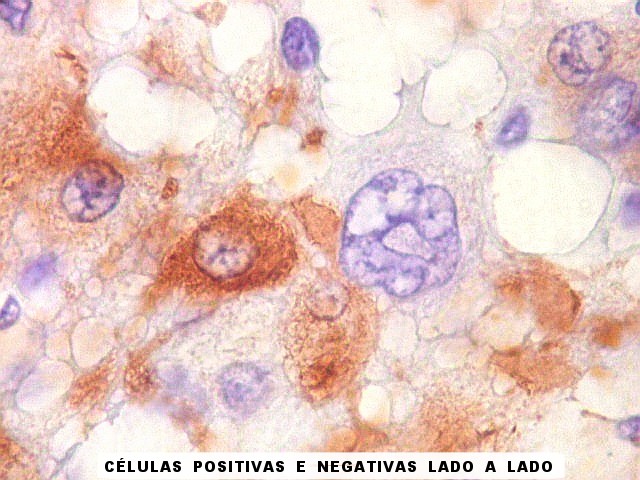
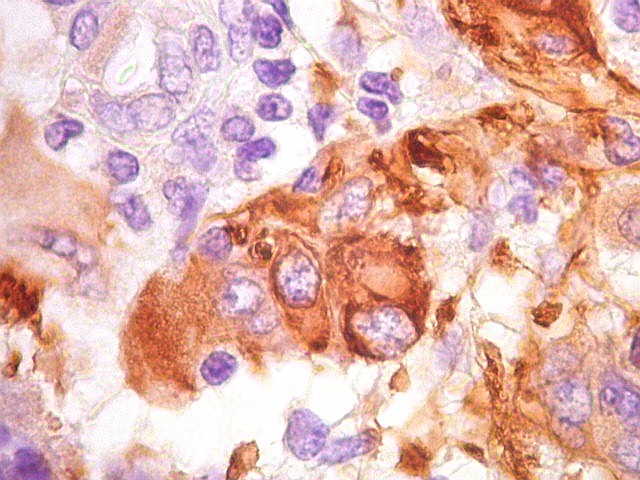
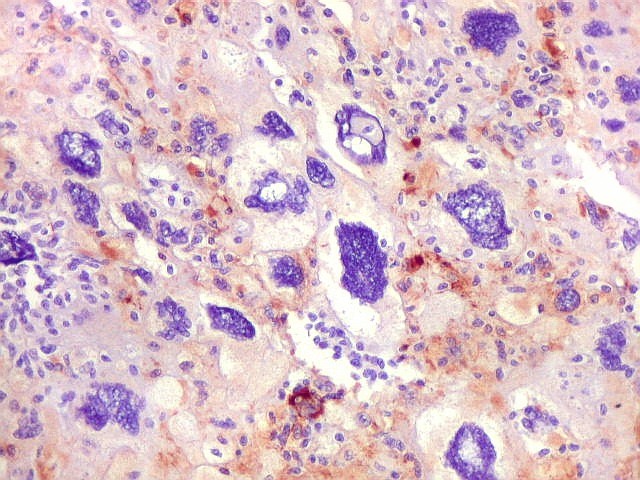
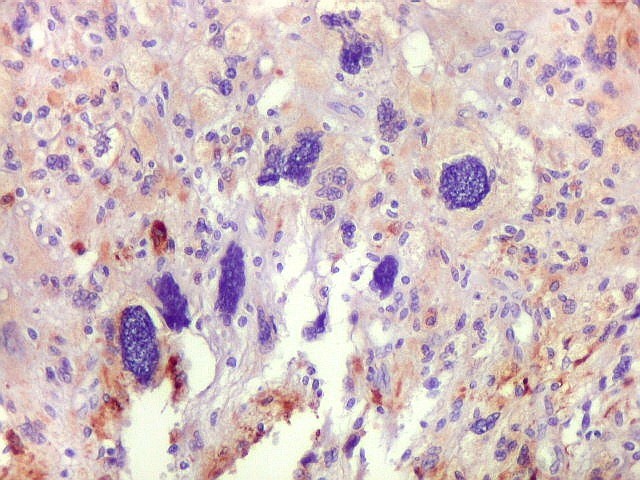
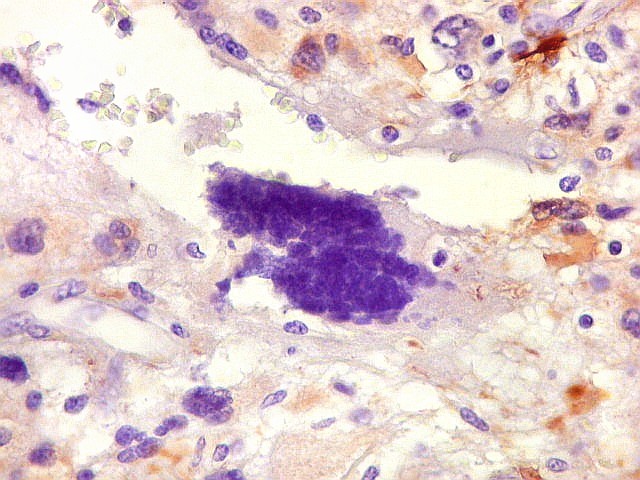
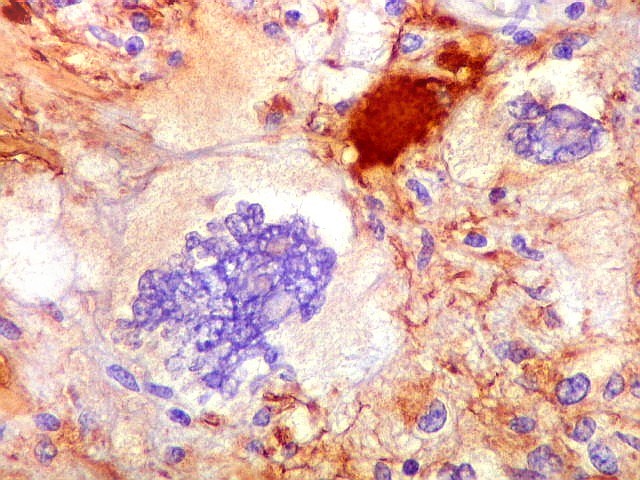
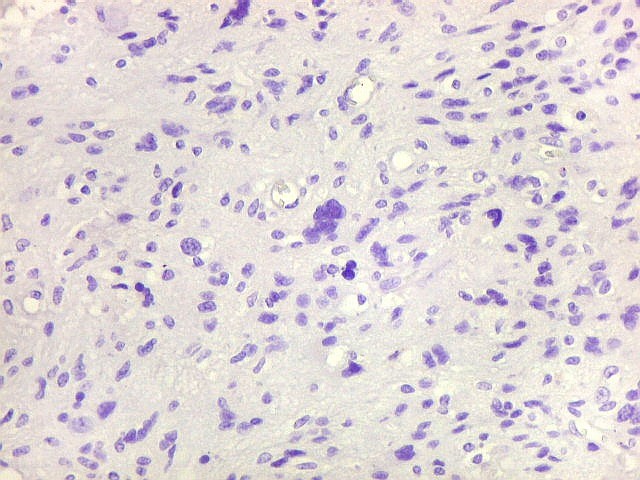
| GFAP. Células atípicas negativas. É digno de nota que muitas das células altamente atípicas foram negativas para GFAP. O mesmo se observou para VIM e S-100. Em todos campos havia pequenas áreas positivas, atestando a validade da reação. | |
 |
 |
 |
 |
 |
 |
 |
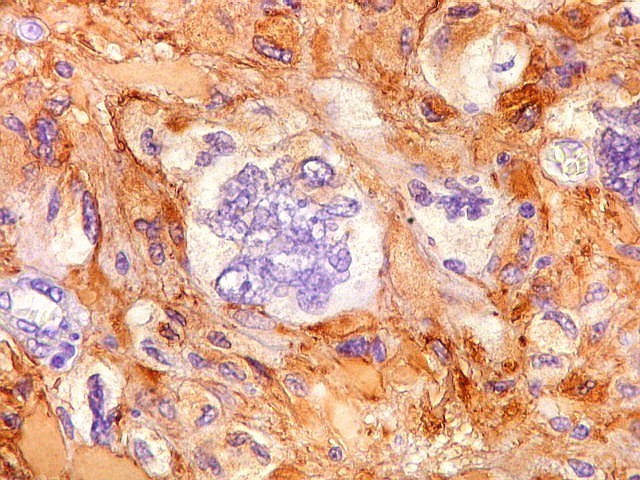 |
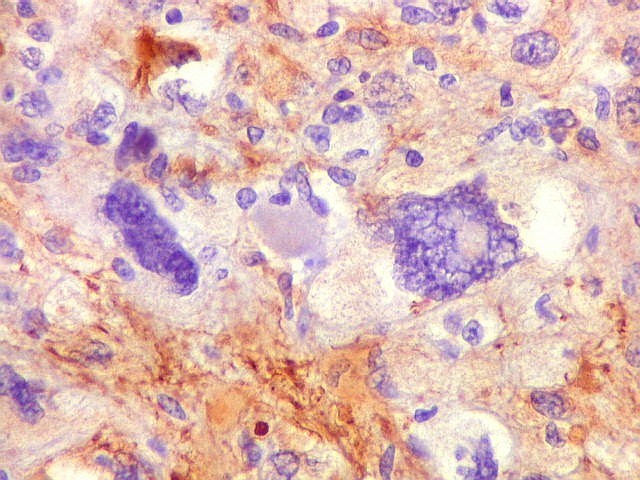
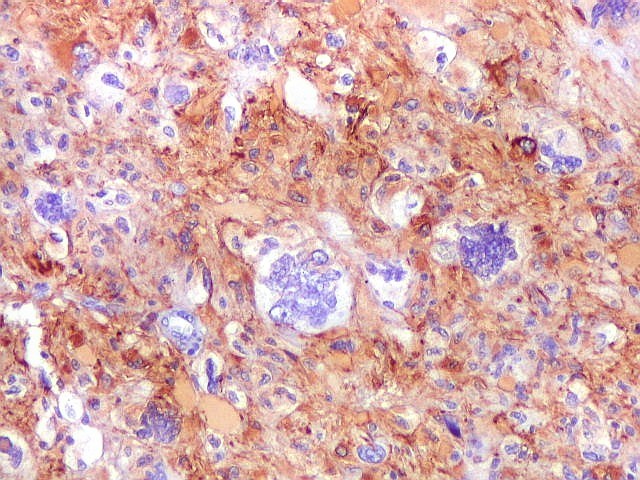
| GFAP. Células menores, lembrando oligodendrócitos. Estas células regulares, praticamente sem atipias, eram variavelmente positivas para GFAP. | |
 |
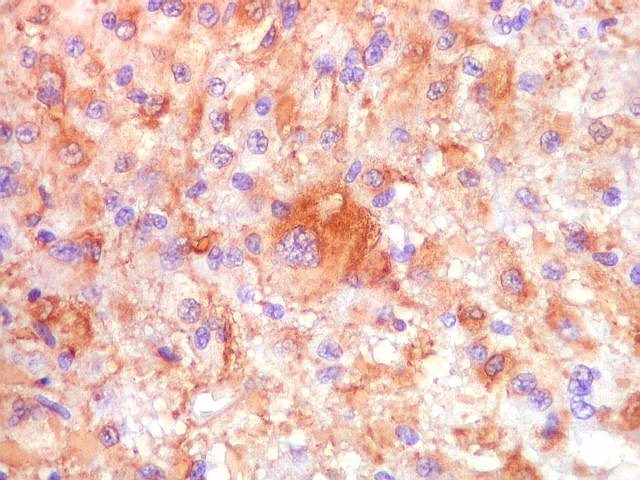 |
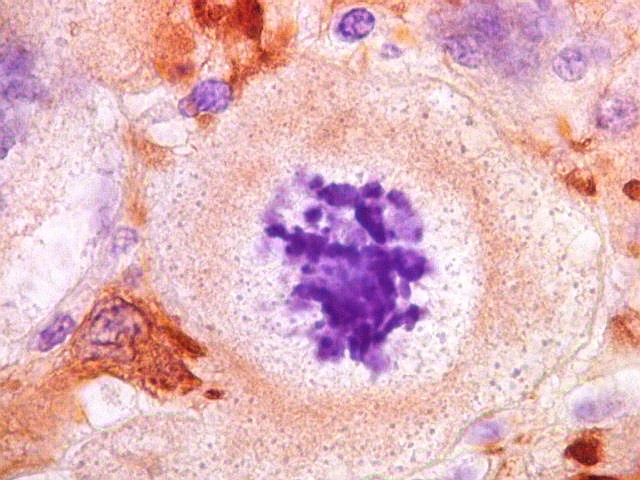
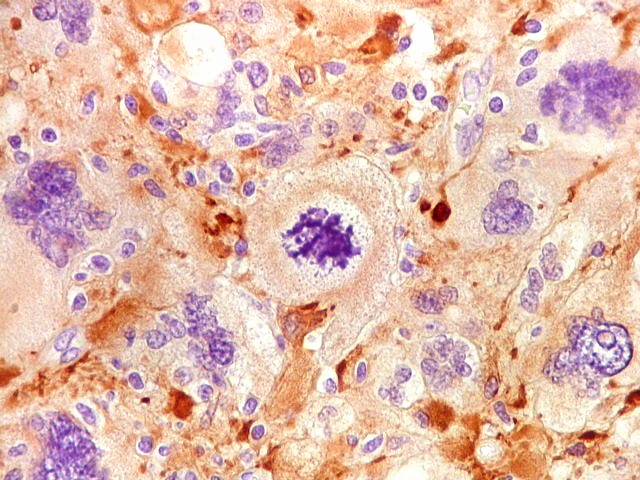
| GFAP. Mitoses. Poucas mitoses foram observadas, sendo a figura atípica abaixo a mais representativa. | |
 |
 |
| GFAP.
Vasos.
Proliferação endotelial era pouco notável. No pequeno vaso ao lado, as células têm aspecto ativado (núcleo grande e frouxo), mas a luz está preservada. Ver VIM, S-100 e CD34. |
 |
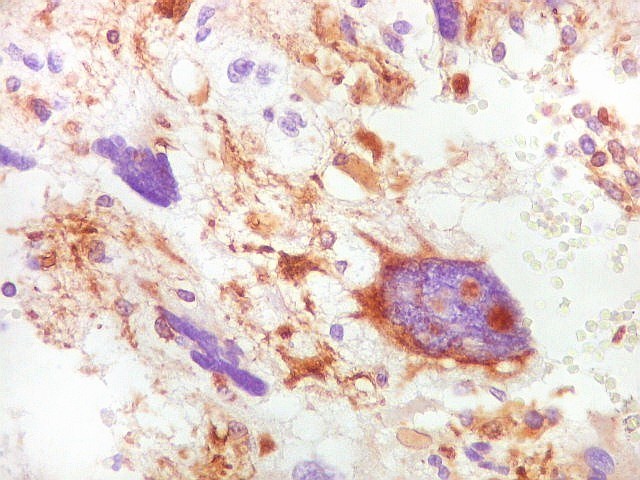
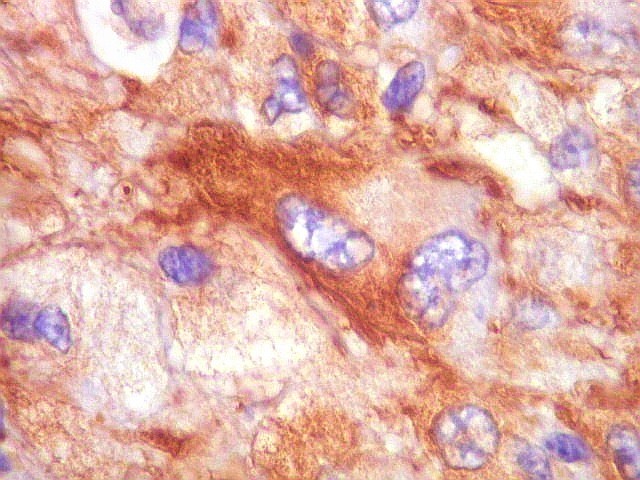
| VIM. Células atípicas positivas. Positividade para vimentina é feição habitual de astrócitos, neoplásicos ou não, e grosseiramente faz paralelo com a expressão de GFAP. | |
 |
 |
 |
 |
 |
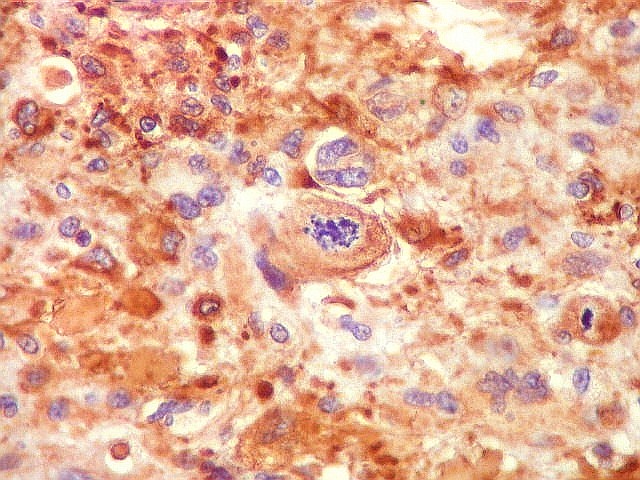 |
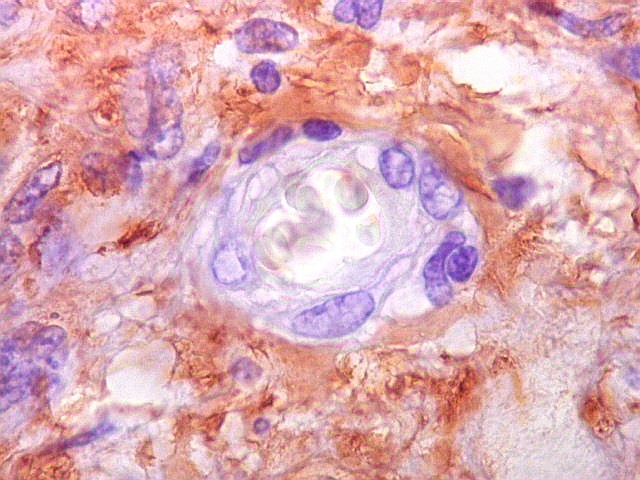
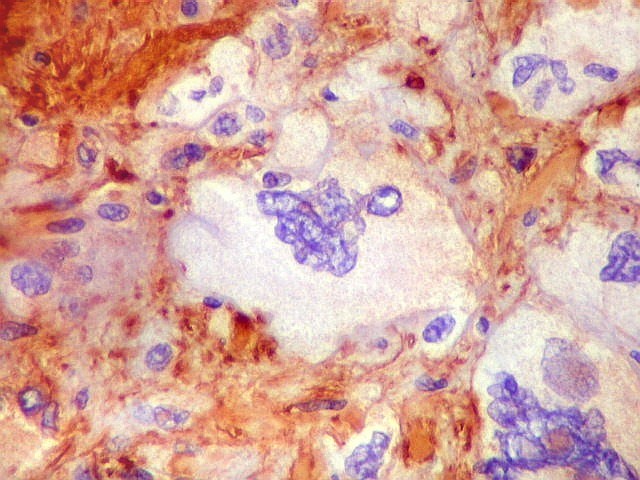
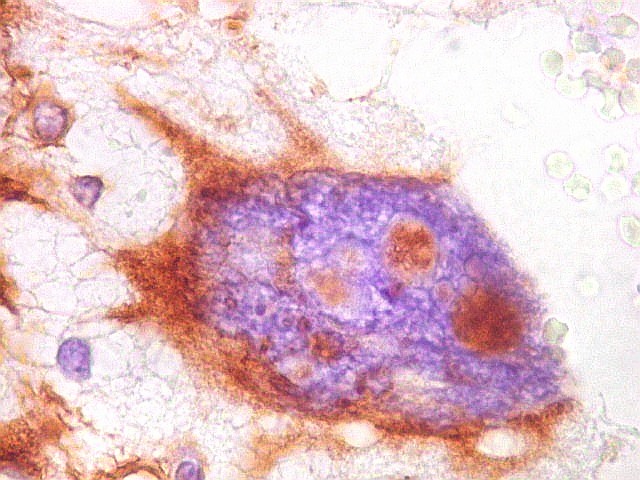
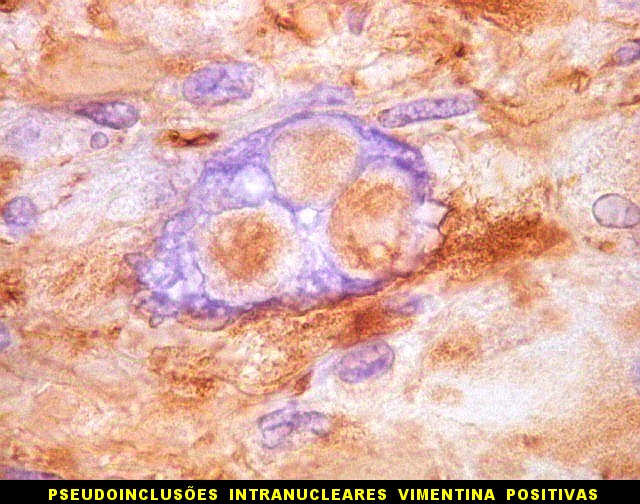
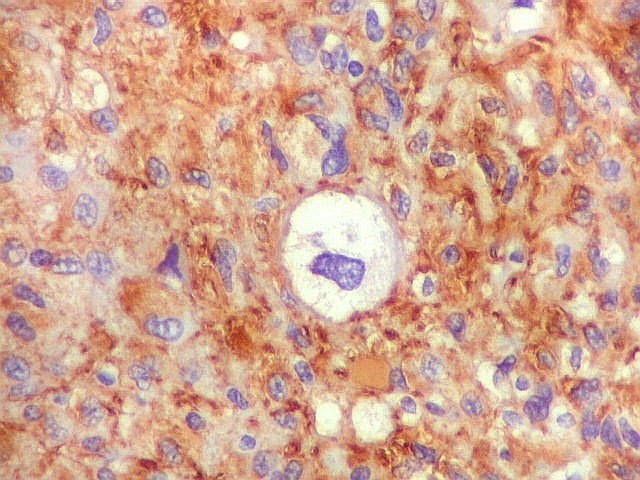
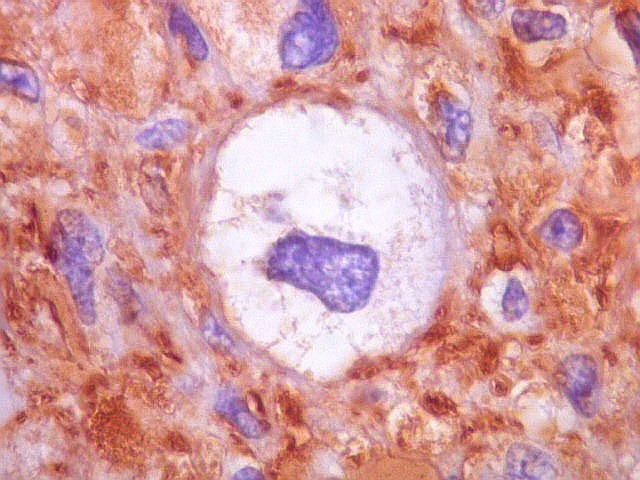
| VIM.
Pseudoinclusões.
Insinuações de citoplasma em dobras da membrana nuclear são positivas para vimentina, um filamento intermediário exclusivamente citoplasmático. Ver também com GFAP. |
 |
 |
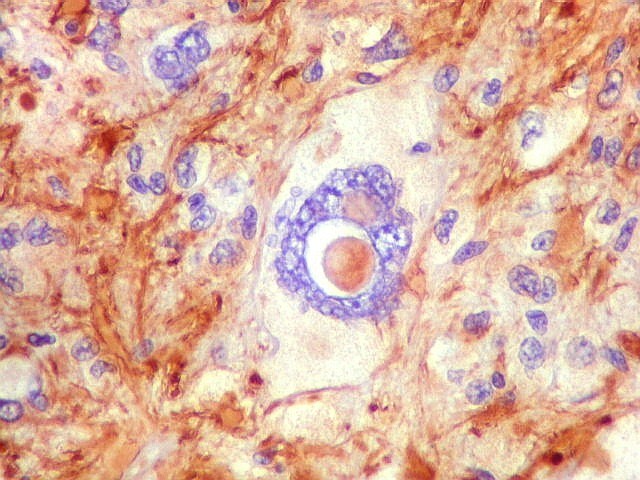 |
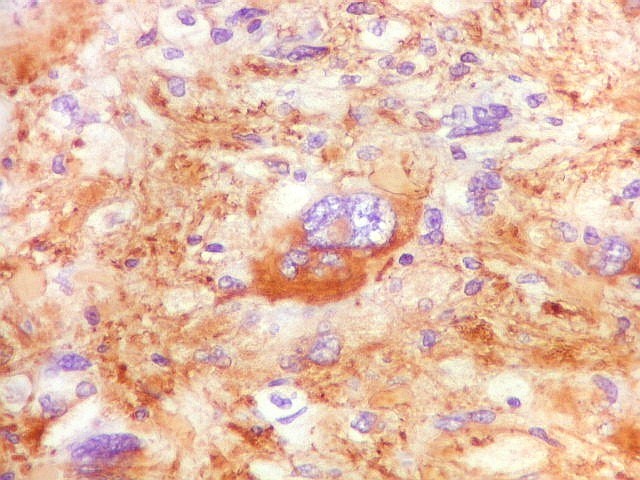
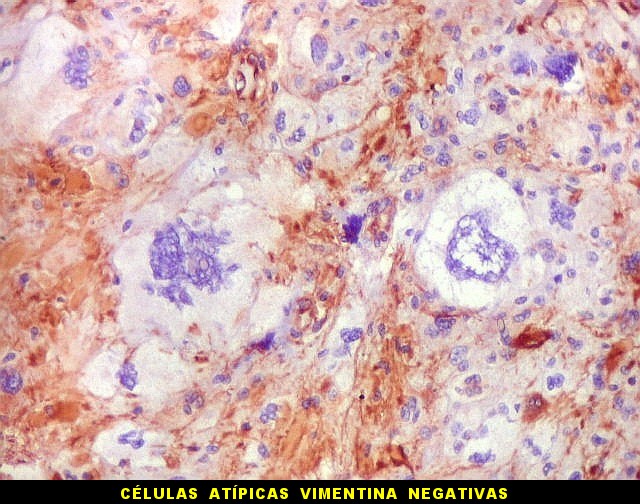
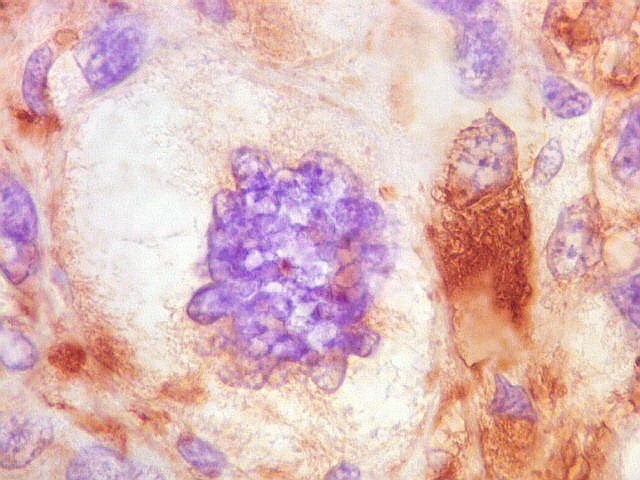
| VIM. Células atípicas negativas. Como com GFAP acima, várias das células mais atípicas eram negativas para vimentina. A título de especulação, sugerimos que estas células seriam de tal forma aberrantes, tanto morfologica- quanto funcionalmente, a ponto de não expressar moléculas do citoesqueleto tão básicas como vimentina ou GFAP. | |
 |
 |
 |
 |
 |
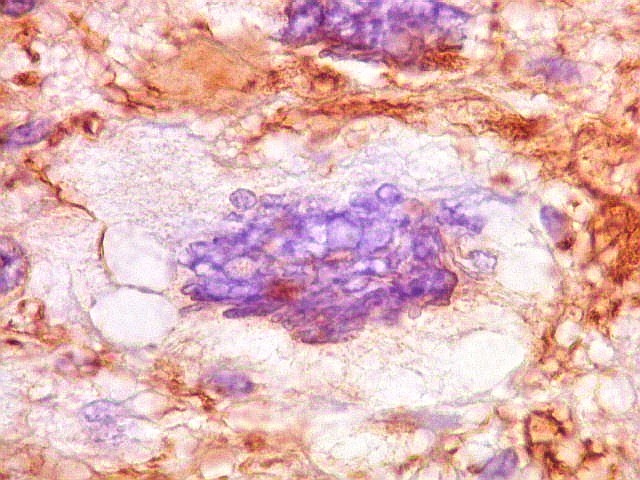 |
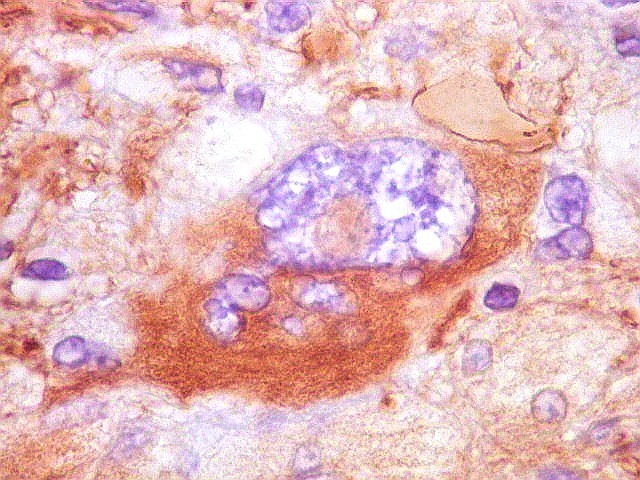
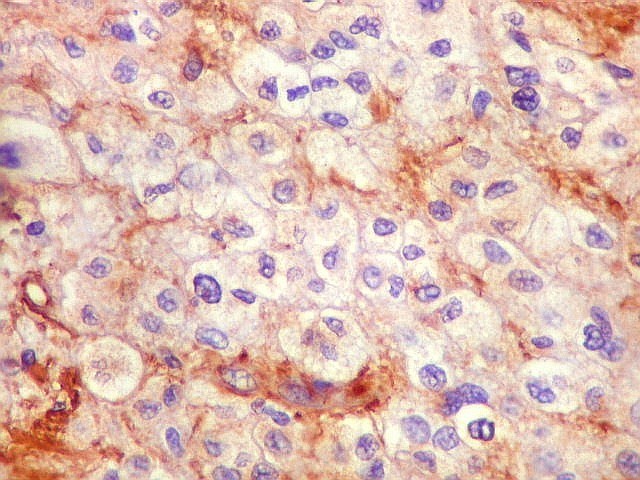
| VIM. Células menores, lembrando oligodendrócitos. Estas pequenas células foram fracamente positivas ou negativas para VIM. | |
 |
 |
 |
 |
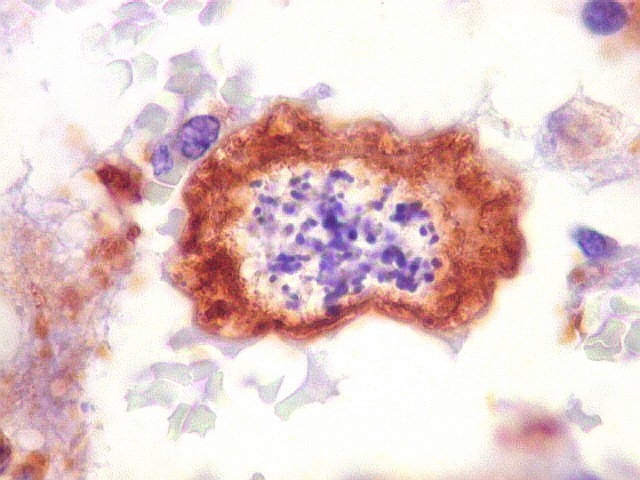
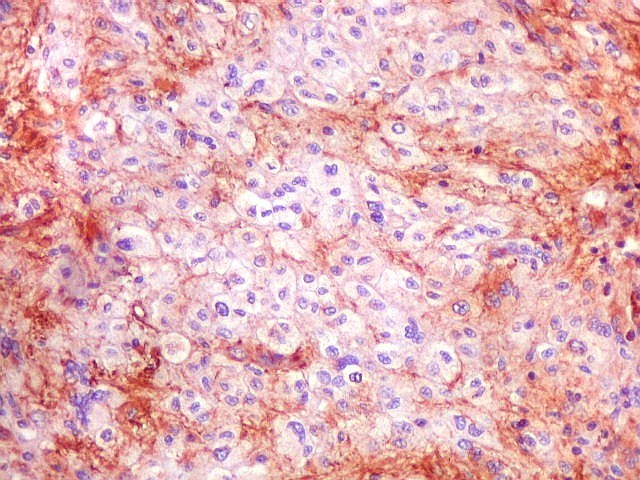
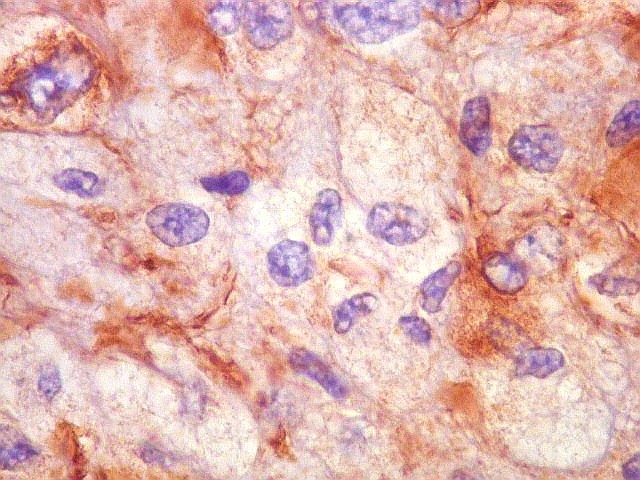
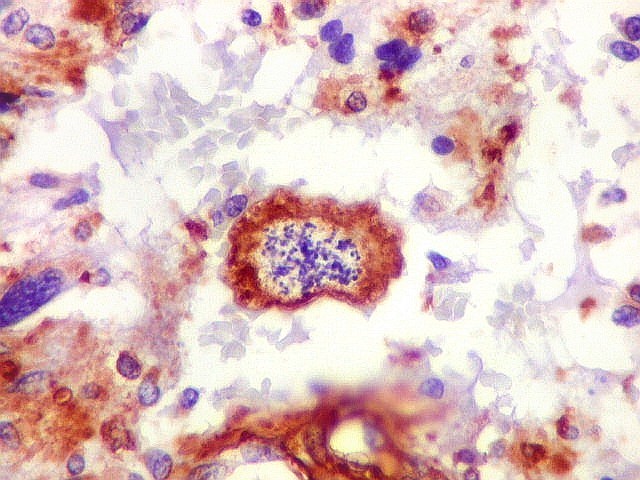
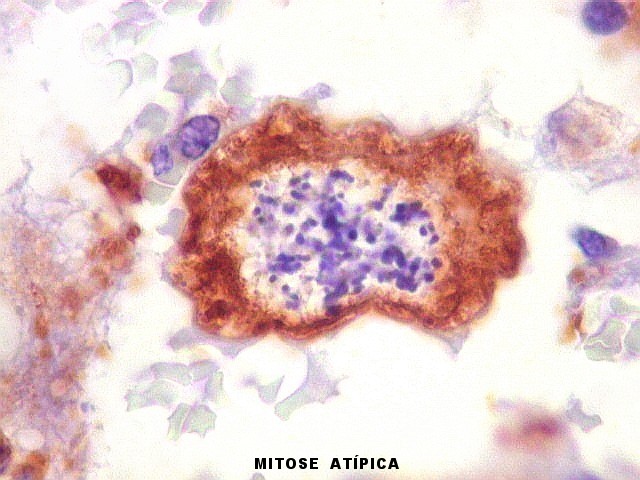
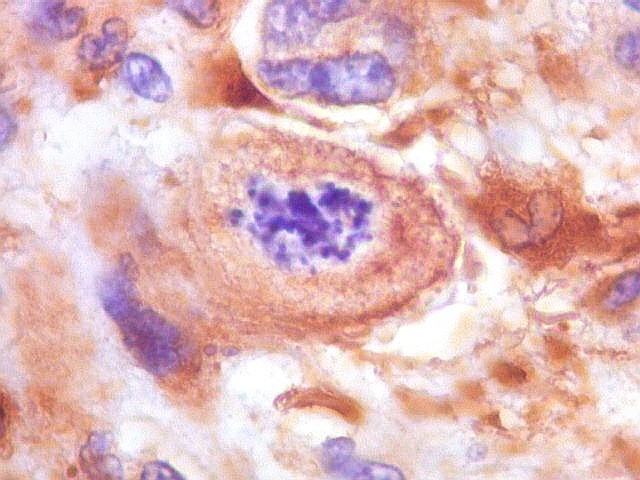
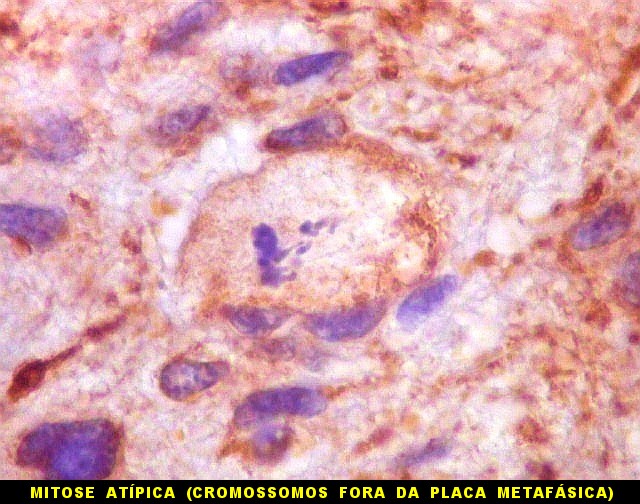
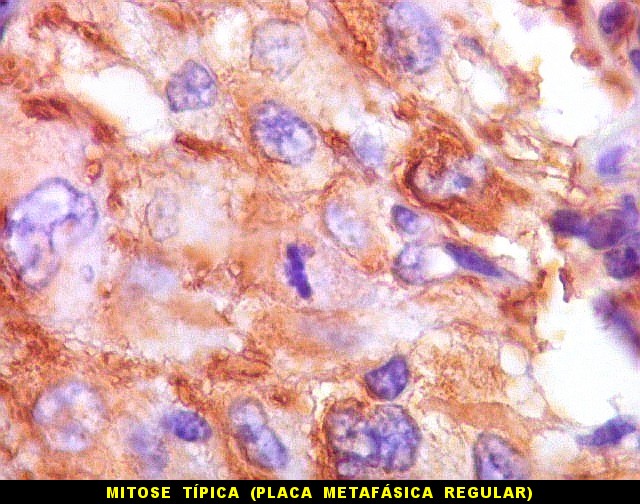
| VIM. Mitoses. As mitoses observadas iam de típicas a atípicas. Nestas, os cromossomos estavam desorganizados na parte central da célula, ou fora da placa metafásica, sugerindo que pudessem ser perdidos durante a mitose. Mitoses típicas mostravam placas metafásicas regulares e retilíneas no equador celular. | |
 |
 |
 |
 |
 |
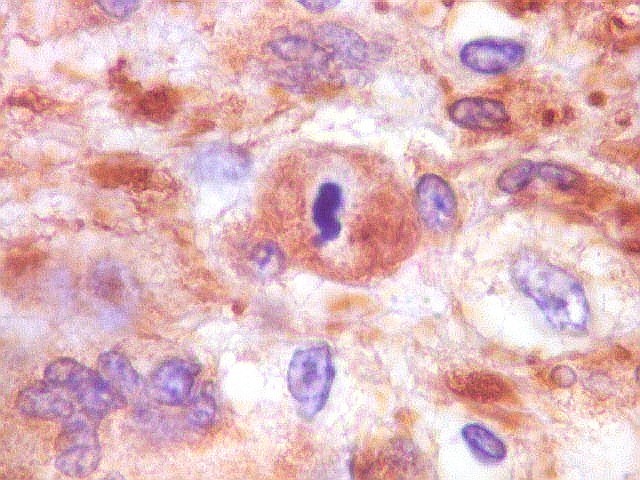 |
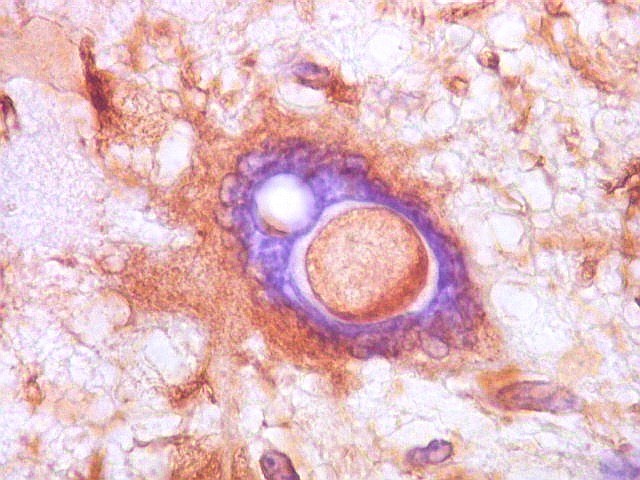
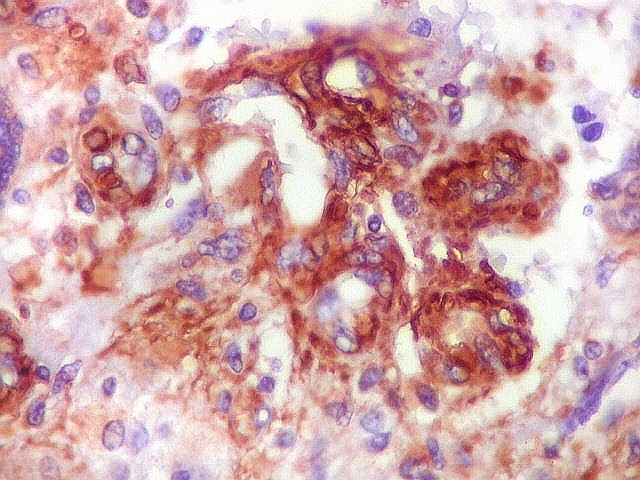
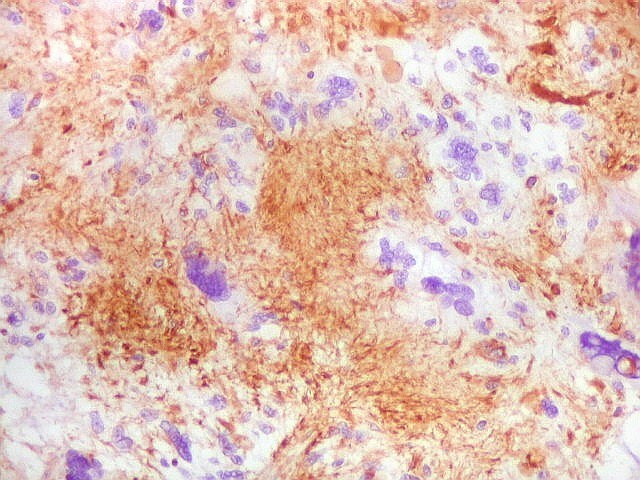
| VIM.
Vasos.
As células participantes de vasos intratumorais, (endotélio e células musculares lisas) são VIM positivas. Ao lado o único exemplo de proliferação vascular que se assemelhava aos pseudoglomérulos do glioblastoma multiforme. Outros pequenos vasos não proliferados se perdiam em meio à positividade geral do tumor. |
 |
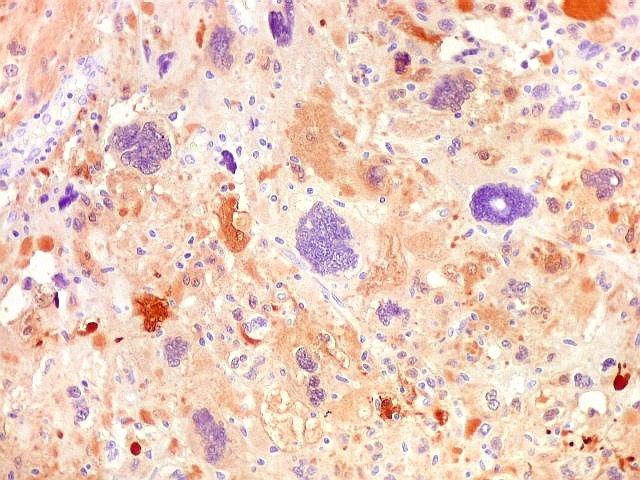
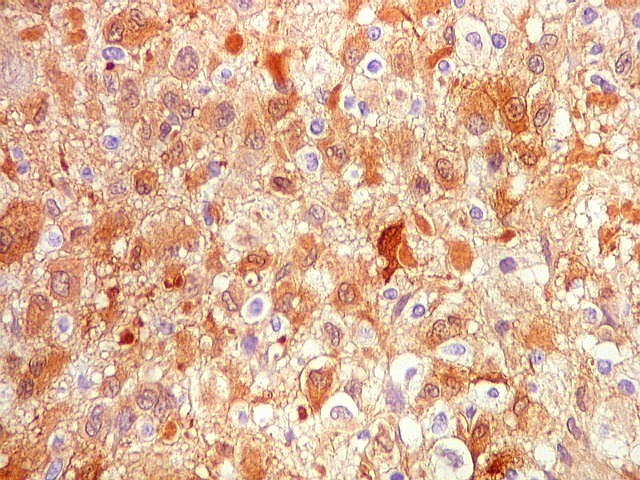
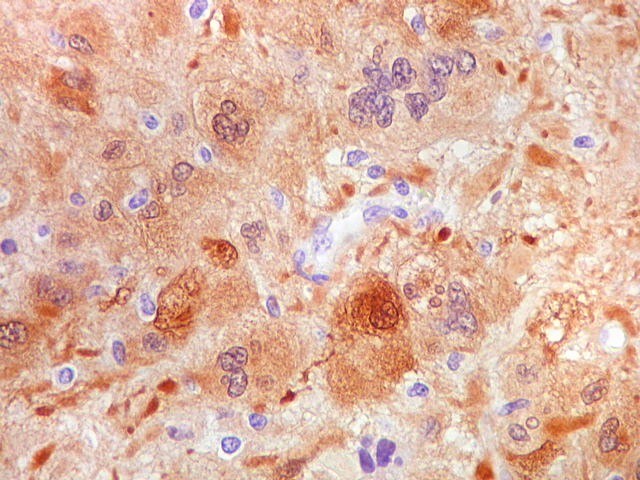
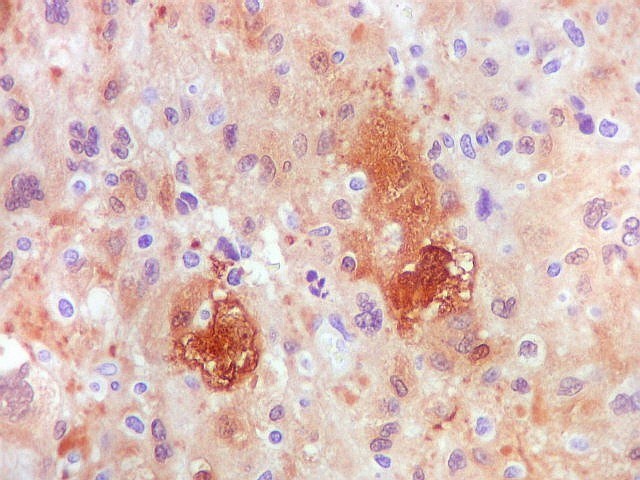
| S-100.
A proteína S-100 (para breve texto, clique) apresentou positividade variável nas células neoplásicas, tanto nuclear como citoplasmática. |
 |
 |
 |
 |
 |
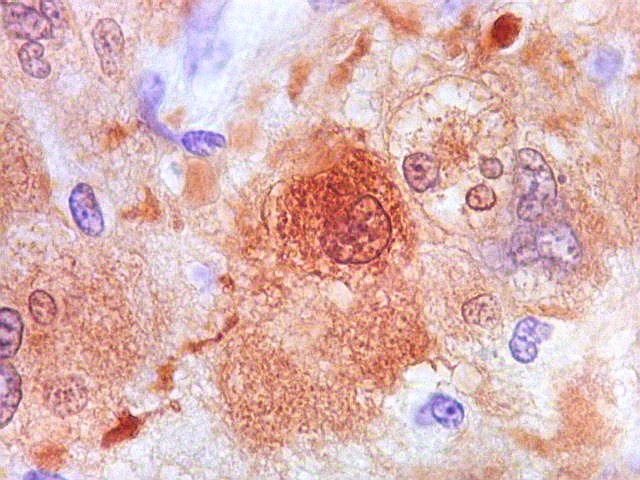
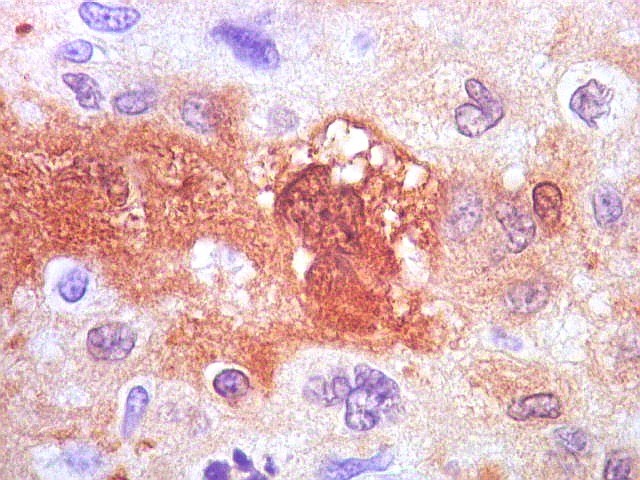
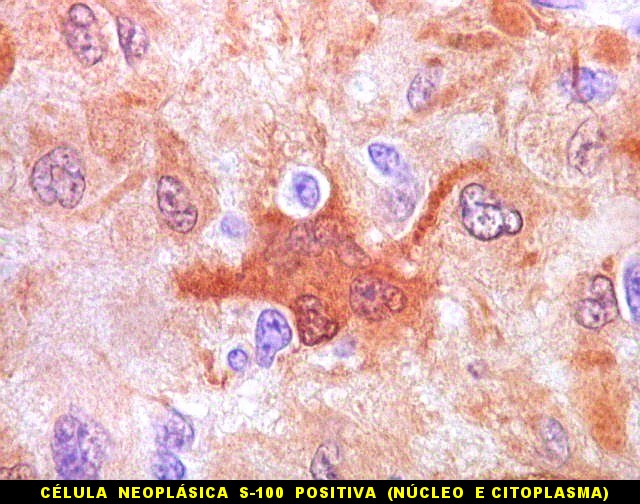
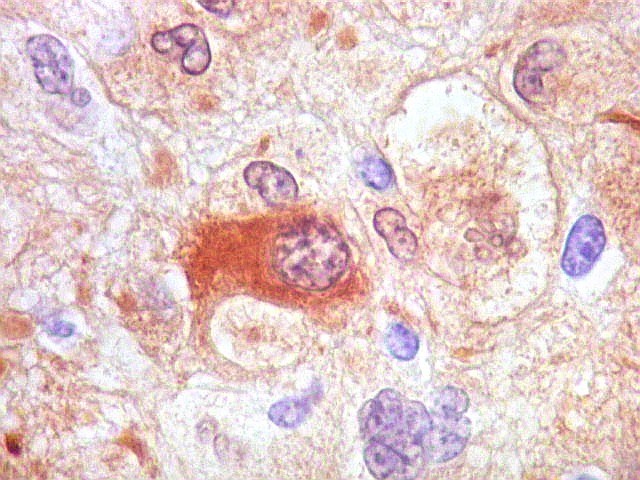
| S-100. Células atípicas positivas. Marcação é citoplasmática e nuclear. Em algumas células notam-se prolongamentos citoplasmáticos. | |
 |
 |
 |
 |
 |
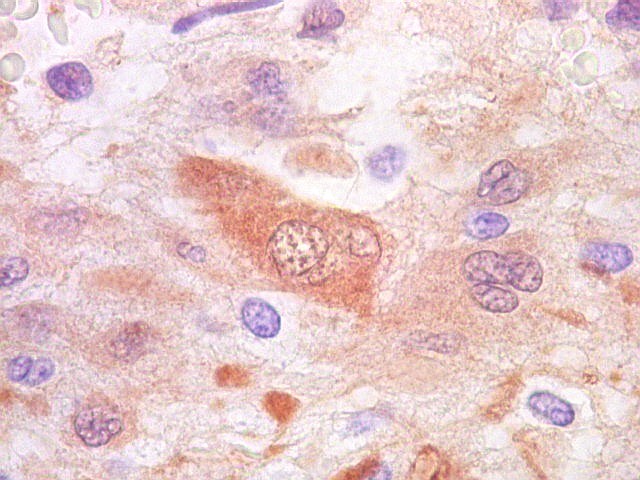 |
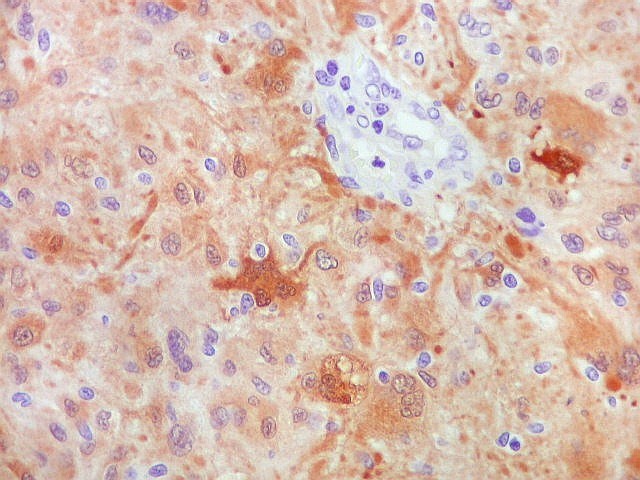
| S-100. Células atípicas negativas. | |
 |
 |
 |
 |
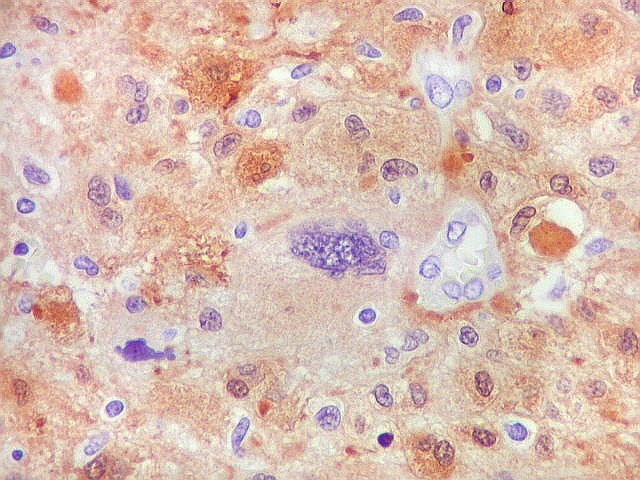
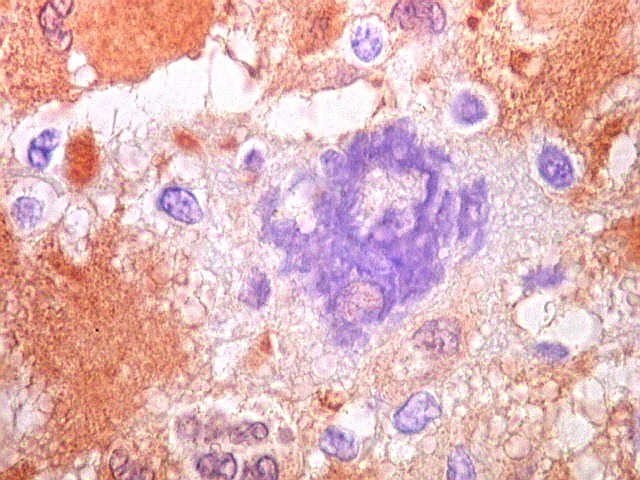
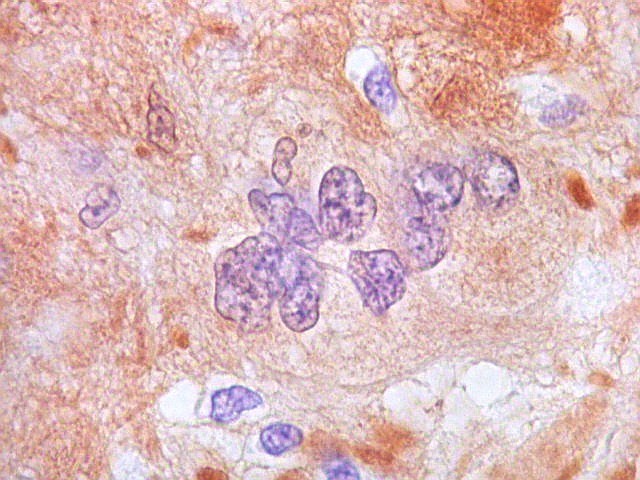
| S-100. Mitose. Única observada na lâmina, altamente atípica. | |
 |
 |
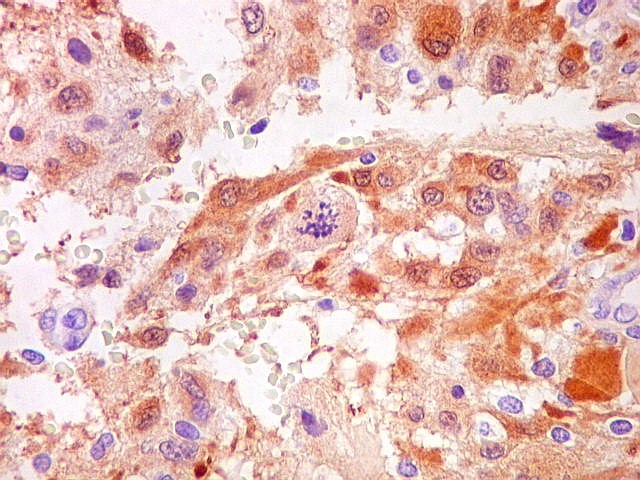
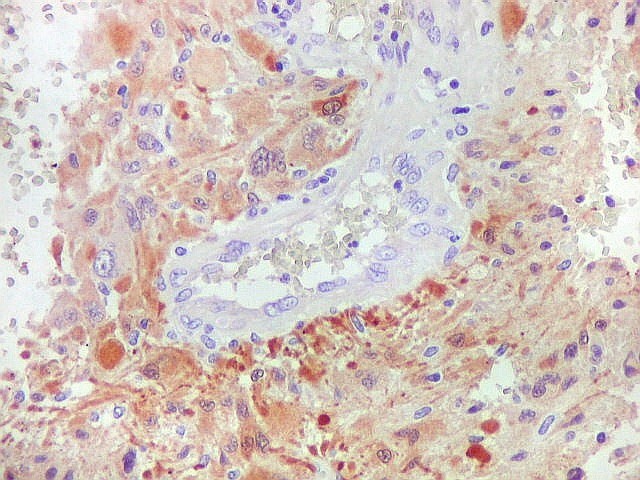
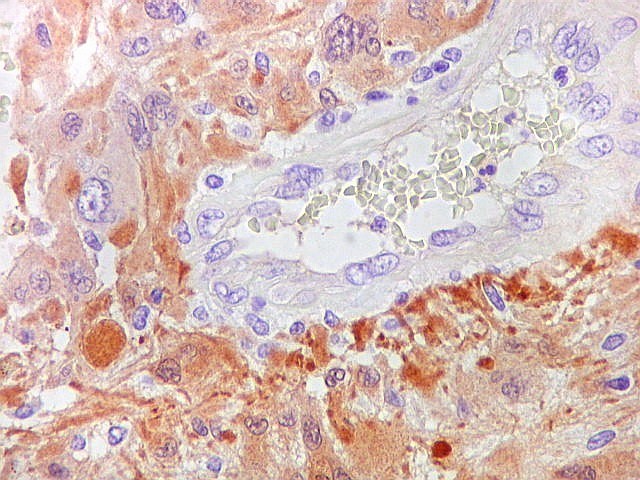
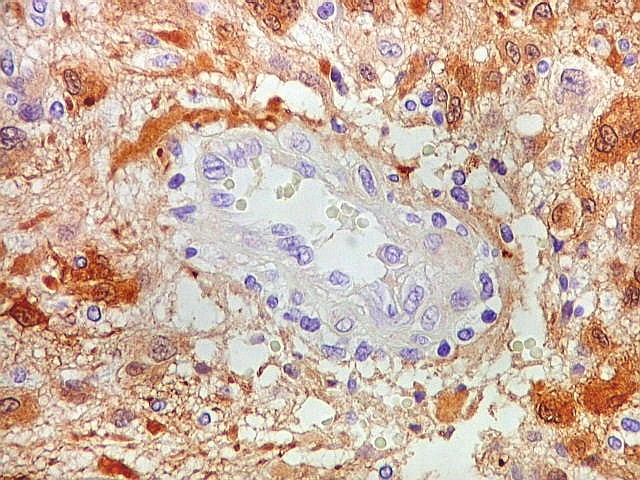
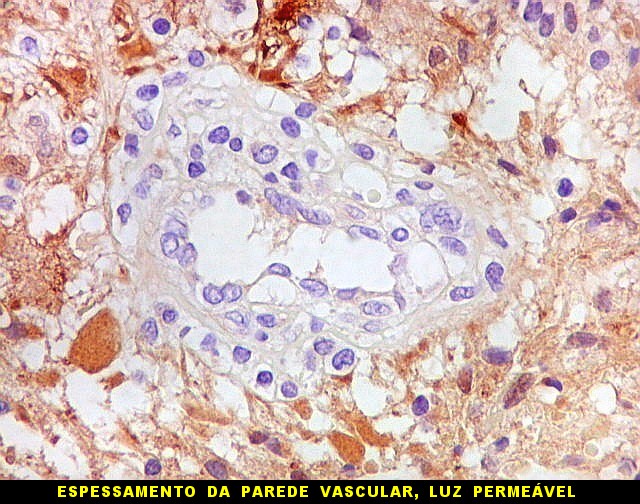
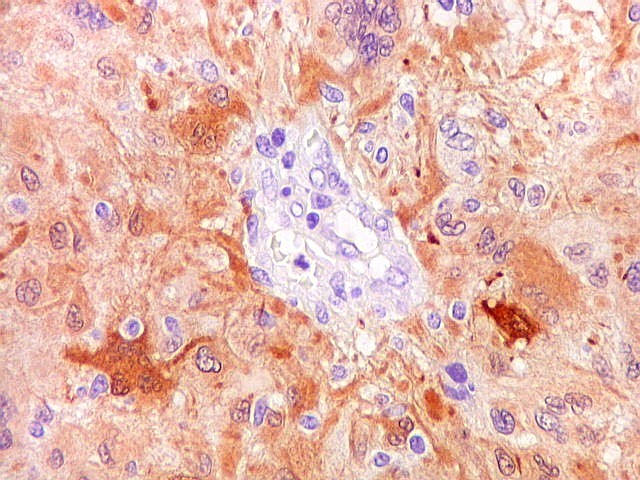
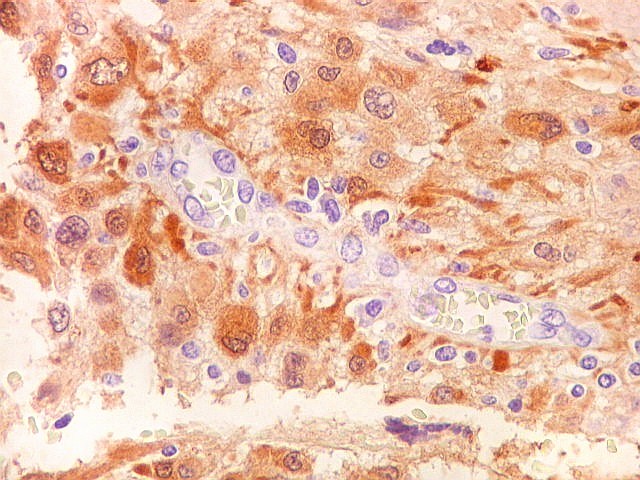
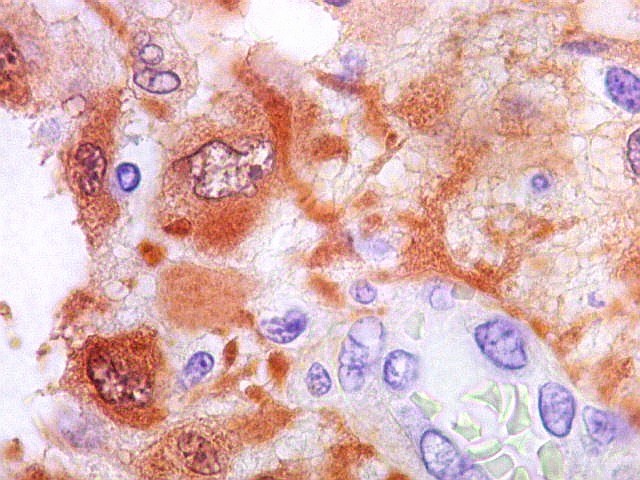
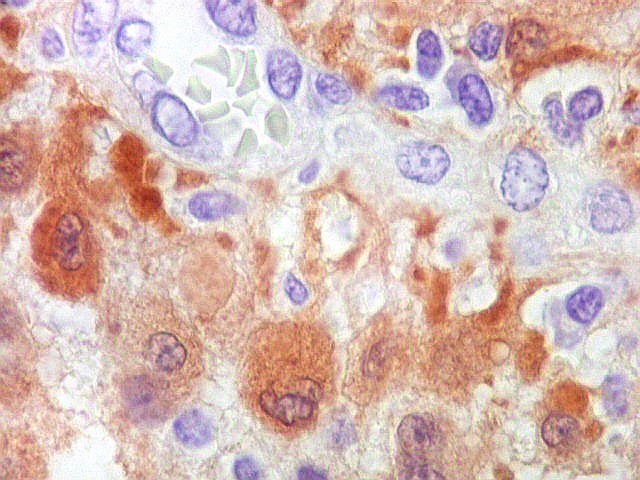
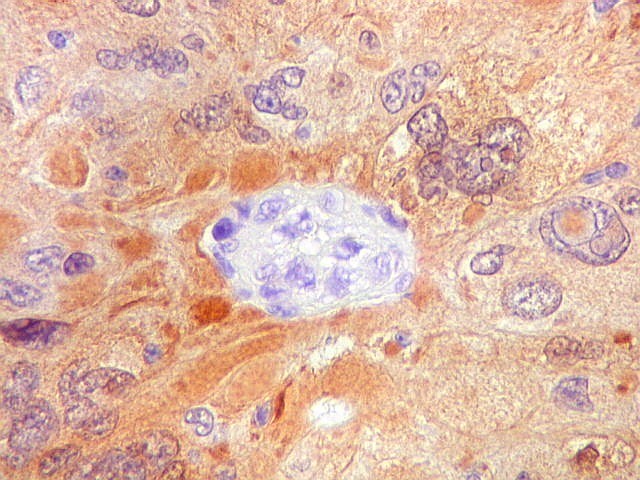
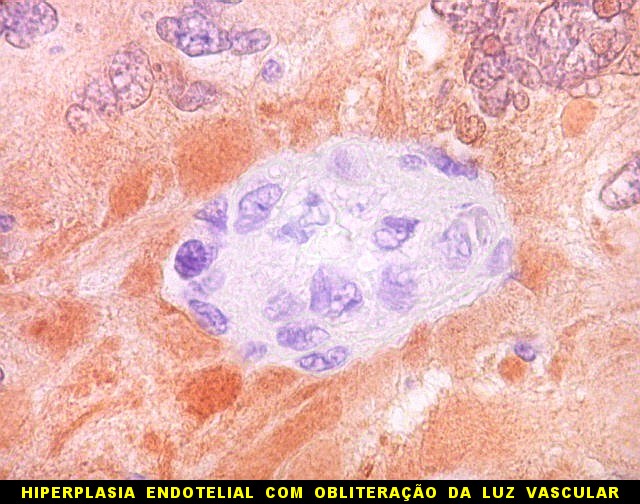
| S-100. Vasos. Como os vasos são sempre negativos para S-100, destacam-se contra os elementos neoplásicos, permitindo análise de sua arquitetura. Observa-se espessamento da parede vascular a custa de hipertrofia e hiperplasia do endotélio. Em alguns vasos, há obliteração total da luz. Mesmo assim, não havia áreas de necrose na amostra. | |
 |
 |
 |
 |
 |
 |
 |
 |
 |
 |
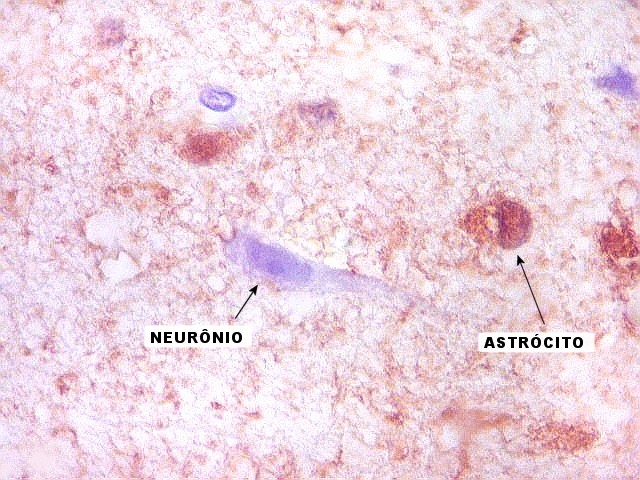
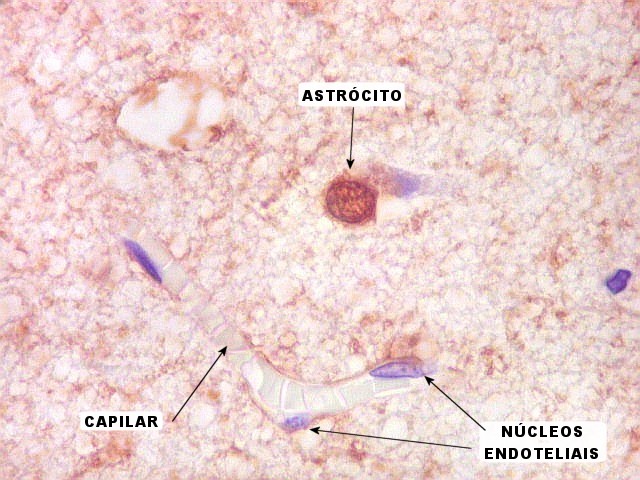
| S-100.
Córtex cerebral normal.
Este pequeno fragmento de córtex cerebral vizinho ao tumor serviu de controle interno da reação. Nele notam-se positividade dos núcleos de células gliais (presumivelmente astrócitos ou oligodendrócitos) e negatividade do núcleo e citoplasma dos neurônios e das células endoteliais dos capilares (resultados esperados em tecido nervoso normal). |
 |
 |
 |
 |
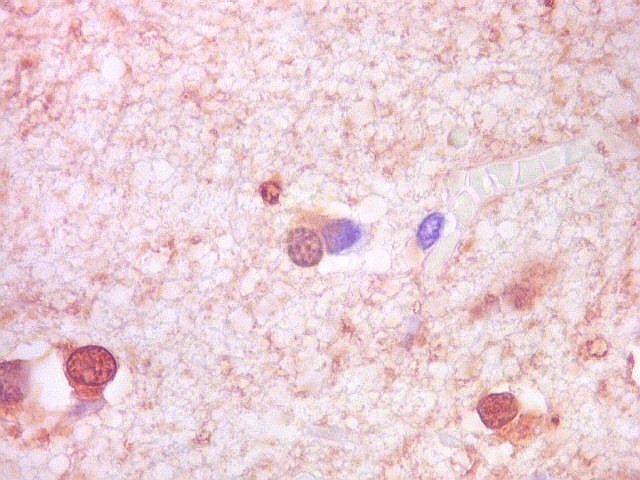 |
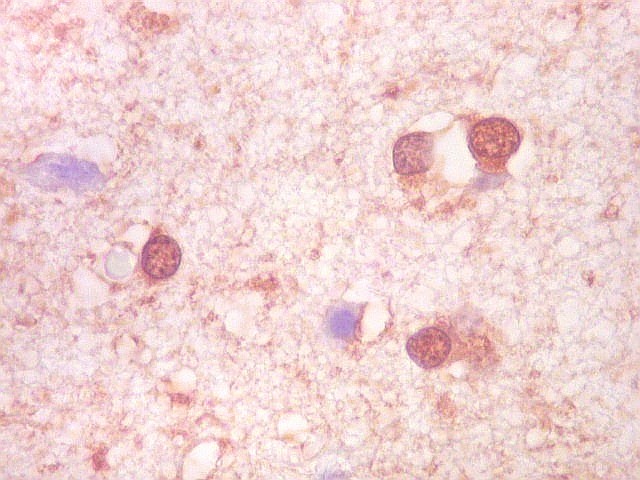
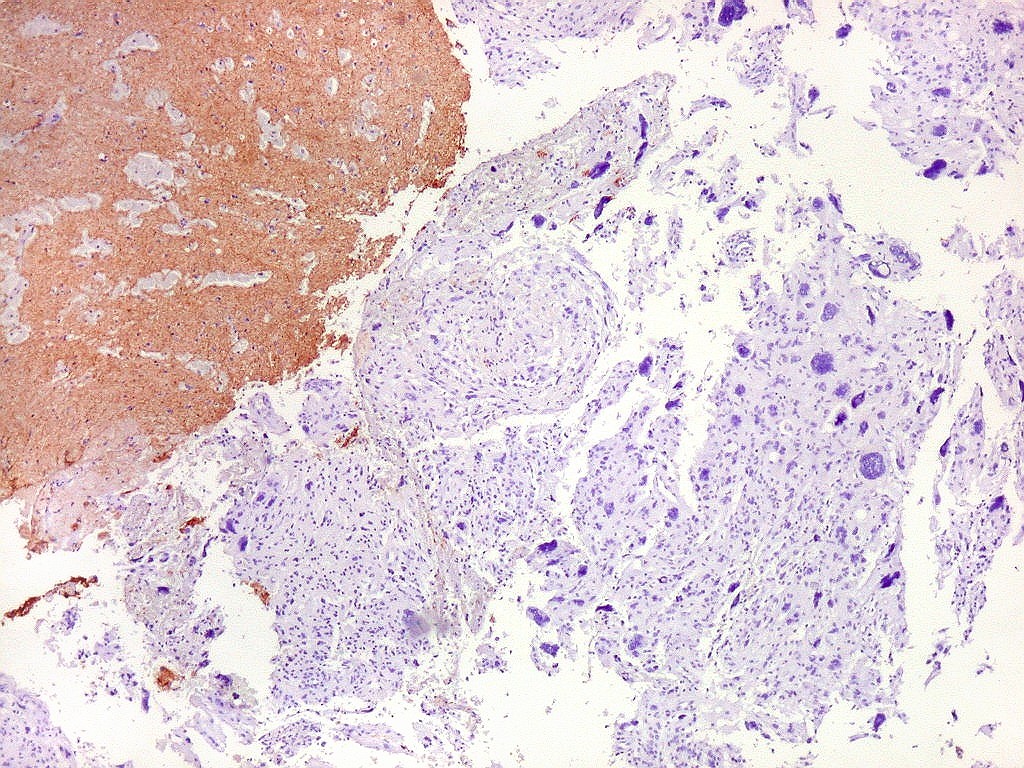
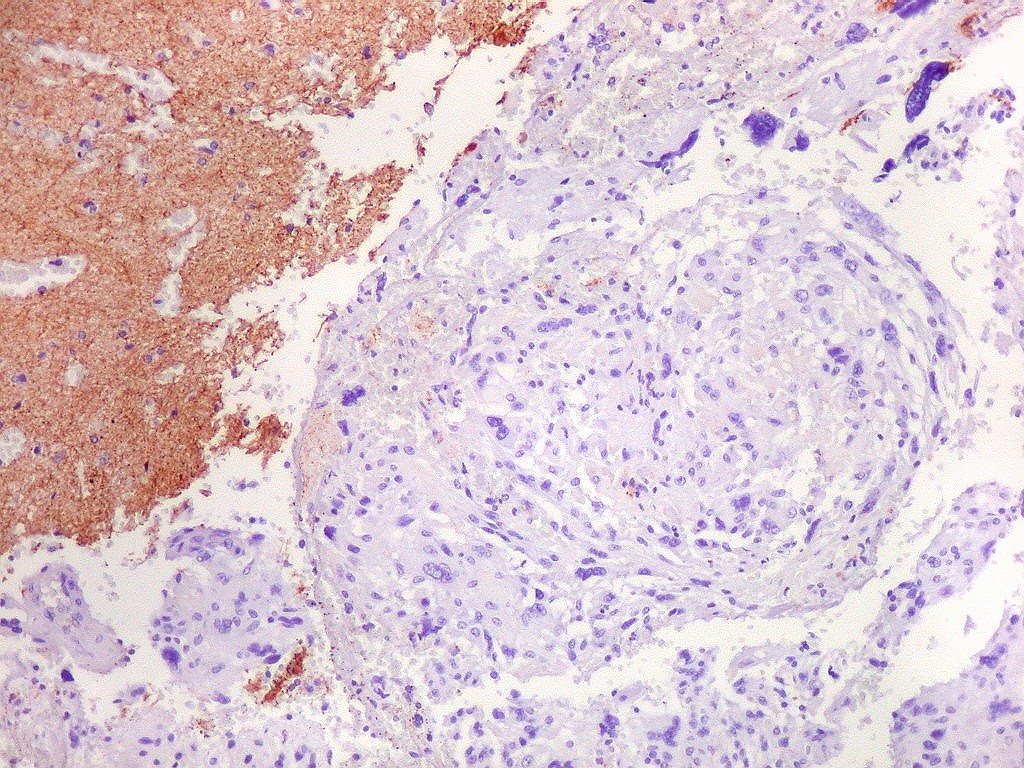
| NF.
A reação para proteína de neurofilamento foi totalmente negativa no tumor, com controle positivo no córtex cerebral limítrofe. Como não há axônios entre as células tumorais, deduz-se que a capacidade infiltrativa do tumor é mínima ou ausente. Isto reforça a natureza expansiva do xantoastrocitoma pleomórfico, e o distingue dos astrocitomas difusos, que são eminentemente infiltrativos. |
 |
 |
 |
 |
| Antígenos negativos. Sinaptofisina (SNF) e cromogranina foram negativos no tumor, com controle interno positivo do córtex cerebral limítrofe. |
| Agradecimentos. Caso do Hospital Centro Médico de Campinas, SP, enviado e gentilmente contribuído pelos Drs. Antonio Augusto Roth Vargas, Marcelo Senna Xavier de Lima, Paulo Roland Kaleff e residentes do Serviço de Neurocirurgia. Preparações histológicas e imunohistoquímicas pelos técnicos Viviane Ubiali, Ana Claudia Sparapani Piaza, Luzia Aparecida Magalhães Ribeiro Reis, Arethusa de Souza, Luis Felipe Billis e Thainá Milena Stela de Oliveira. Depto de Anatomia Patológica da FCM-UNICAMP, Campinas, SP. |
| Para mais imagens deste caso: | RM | HE | IH : GFAP, VIM, S100, NF | IH : CD34, CD99, 1A4, Ki67, p53 |
 |
 |
 |
 |
| Características de imagem dos xantoastrocitomas | Textos sobre xantoastrocitoma pleomórfico (1) (2) | Xantoastrocitomas - mais casos: neuroimagem, neuropatologia |
| Neuropatologia
- Graduação |
Neuropatologia -
Estudos de casos |
Neuroimagem
- Graduação |
Neuroimagem -
Estudos de Casos |
Roteiro
de aulas |
Textos
de apoio |
Correlação
Neuropatologia - Neuroimagem |
| Índice alfabético - Neuro | Adições recentes | Banco de imagens - Neuro | Textos ilustrados | Neuromuscular | Patologia - outros aparelhos | Pages in English |
|
|