|
|
Página de resumo do caso. |
|
|
|
Página de resumo do caso. |
|
| Masc. 54 a. Paciente teve tricoleucemia, tratada em 2000 com sucesso. A partir de 2004, passou a apresentar sinais e sintomas medulares atribuídos a 'meningite crônica', possivelmente por tuberculose (assim foi considerado, na época). Teve evolução arrastada com agravamentos e remissões. Em setembro de 2011 realizou ressonância magnética de crânio, que revelou hidrocefalia supratentorial. Duas pequenas lesões foram detectadas no ventrículo lateral direito (abaixo). Foi indicada derivação ventrículo-peritonial. Por piora do quadro medular, foi aumentada a dose de corticosteróides. Cerca de 15 dias antes do óbito voltou a ser internado com cefaléia e sonolência, tendo evoluido com deterioração neurológica progressiva. Foram realizadas outra RM e uma tomografia de crânio, que mostraram obliteração do III ventrículo por tecido cuja natureza foi interpretada como possivelmente inflamatória. Na necrópsia, os achados relevantes limitaram-se ao cérebro, não tendo sido encontradas lesões dignas de nota em outros órgãos, inclusive nos pulmões. A medula espinal não foi examinada. |
| Clique para : estudos de imagem (RM 2011; RM e TC 2012), macroscopia do cérebro, HE (lesões no III ventrículo, lesão fibrótica / gliótica na comissura anterior, lesões nos ventrículos laterais, lesões no IV ventrículo e meninges da base), destaques da microscopia em HE; das colorações especiais, da imunohistoquímica e da microscopia eletrônica. Texto sobre histoplasmose. |
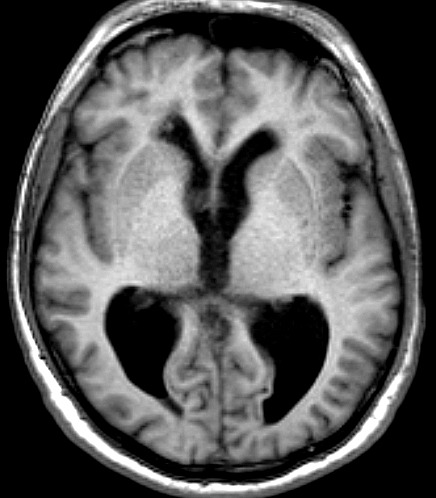
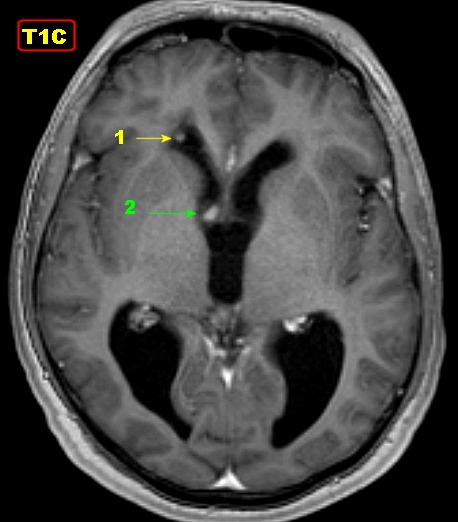
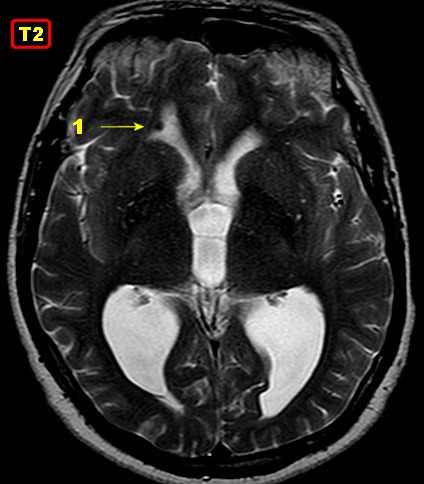
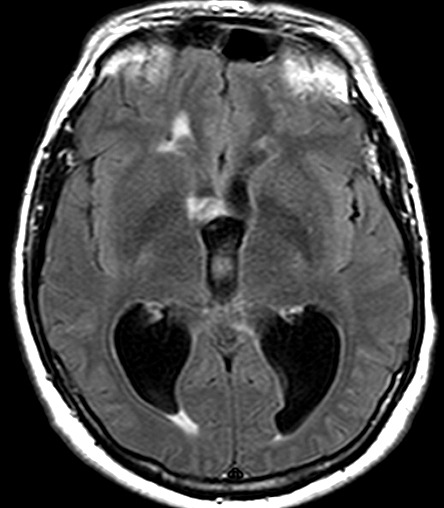
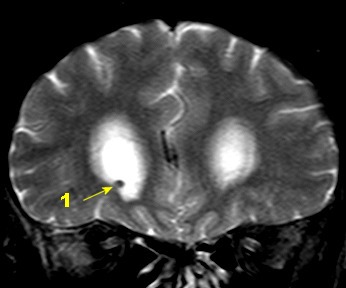
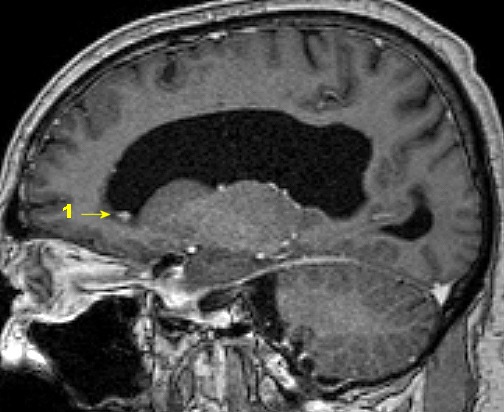
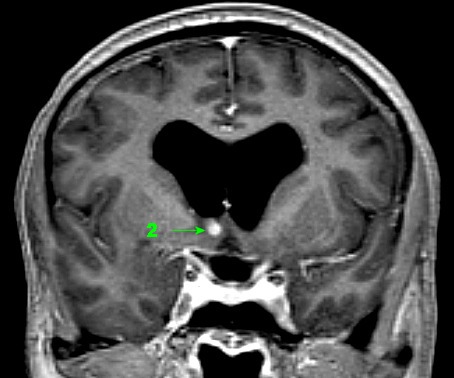
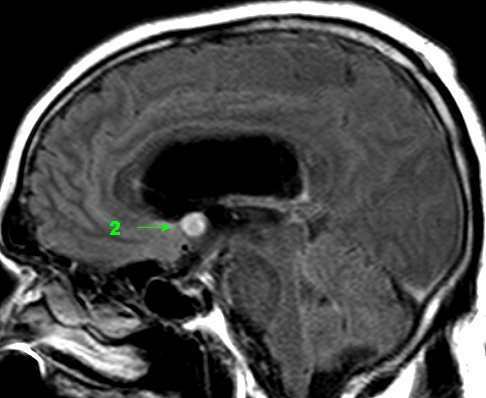
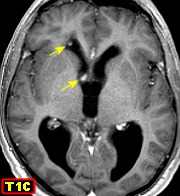
| RM 26/9/2011. Mostra hidrocefalia supratentorial e duas pequenas lesões bem delimitadas: uma menor no corno anterior do ventrículo lateral direito (#1) e outra um pouco maior na região do foramen de Monro (#2), também à direita. Estas foram identificadas na necrópsia como pequenos histoplasmomas (#1, #2), possivelmente focos iniciais de chegada do fungo ao cérebro. | |||
| T1 sem contraste | T1 com contraste | T2 | FLAIR |
 |
 |
 |
 |
| T2 | T1 com contraste | FLAIR | |
 |
 |
 |
 |
| Mais imagens deste exame. | |||
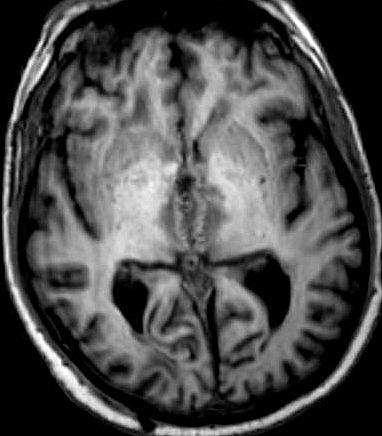
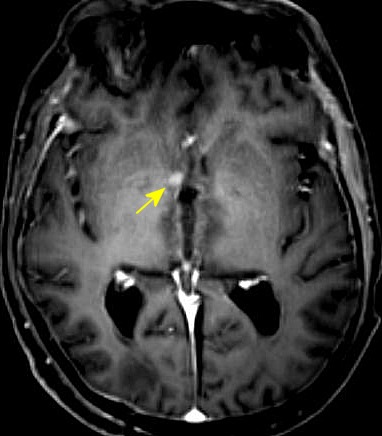
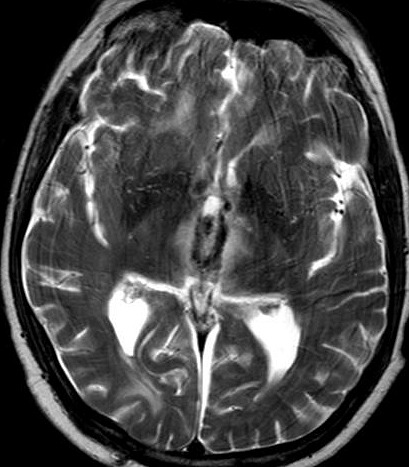
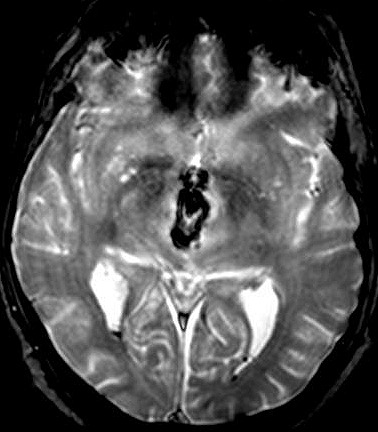
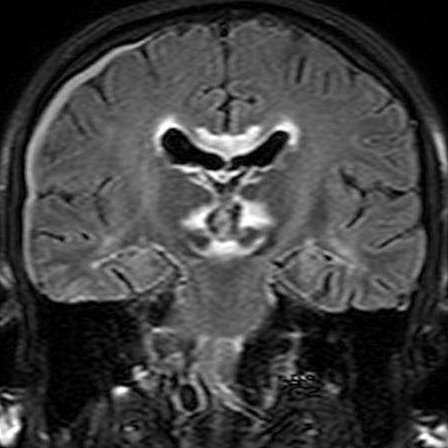
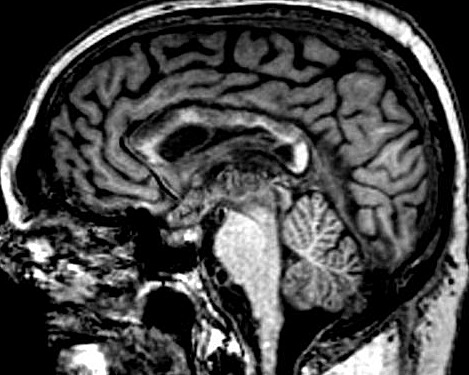
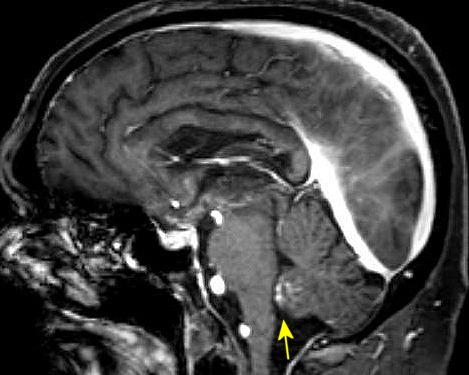
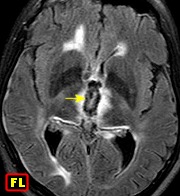
| RM 29/3/2012. Após 6 meses. Obliteração do III ventrículo, notada pela ausência de líquor. O tecido que o preenche não se impregna por contraste. Hipossinal na periferia do III ventrículo em T2, FLAIR e gradiente pode corresponder a hemossiderina de hemorragias crônicas. A pequena lesão na região do foramen de Monro (#2 no exame anterior) persiste (seta no T1 com contraste). Hidrocefalia regrediu após derivação. No coronal FLAIR, permeação liquórica transependimária nos ventrículos laterais e hipersinal no corpo caloso são resquícios da hipertensão liquórica. Edema nos tálamos junto ao III ventrículo obstruído pode ser atribuído à inflamação. Impregnação do córtex cerebelar no vermis inferior (no sagital com contraste) corresponde a infiltração do cerebelo pelos parasitas. | |||
| T1 sem contraste | T1 com contraste | T2 | Gradiente |
 |
 |
 |
 |
| FLAIR | T1 sem contraste | T1 com contraste |
 |
 |
 |
| Mais imagens deste exame. | ||
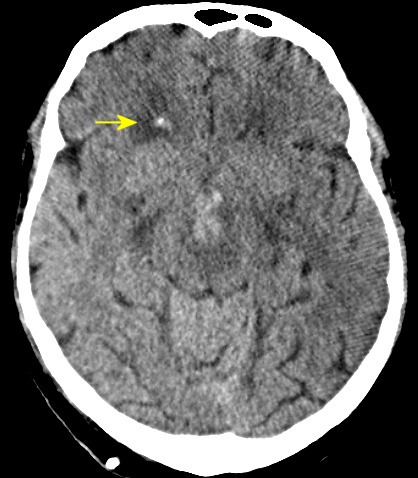
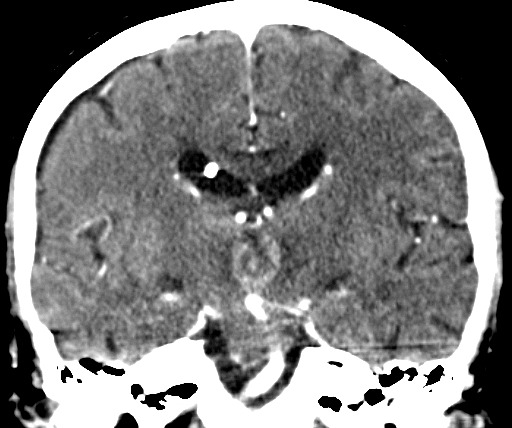
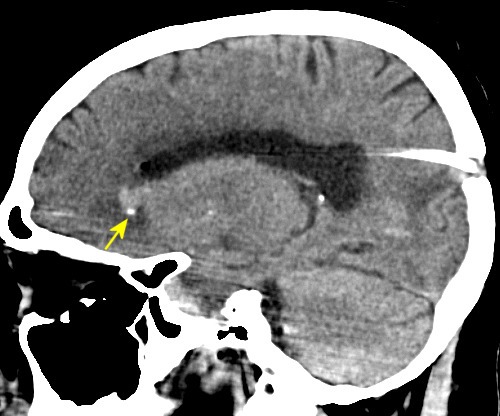
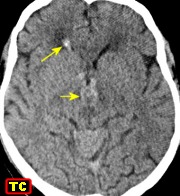
| TC 30/3/2012. Confirma a RM do dia anterior (acima). A diminuta lesão #1 na RM de 26/9/11 é aqui identificada como um ponto calcificado no corno anterior do ventrículo lateral direito (setas). Veja macroscopia e histologia da lesão. | ||
| Sem contraste | Com contraste | Sem contraste |
 |
 |
 |
| Mais imagens deste exame. | ||
|
|
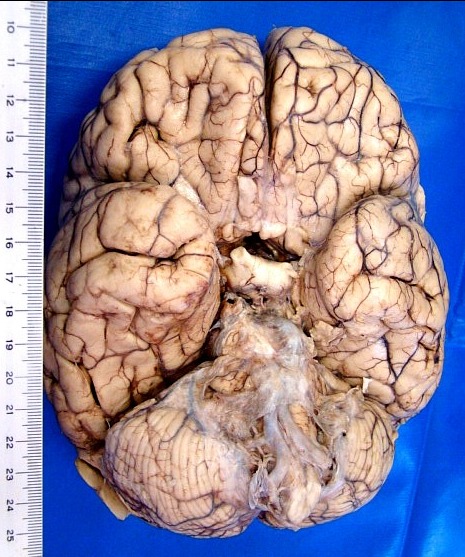
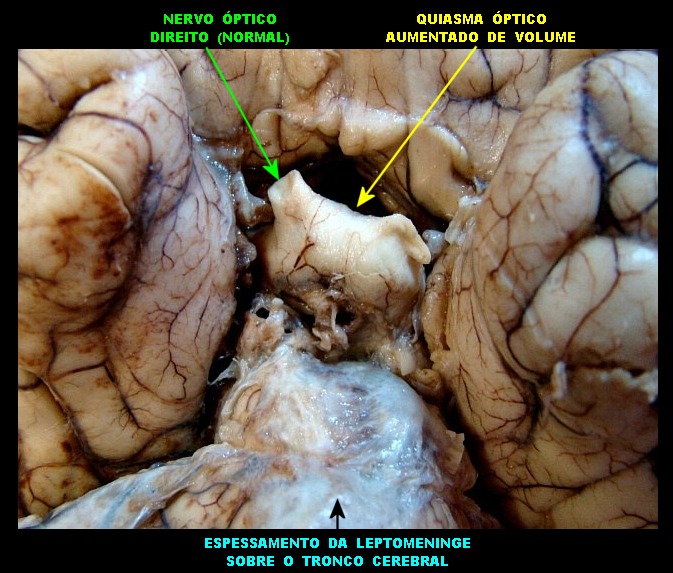
| Face ventral do encéfalo. Espessamento das leptomeninges da face anterior do tronco cerebral. Aumento de volume do quiasma óptico. Mais imagens. | |
 |
 |
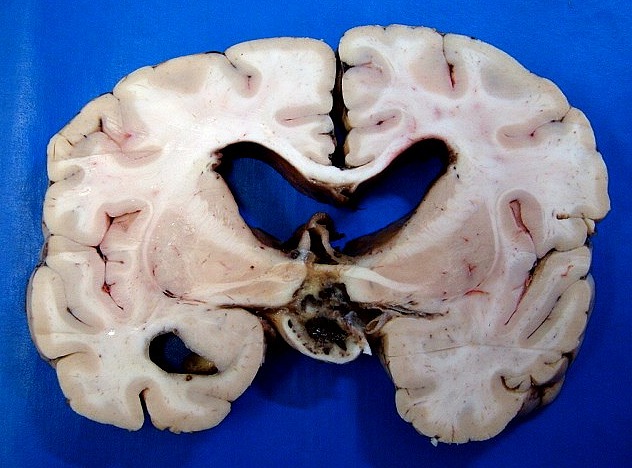
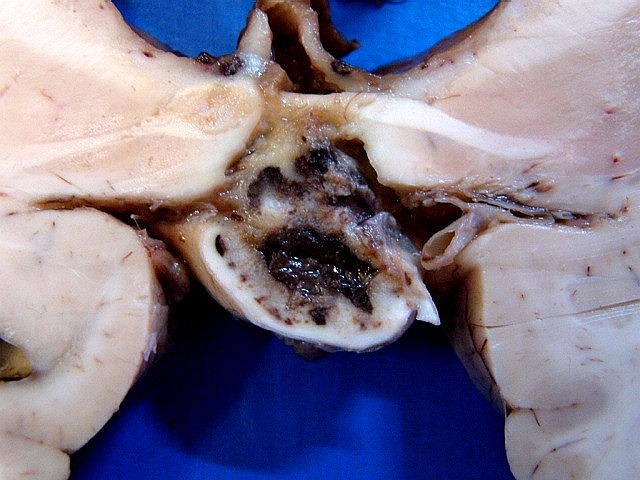
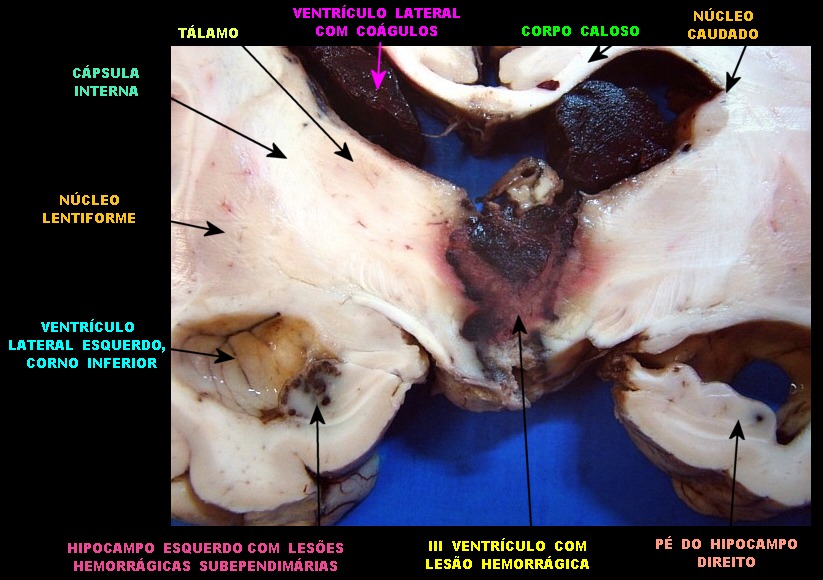
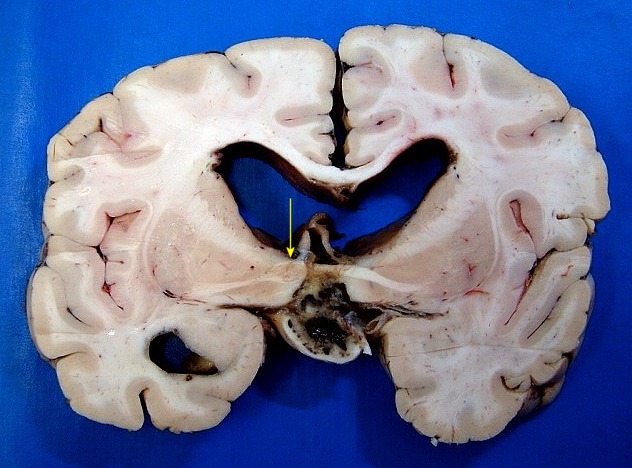
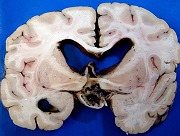
| Cortes coronais. Ventrículos laterais dilatados com coágulos saguíneos. III ventrículo preenchido por sangue e tecido acinzentado que, na microscopia, revelou exsudato de neutrófilos e macrófagos contendo histoplasmas. Pequeno nódulo paramediano direito na comissura anterior / forâmen de Monro corresponde à lesão #2 encontrada nos exames de ressonância magnética. Para detalhes da histologia da mesma, clique. | |
 |
 |
 |
|
 |
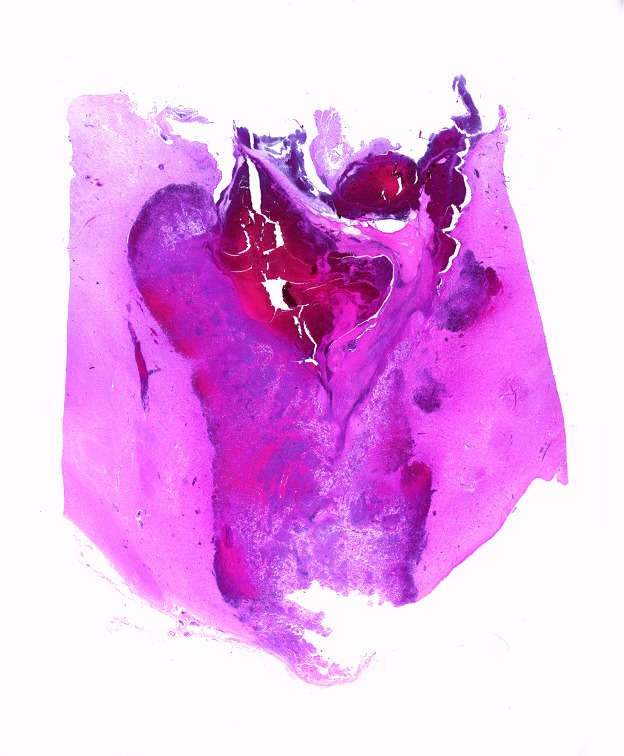 |
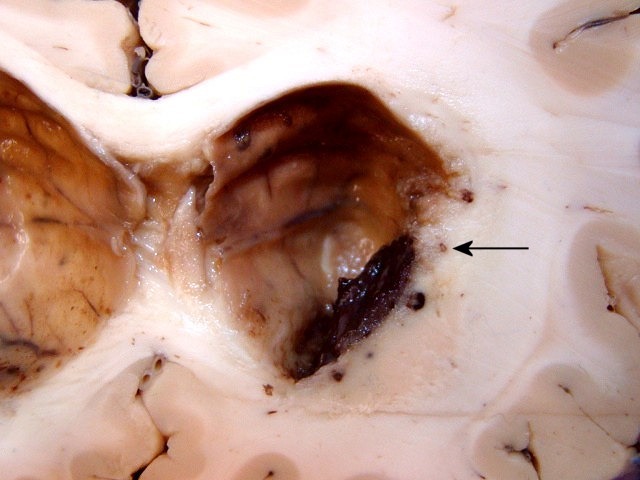
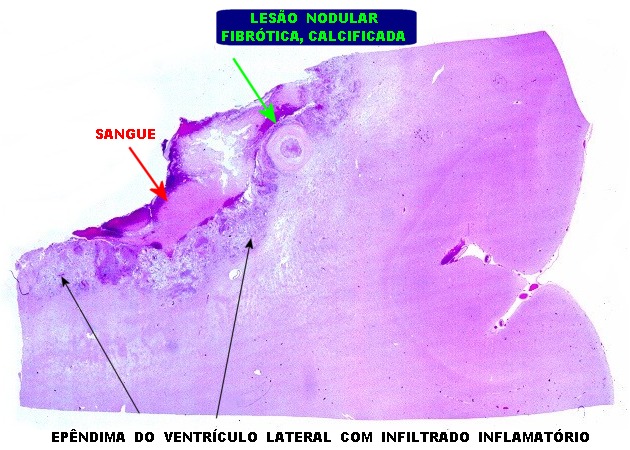
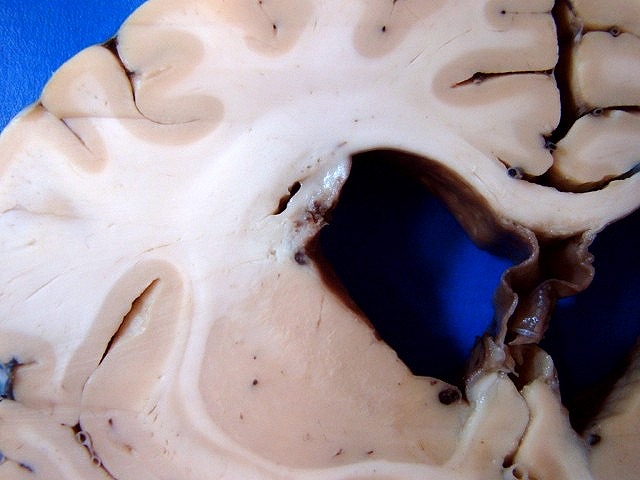
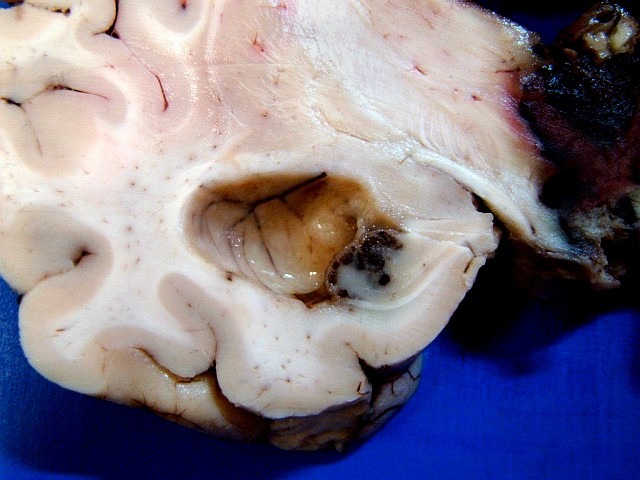
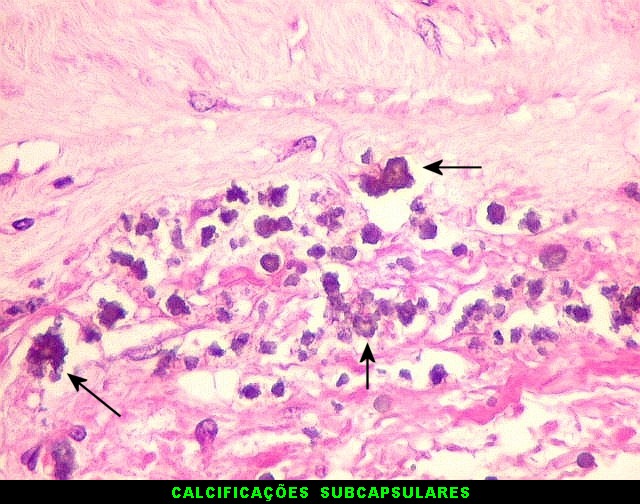
| Lesões no epêndima. O epêndima dos ventrículos laterais apresentava espessamento e petéquias, principalmente no hipocampo esquerdo. Histologicamente, havia ependimite, infiltrado macrofágico rico em histoplasmas e vasculite. No corno anterior direito foi encontrada pequena lesão nodular fibrótica e calcificada (#1 na RM de 2011 e na TC acima). | |
 |
 |
 |
 |
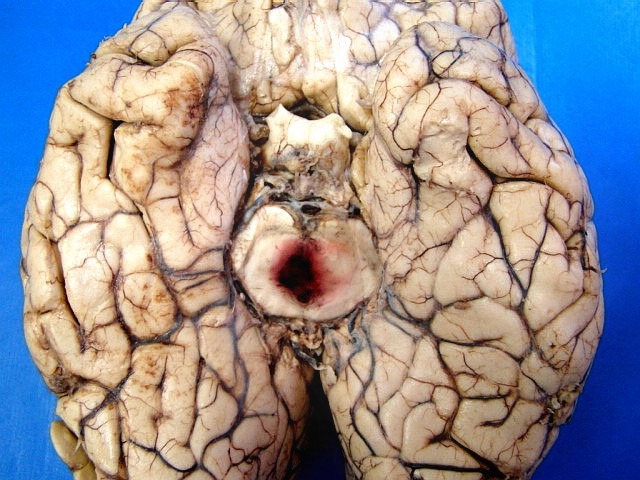
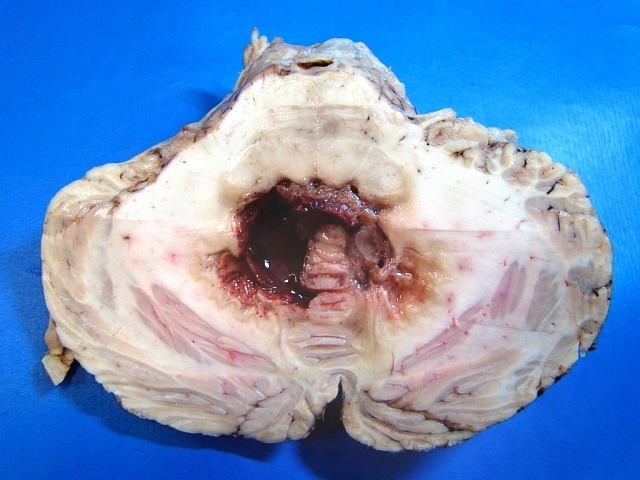
| Lesões no tronco cerebral. Hemorragia na linha média do mesencéfalo, em continuidade com a do III ventrículo. Sangue também no IV ventrículo. Espessamento da leptomeninge da base da ponte. | |
 |
 |
|
|
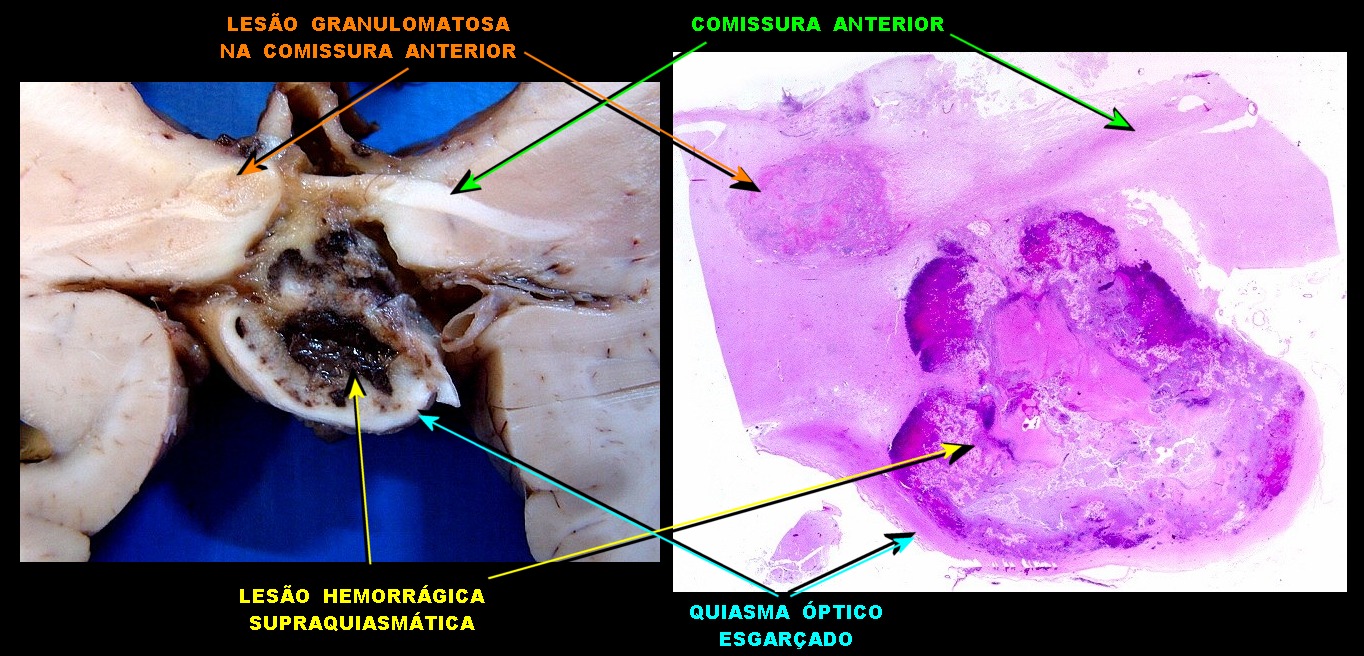
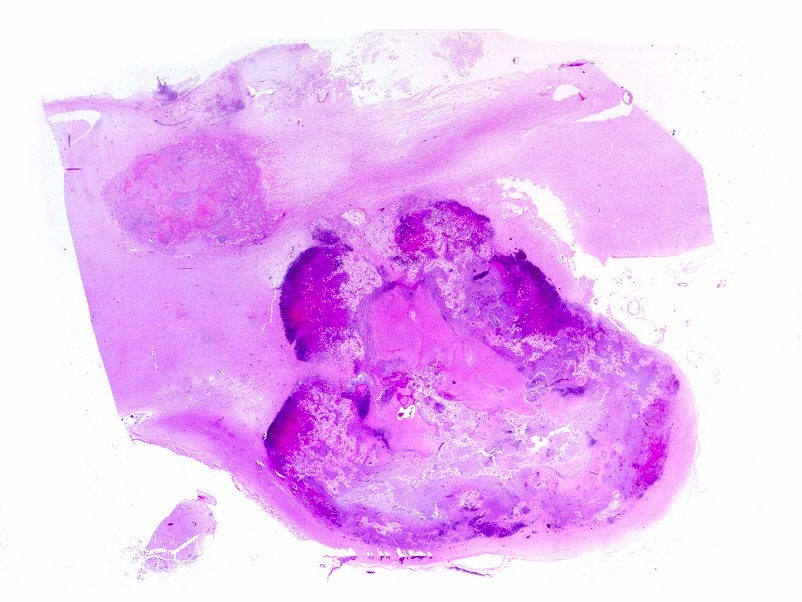
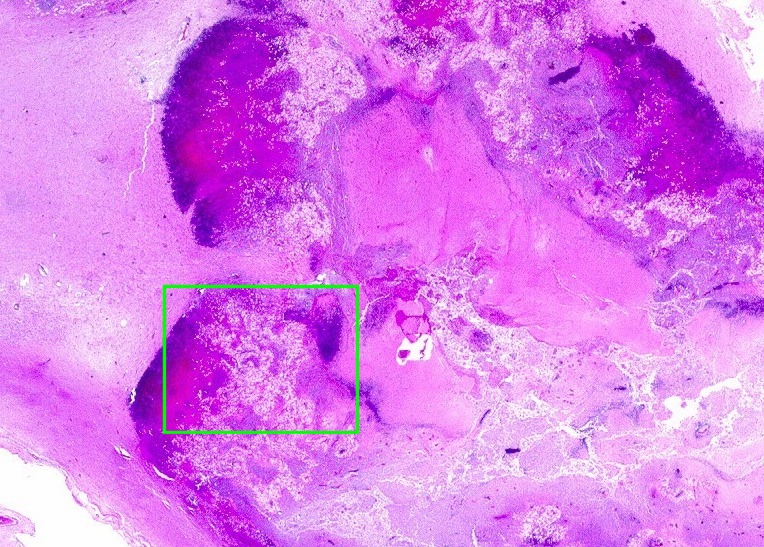
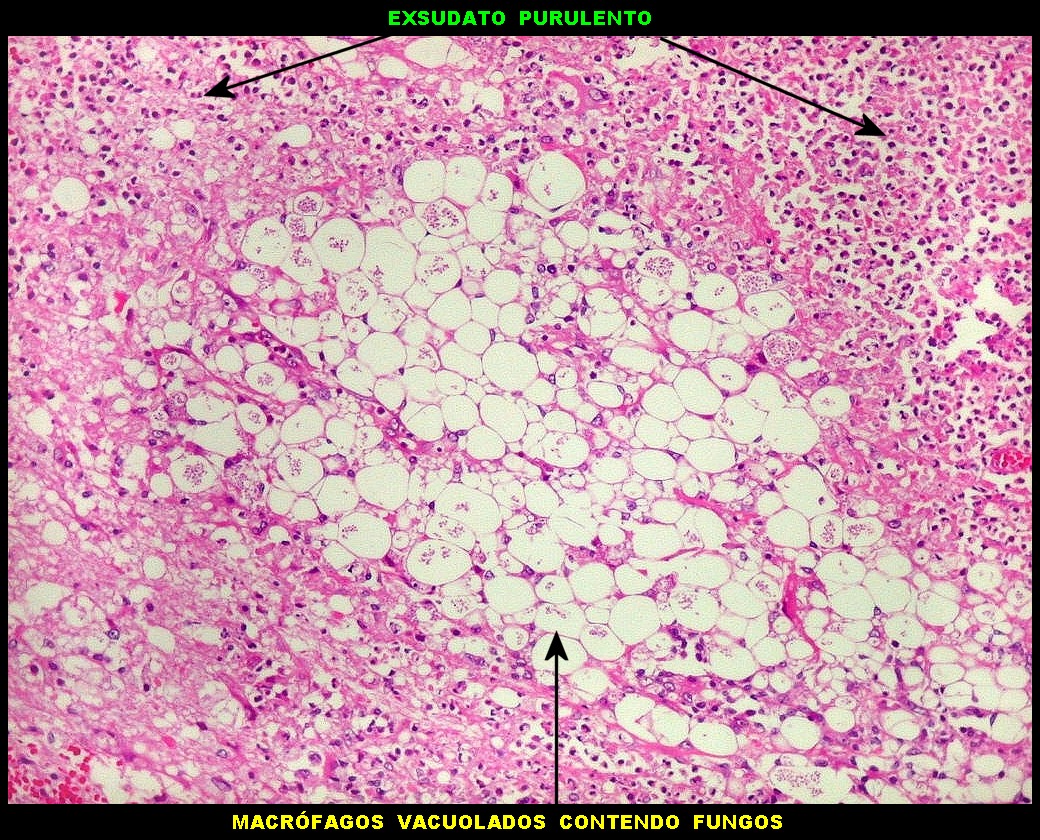
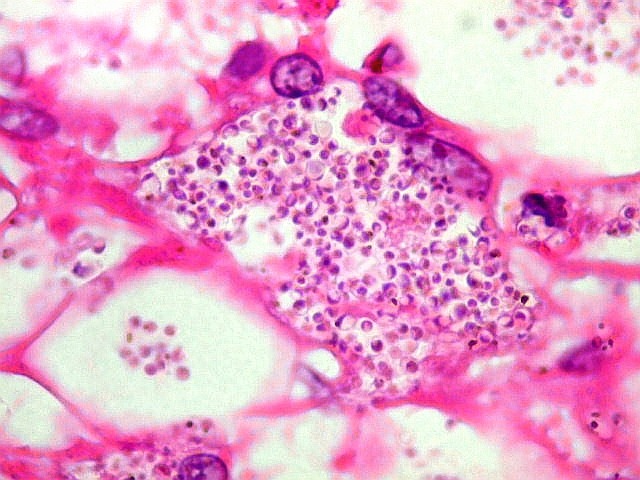
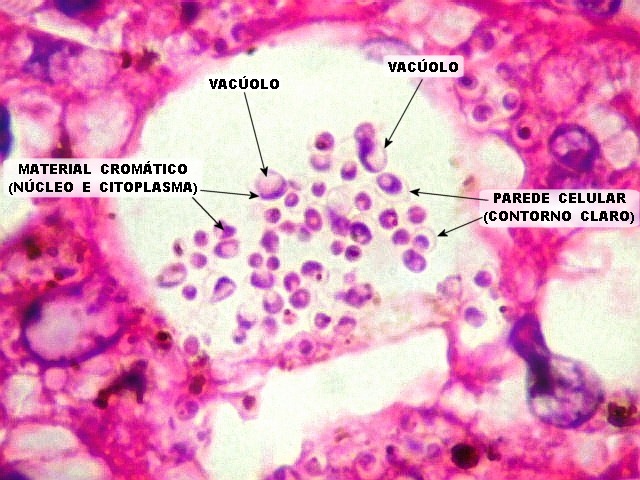
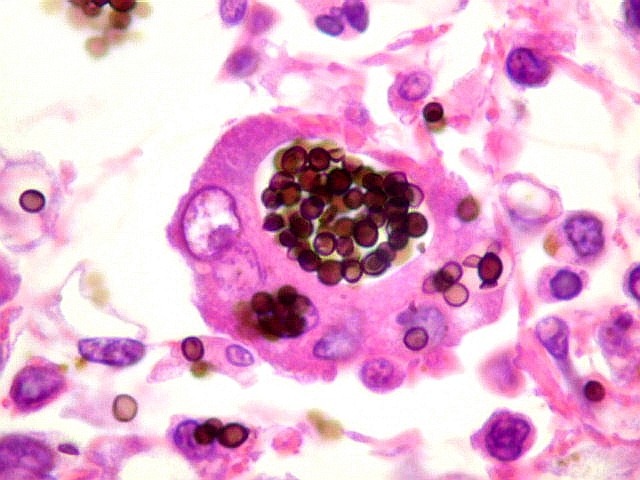
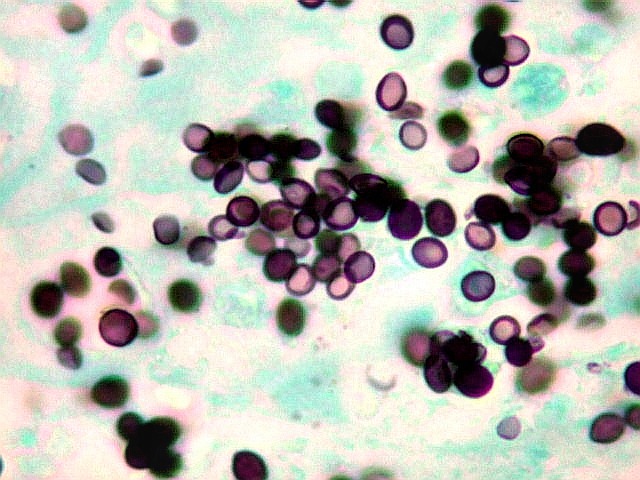
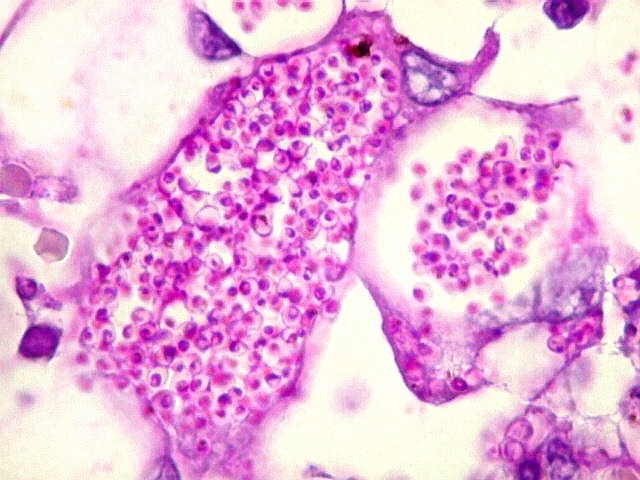
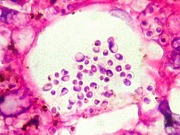
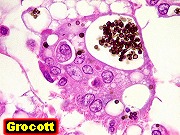
| Lesão do III ventrículo. Lâmina escaneada da região anterior do III ventrículo ao nível do quiasma óptico. O centro da lesão é preenchido por sangue. Na periferia, alternância de áreas claras e basófilas. As claras mostram macrófagos com fagossomos dilatados, contendo miríades de pequenos fungos com morfologia compatível com Histoplasma capsulatum. Estes são demonstrados na impregnação pela metenamina-prata de Grocott, contracorada por HE, por verde-luz e com PAS + hematoxilina. | |
 |
 |
 |
 |
 |
 |
 |
 |
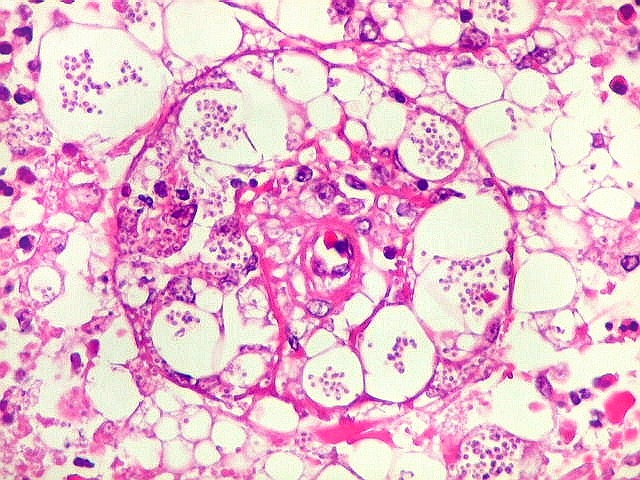
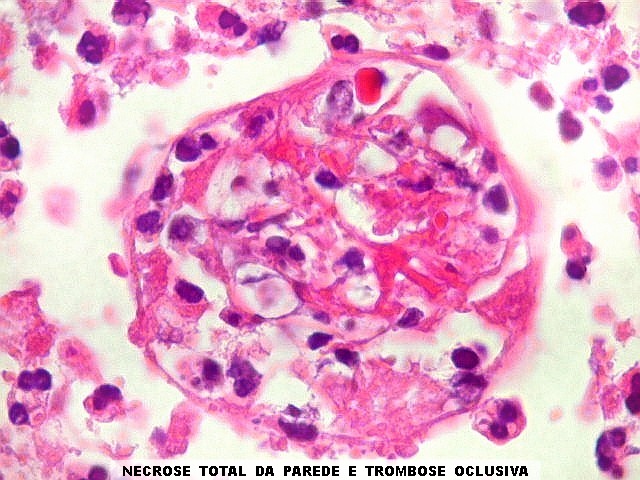
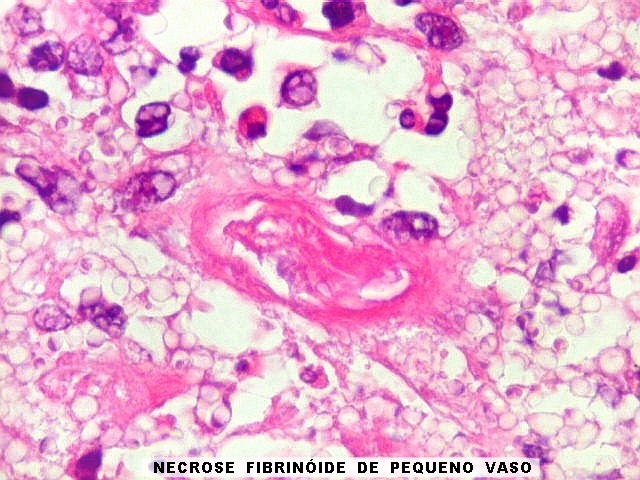
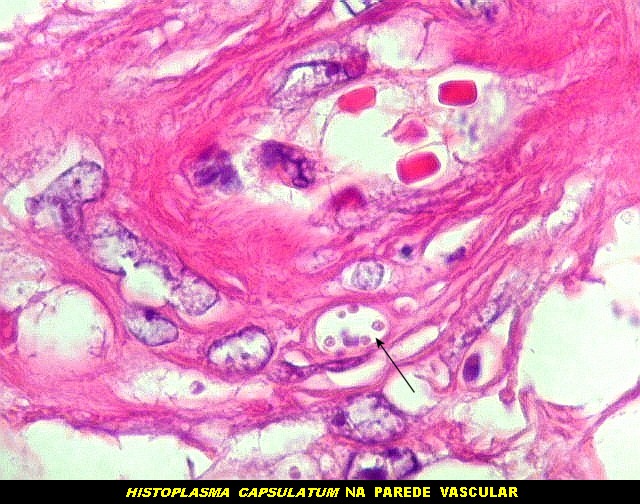
| Vasculite. A causa da hemorragia intraventricular (não observada nos exames de imagem de uma semana antes do óbito) foi atribuída a lesão inflamatória de pequenos vasos, também observada nas petéquias do epêndima. | |
 |
 |
 |
 |
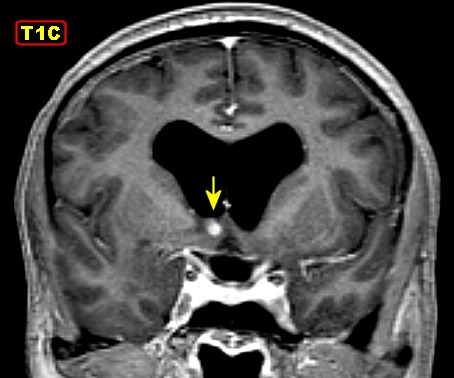
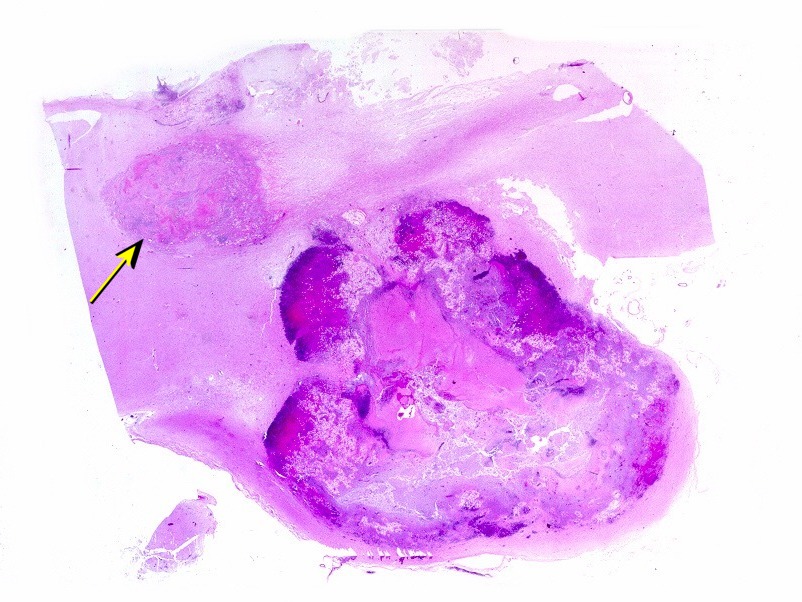
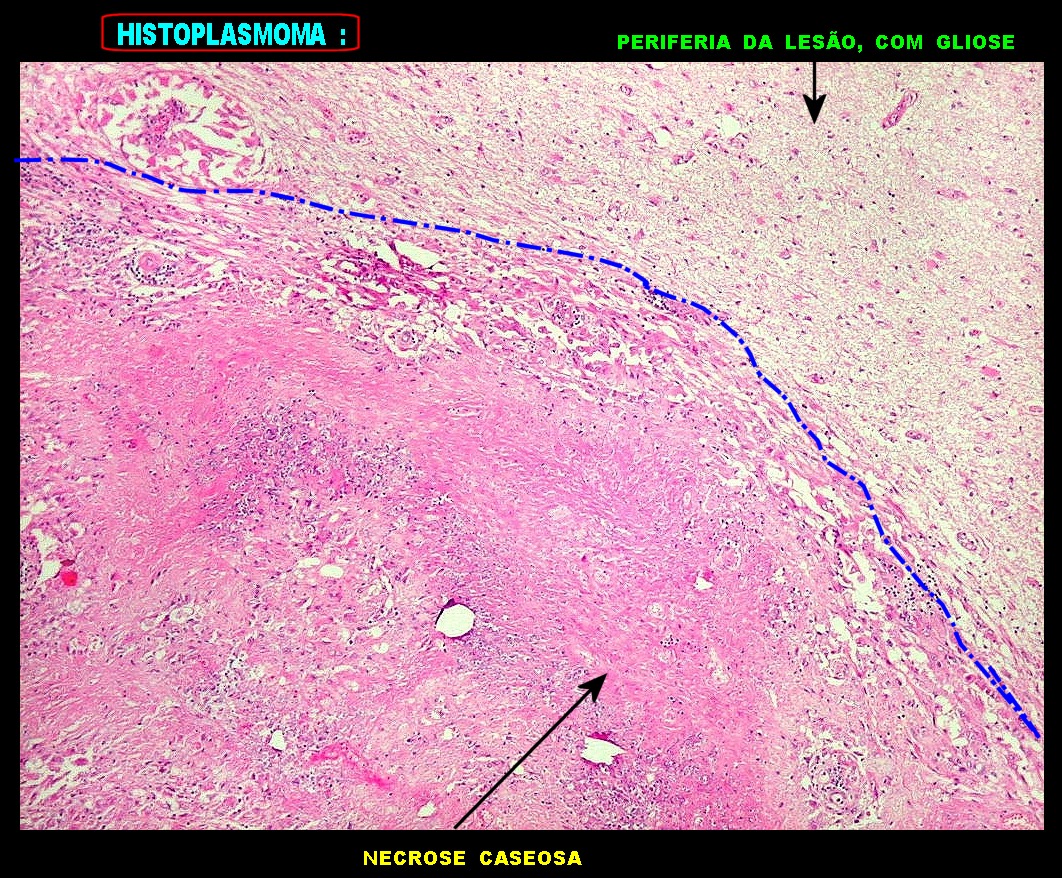
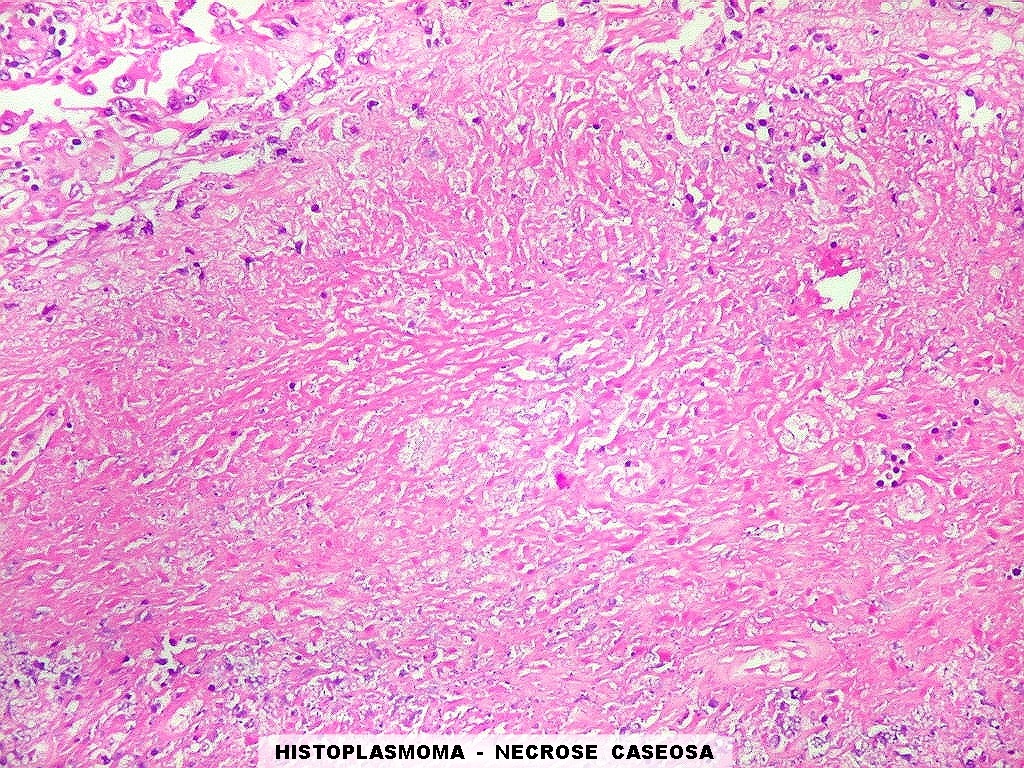
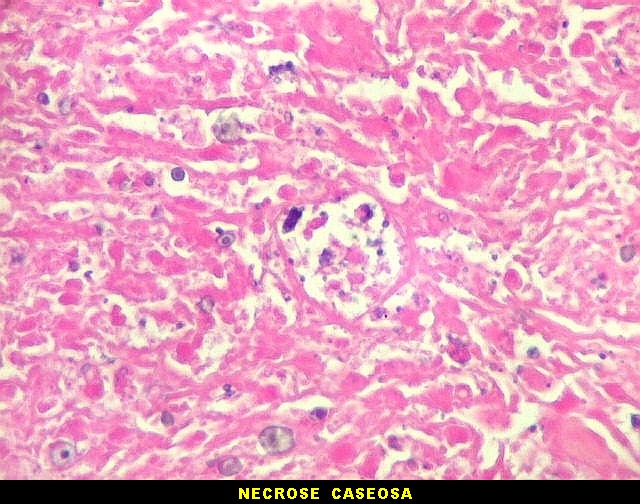
| Lesão fibrótica / gliótica no forâmen de Monro e comissura anterior. Esta lesão foi observada na RM de 6 meses pré-óbito (#2) e identificada na necrópsia. Corresponde a um histoplasmoma, semelhante aos tuberculomas da tuberculose. Apresenta tecido glial (astrócitos fibrosos), fibroblastos, infiltrado inflamatório crônico linfocitário, necrose caseosa e abundantes parasitas. | ||
 |
 |
 |
 |
 |
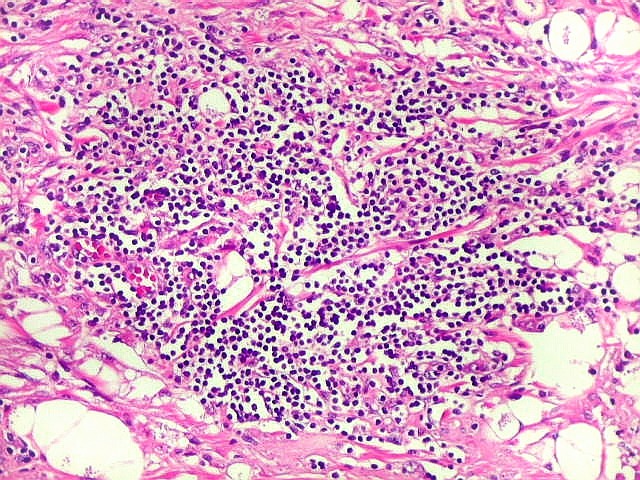 |
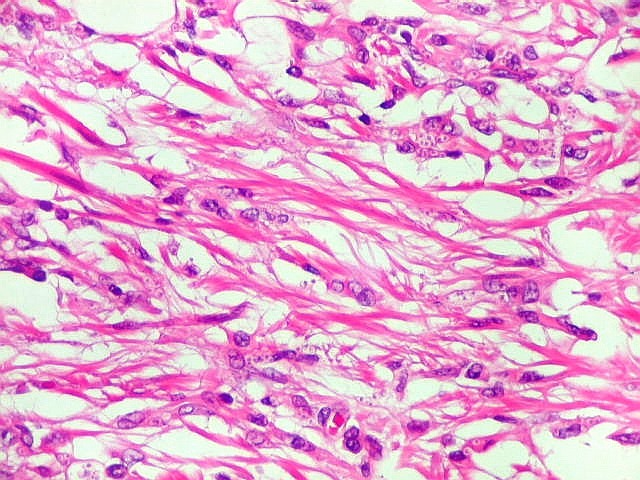 |
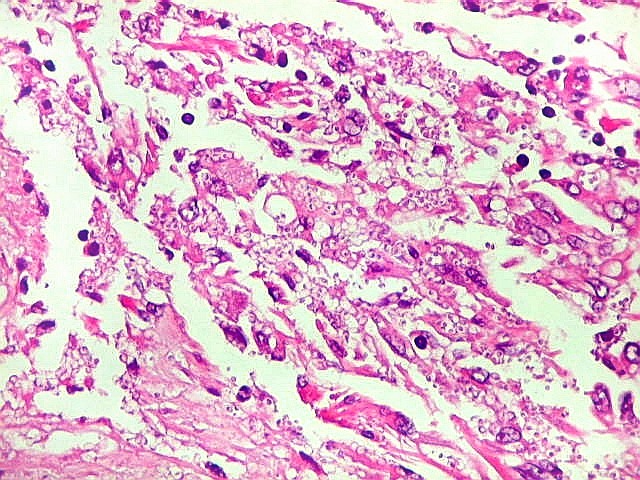 |
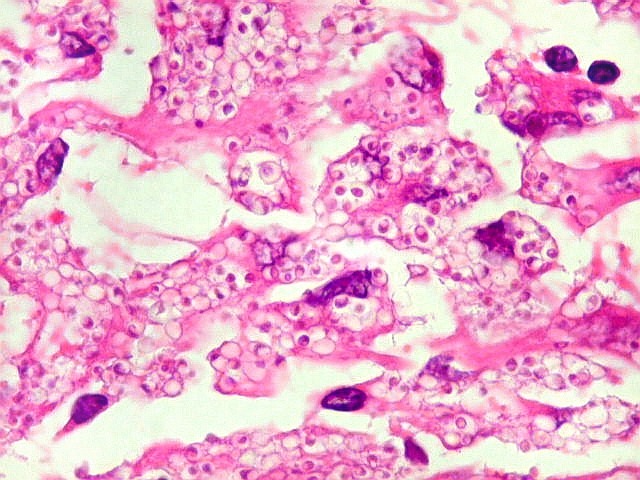 |
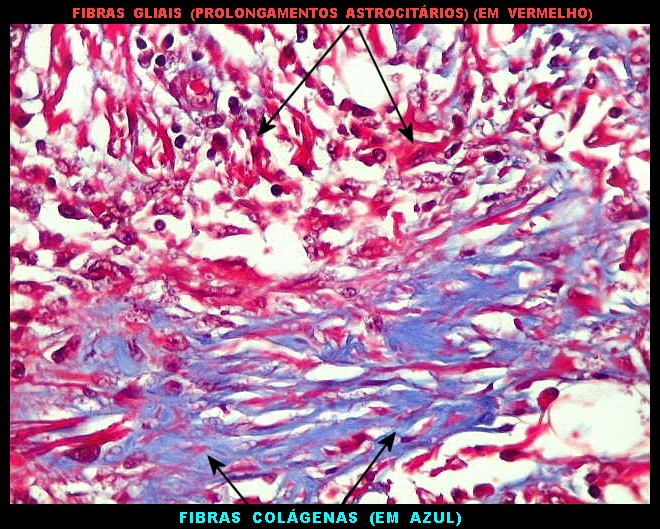
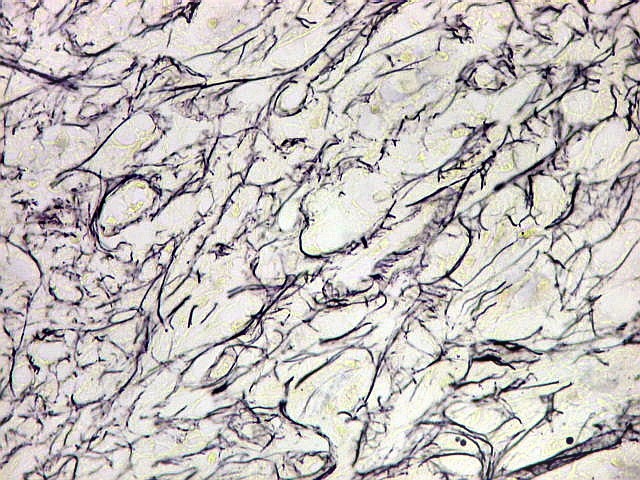
| Tricrômico de Masson, reticulina. Mostram fibras colágenas (em azul no Masson) e reticulínicas (finas, em negro), denotando participação de fibroblastos na lesão. | |
 |
 |
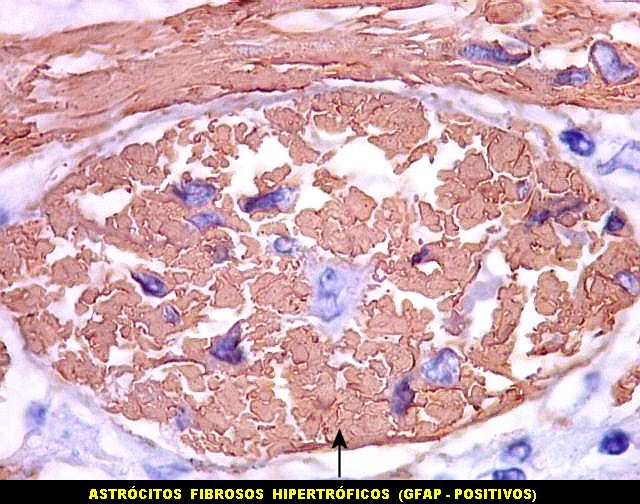
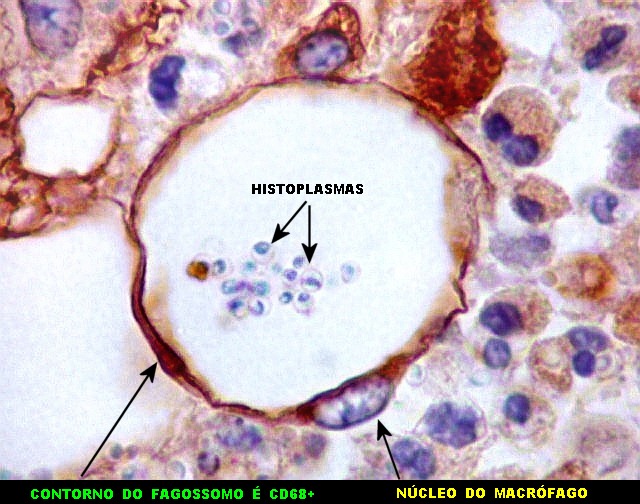
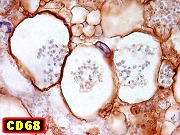
| Imunohistoquímica. Astrócitos fibrosos são marcados para GFAP. Macrófagos com seus fagossomos dilatados são positivos para CD68 e HAM-56. | |
 |
 |
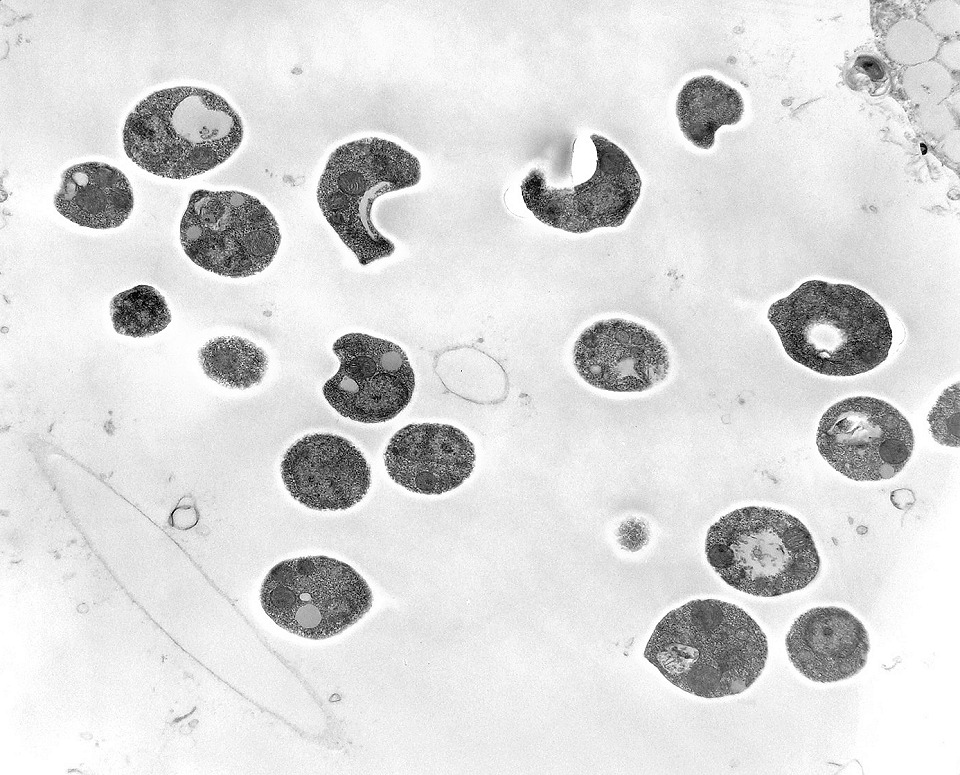
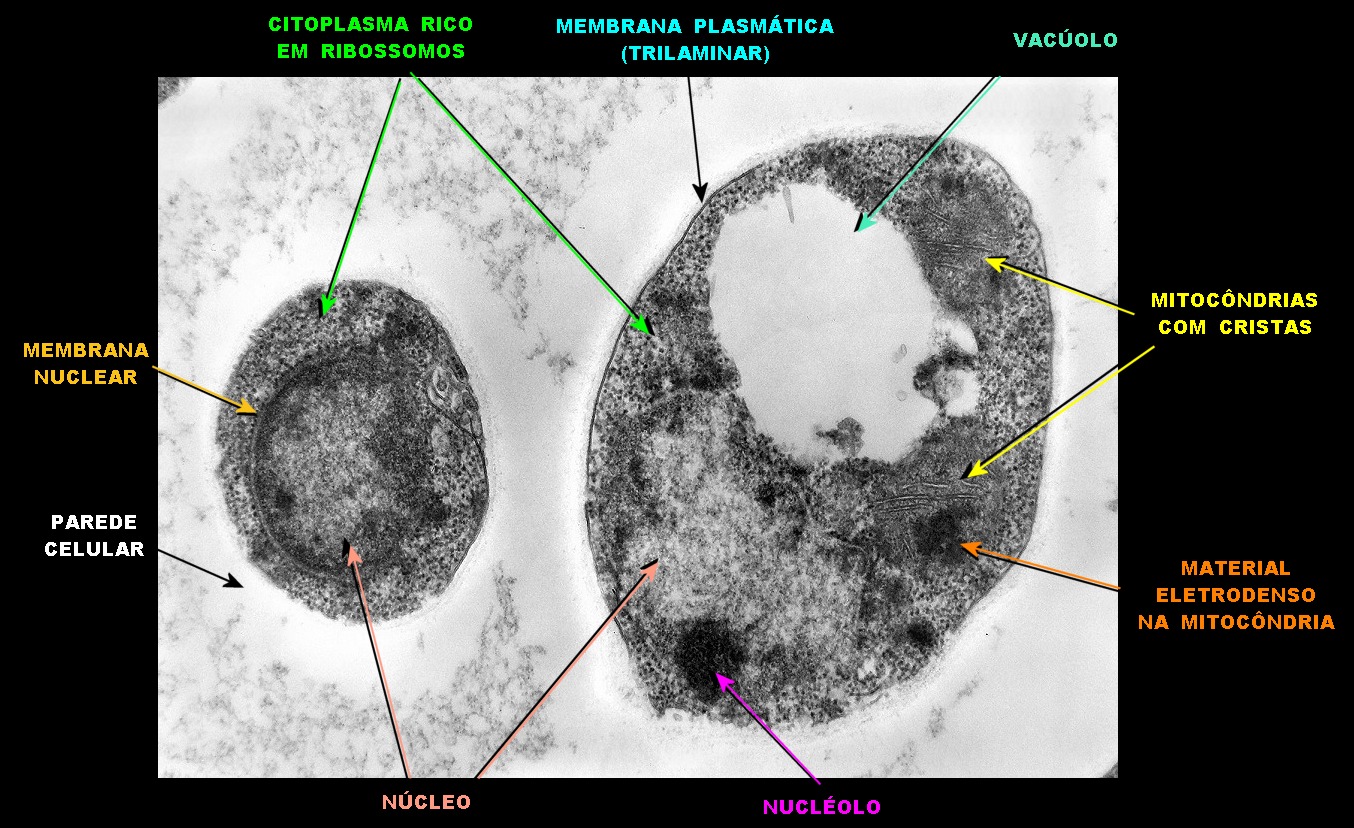
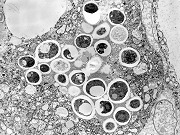
| Microscopia eletrônica. Fungos em fagossomos são na maioria viáveis, reconhecendo-se núcleo, citoplasma com ribossomos, mitocôndrias, vacúolo e parede celular. Para mais imagens, clique. | |
 |
 |
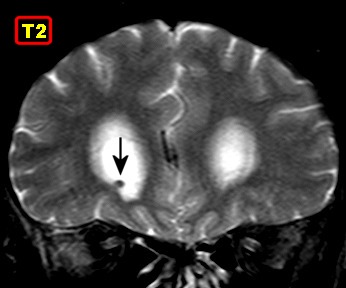
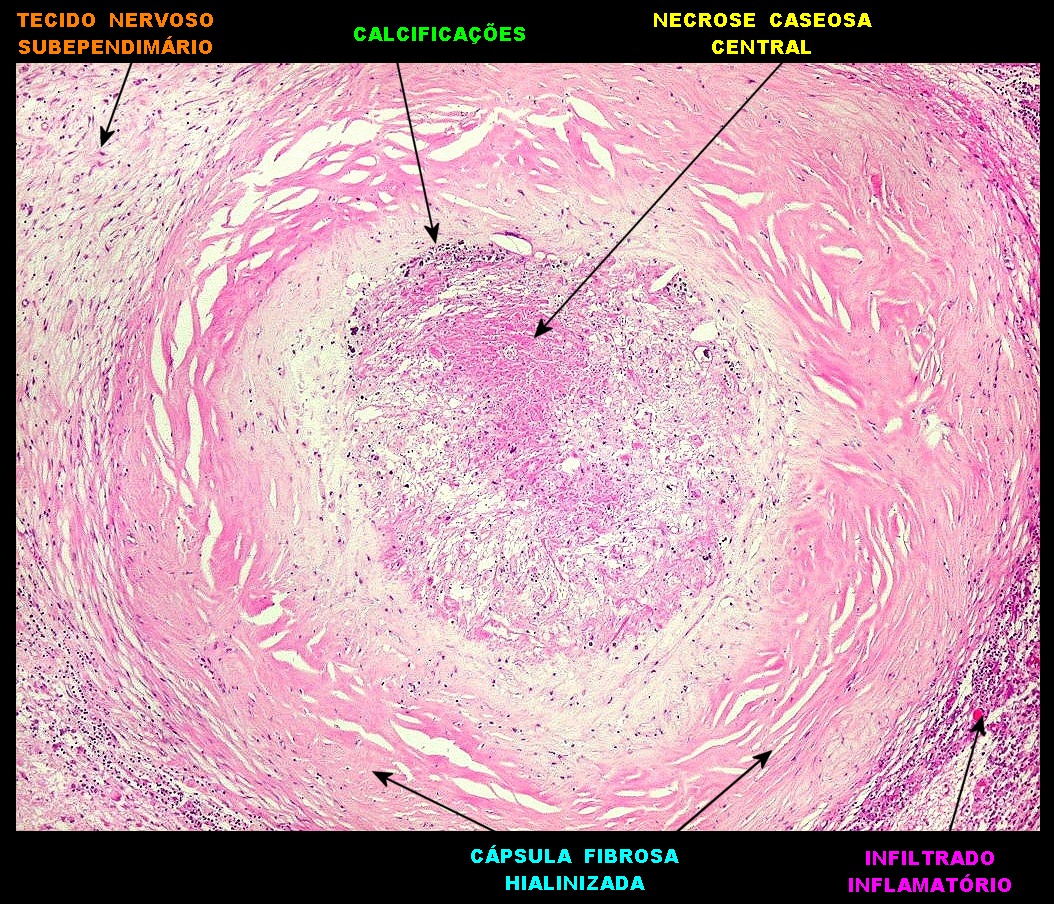
| Lesão no corno anterior do ventrículo lateral direito. Outro diminuto histoplasmoma com necrose caseosa central, calcificações e parasitas na periferia, detectado originalmente na RM de setembro de 2011 (lesão #1), na peça de autópsia e histologicamente. | ||
 |
 |
 |
 |
 |
 |
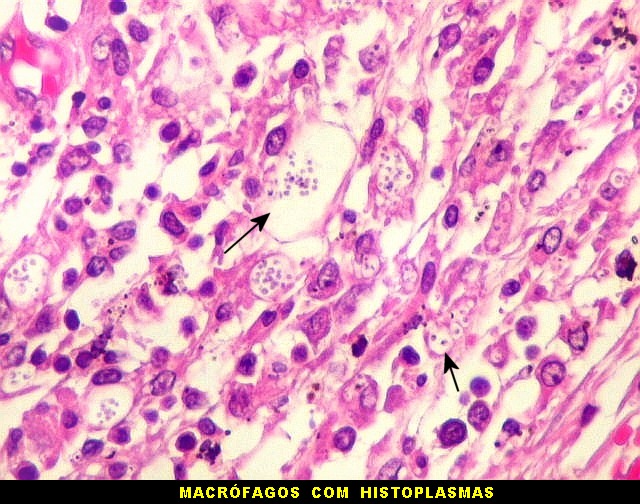 |
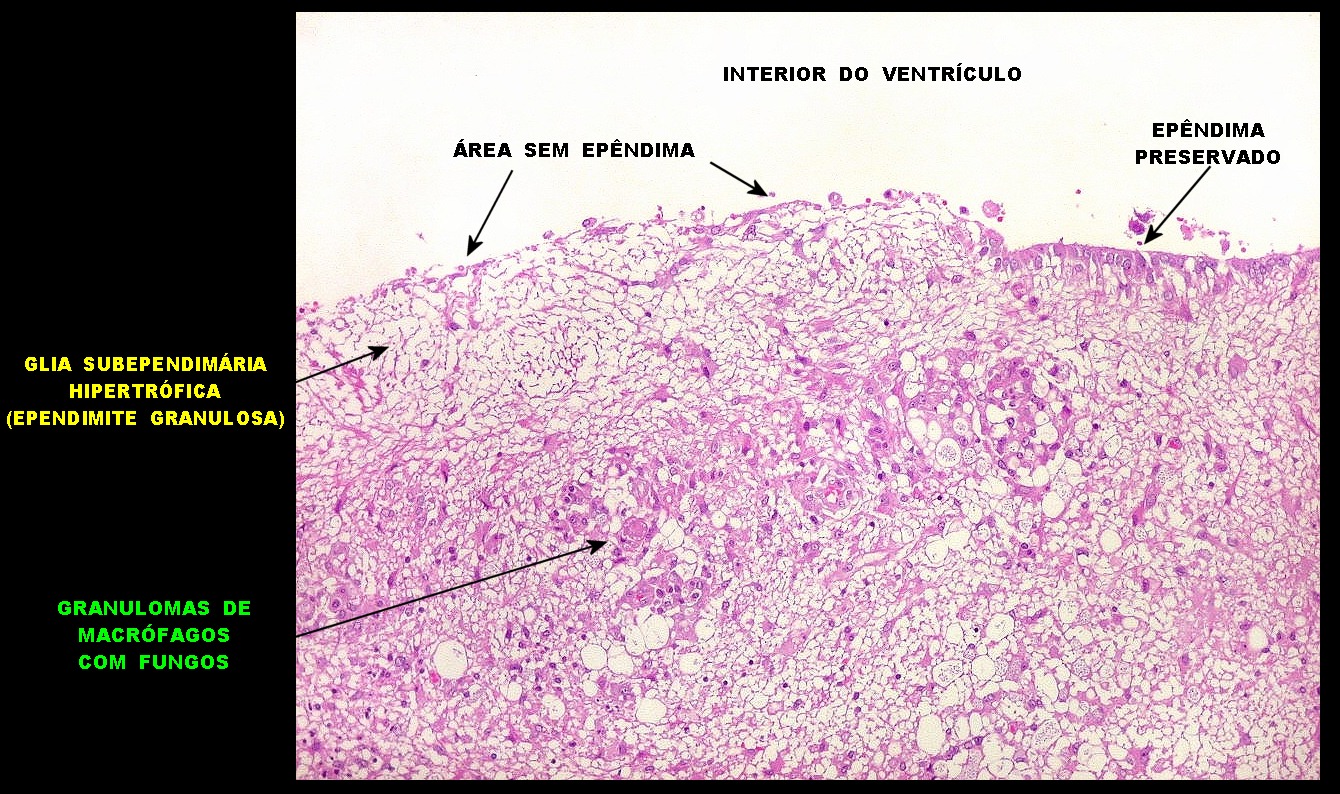
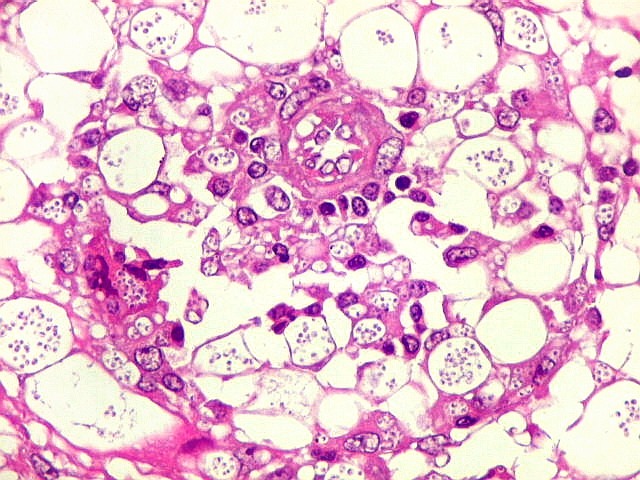
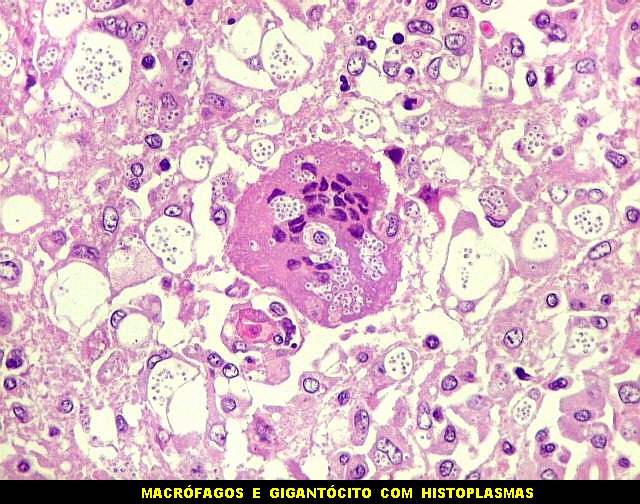
| Ependimite no ventrículo lateral. Áreas de desnudação do epêndima, com hipertrofia dos astrócitos subjacentes (ependimite granulosa). Infiltrado inflamatório perivascular subependimário, por vezes com manguitos de macrófagos ricos em parasitas. Vasculite necrosante manifesta-se macroscopicamente como petéquias. | |
 |
|
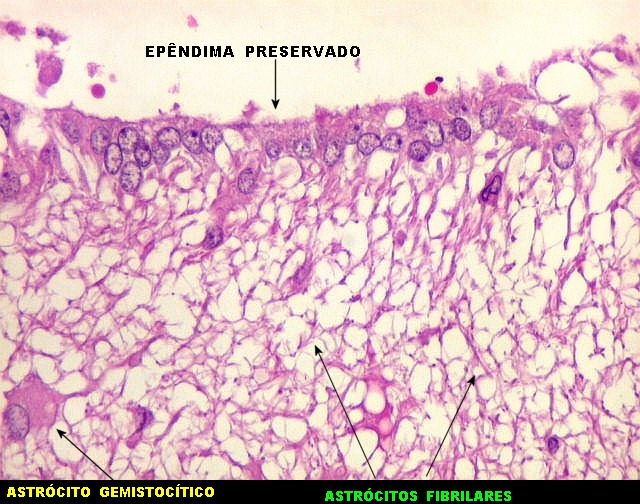 |
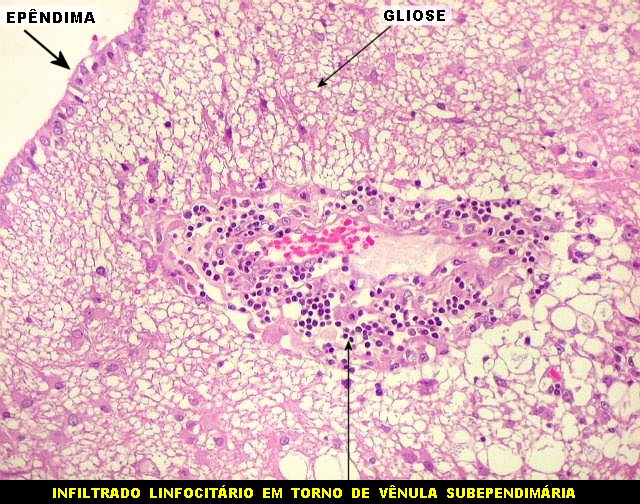 |
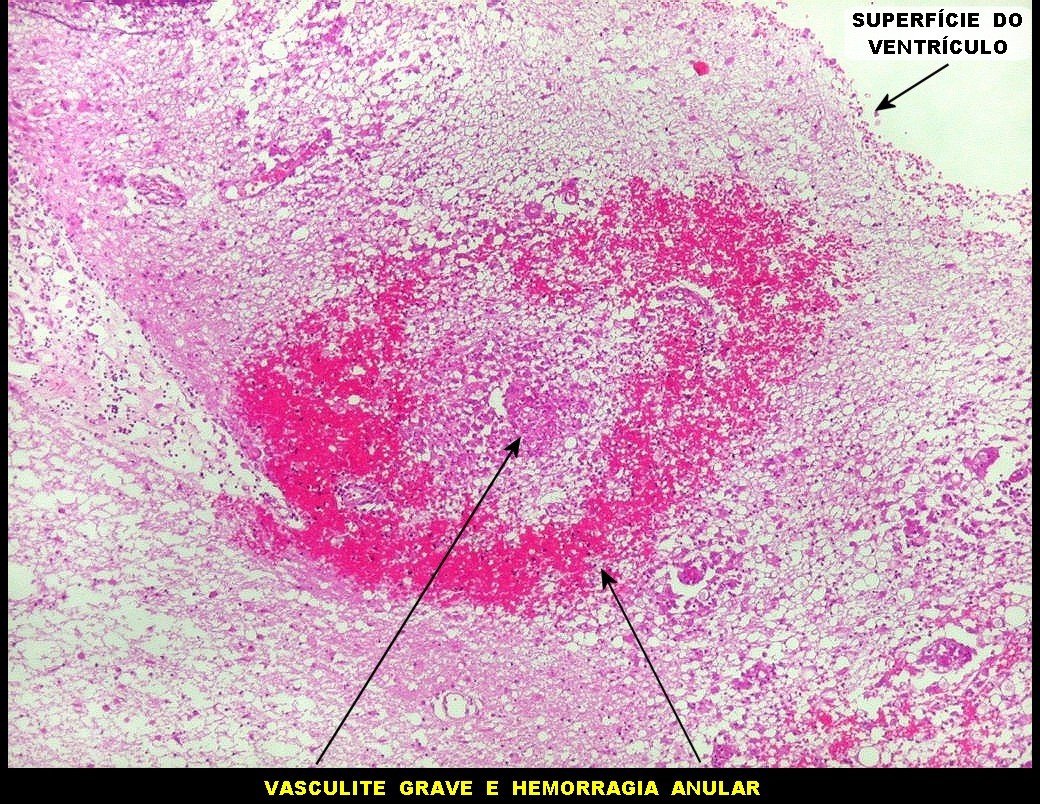 |
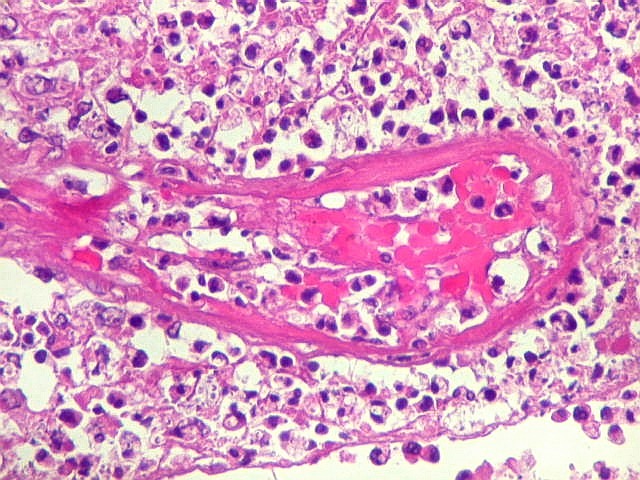 |
 |
 |
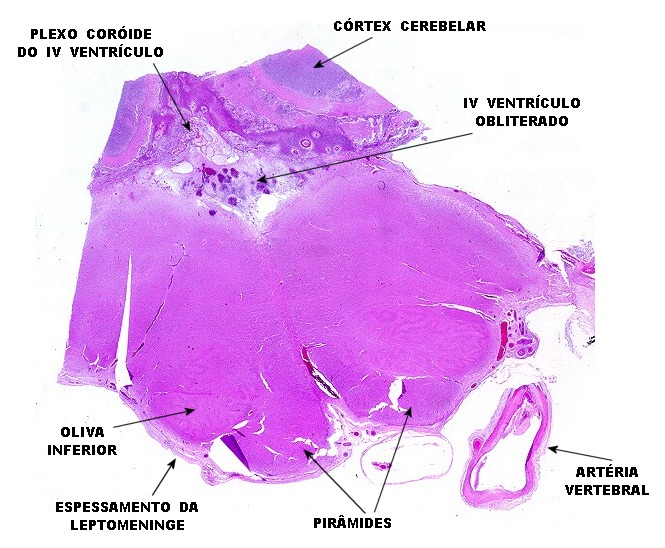
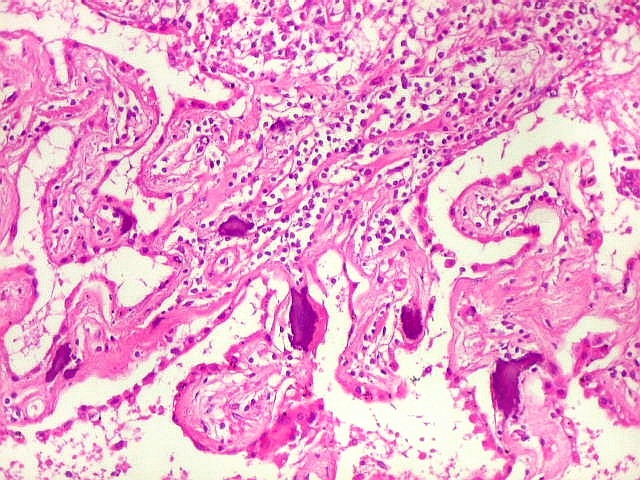
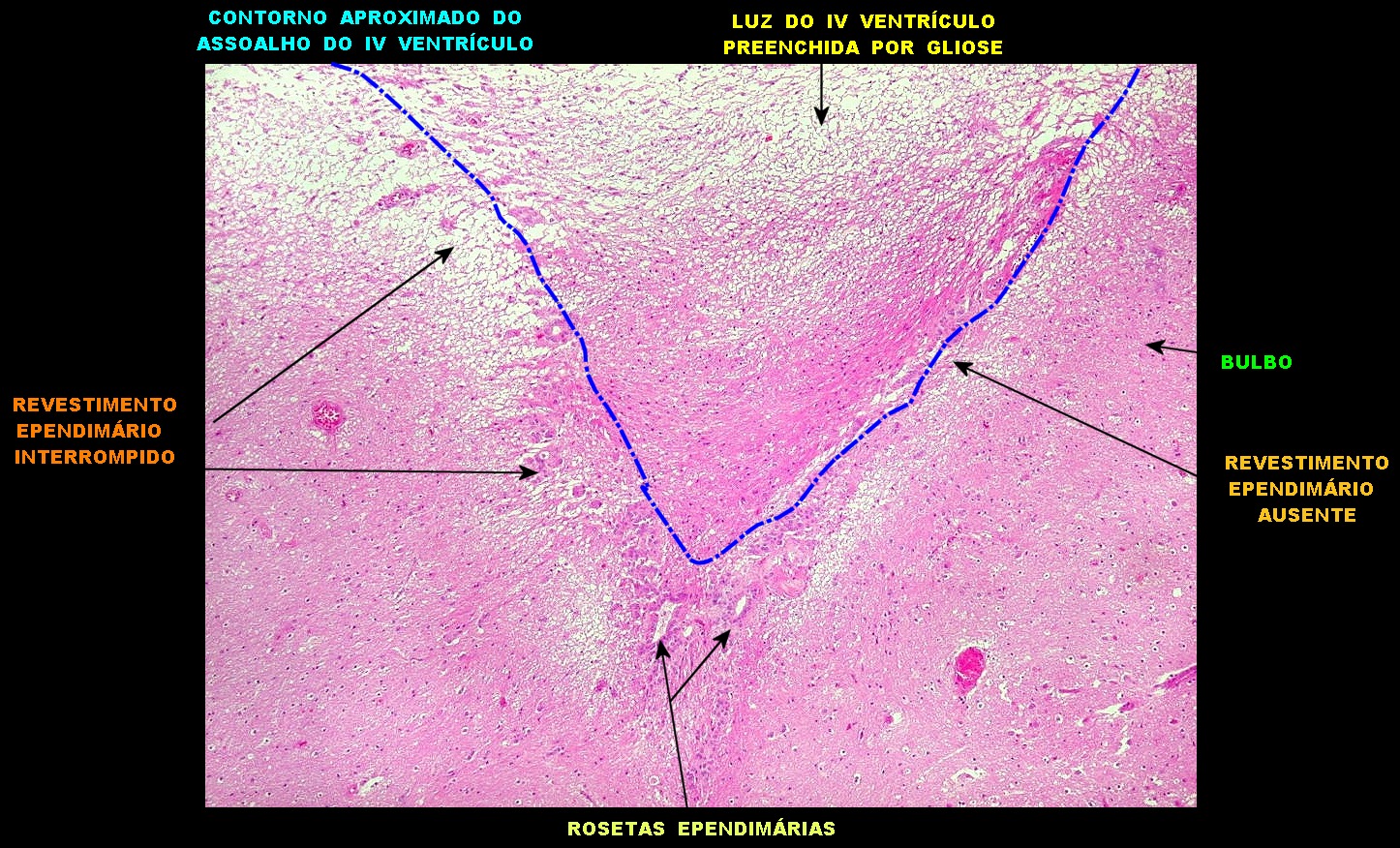
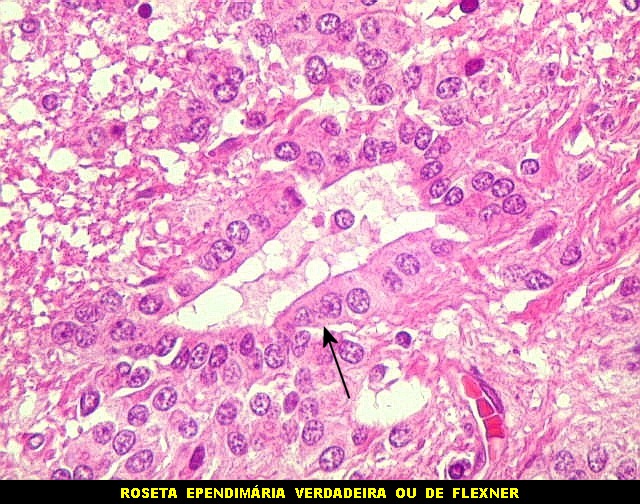
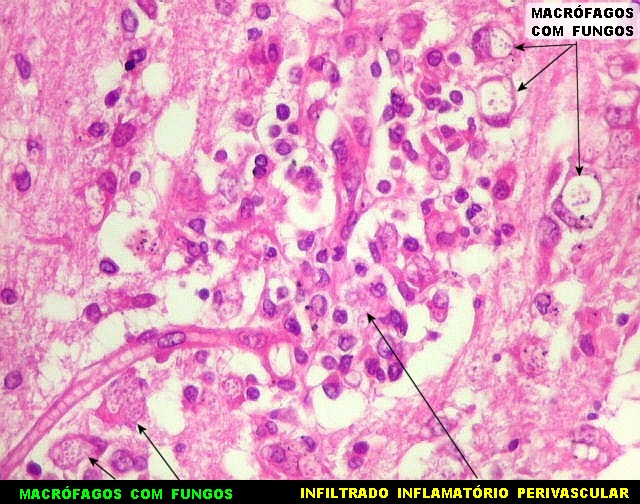
| Lesões no IV ventrículo. Exsudato e gliose obliterando a luz do ventrículo, plexite coróide, ependimite com rosetas de Flexner e inflamação das folhas cerebelares adjacentes. | |
 |
 |
 |
|
 |
 |
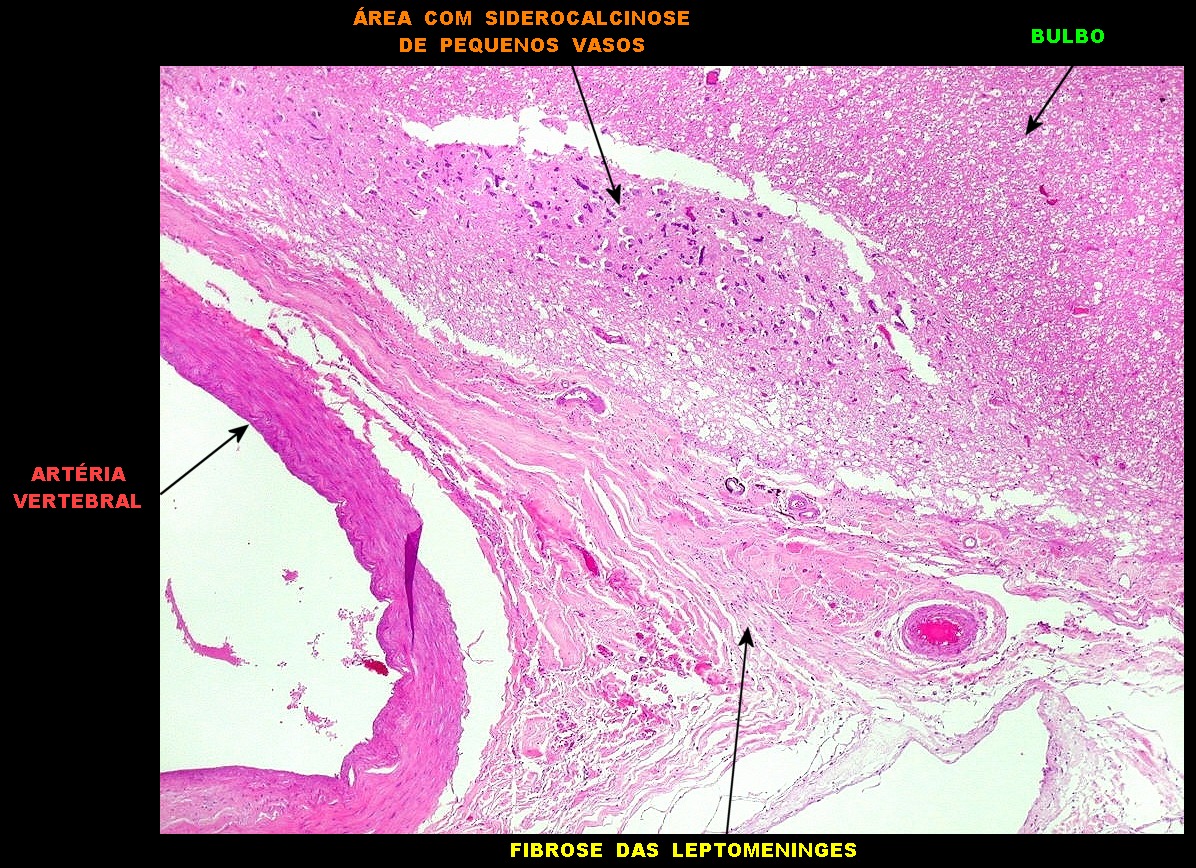
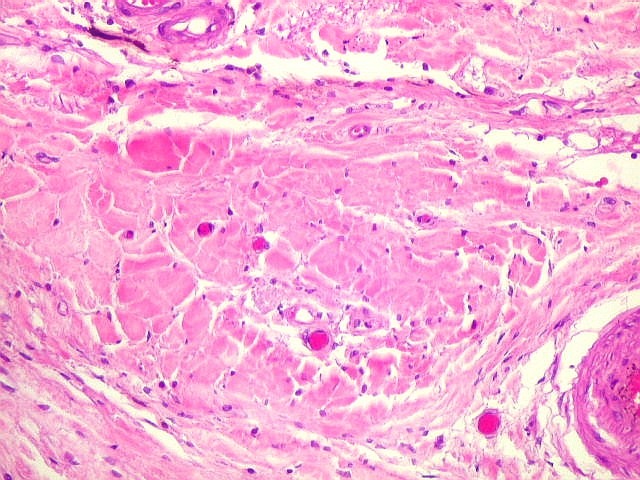
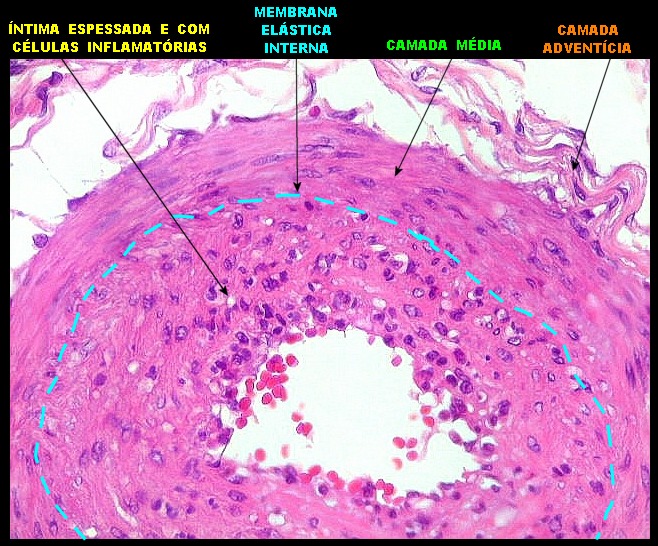
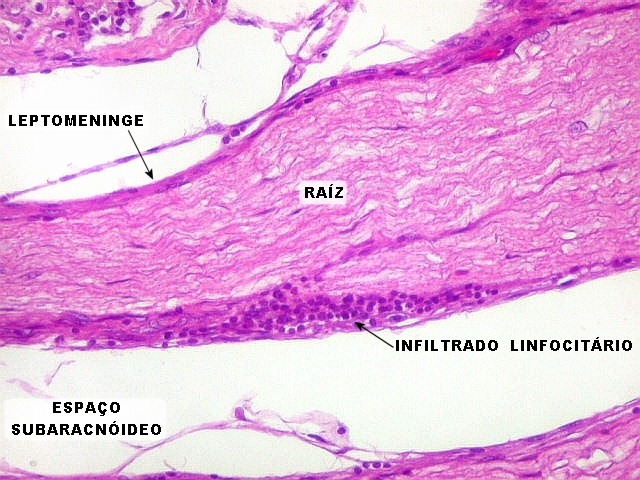
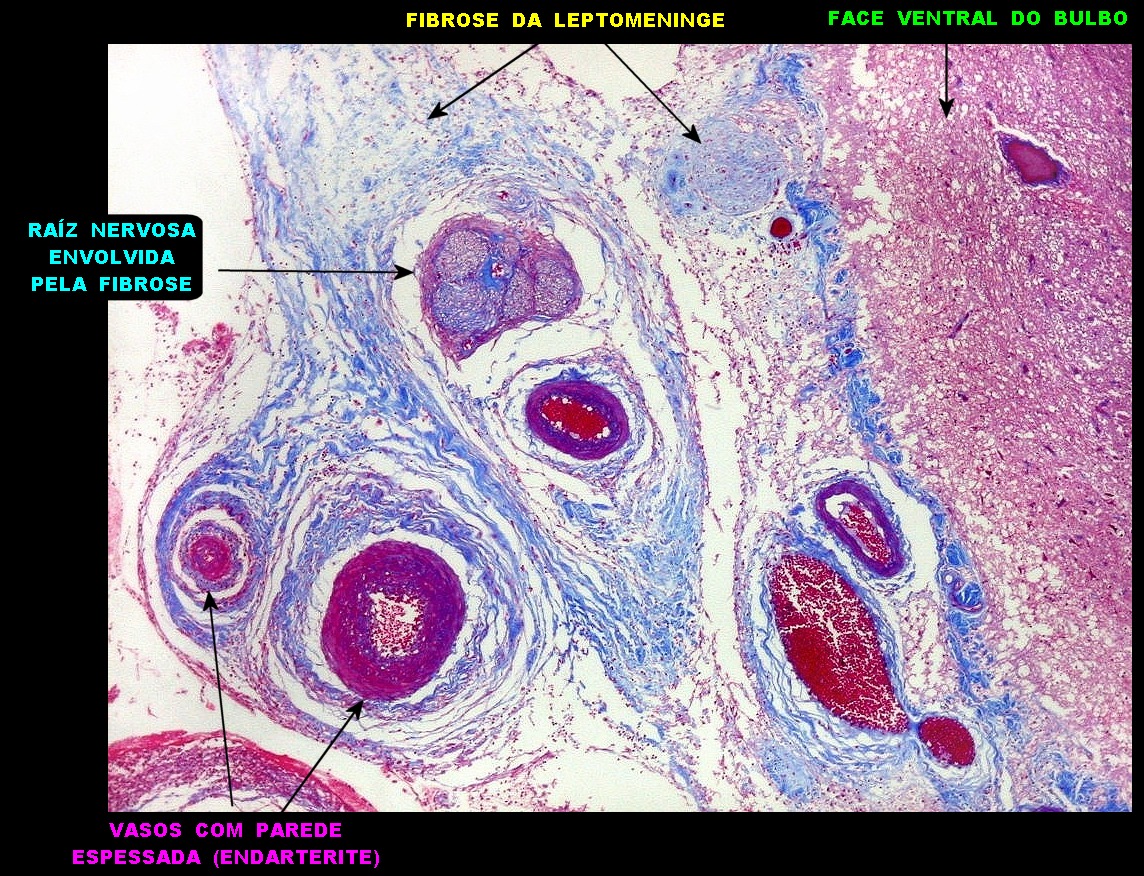
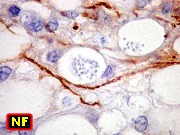
| Lesões nas leptomeninges da base - fibrose, endarterite, radiculite. Há fibrose crônica de longa duração das leptomeninges na face anterior do tronco cerebral, aqui demonstrada em HE e tricrômico de Masson. O processo inflamatório crônico levou a espessamento da íntima de pequenas artérias (endarterite produtiva) e atinge também raízes de nervos cranianos (radiculite). | |
 |
 |
 |
 |
 |
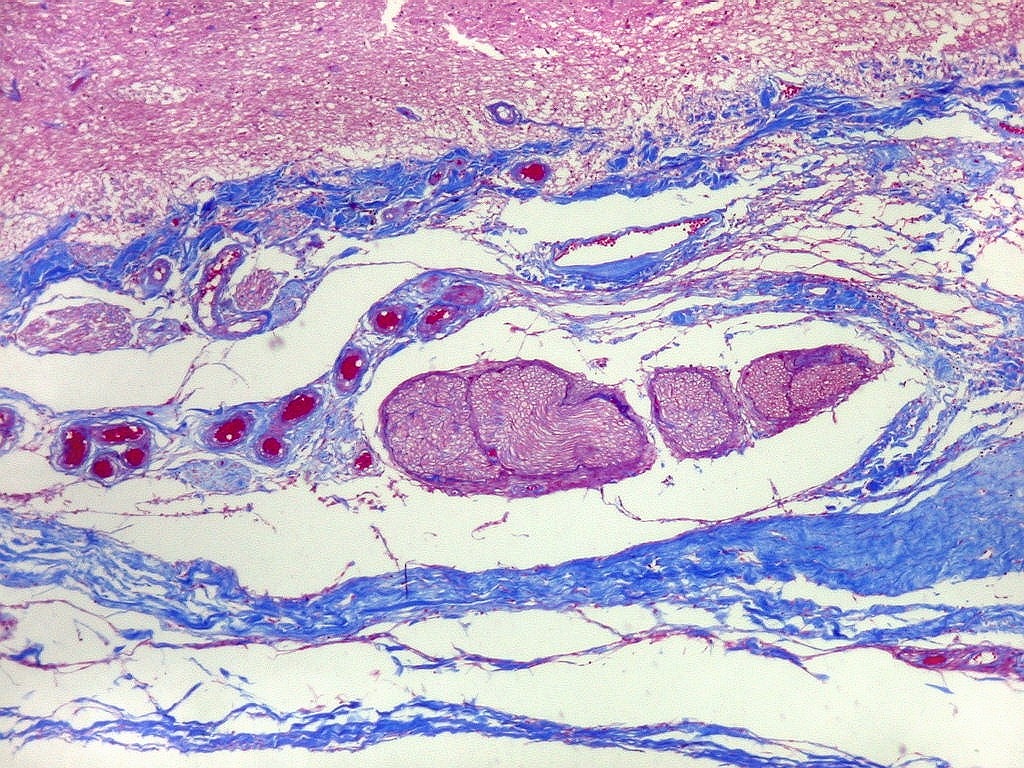 |
| Abaixo, destaques da microscopia, com acesso direto às páginas. HE. | ||
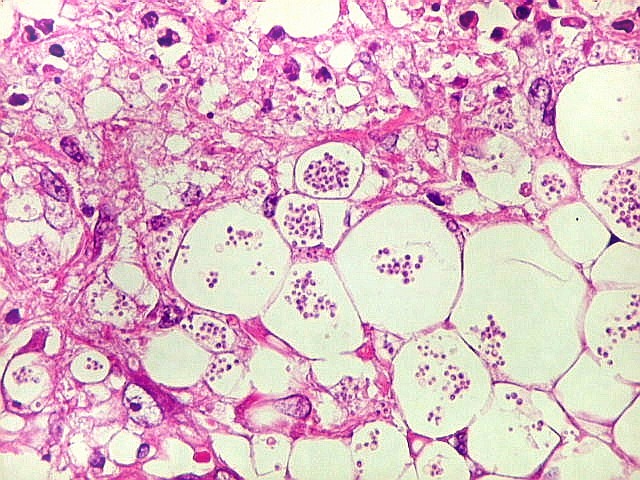
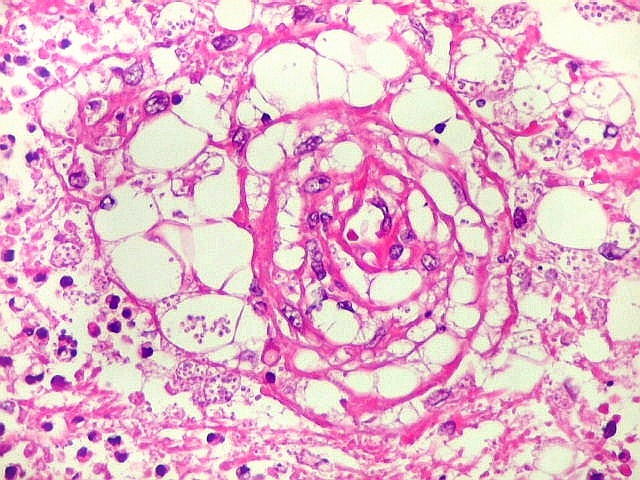
| Lesões na parede do III ventrículo. Fungos em fagossomos de macrófagos | Idem, vasculite | Lesão gliótica/fibrótica na comissura anterior. Necrose caseosa |
 |
 |
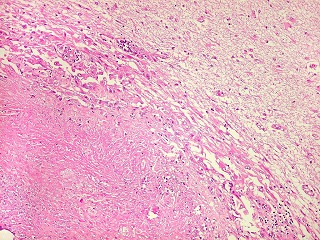 |
| Idem, infiltrado inflamatório crônico | Idem, gliose, fibrose | Idem, histoplasmas |
 |
 |
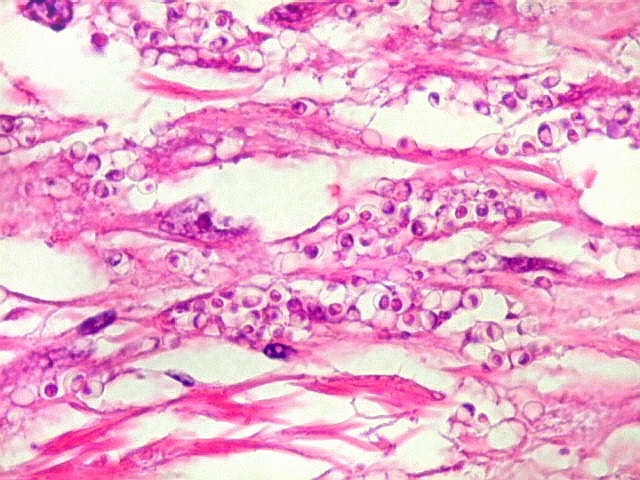 |
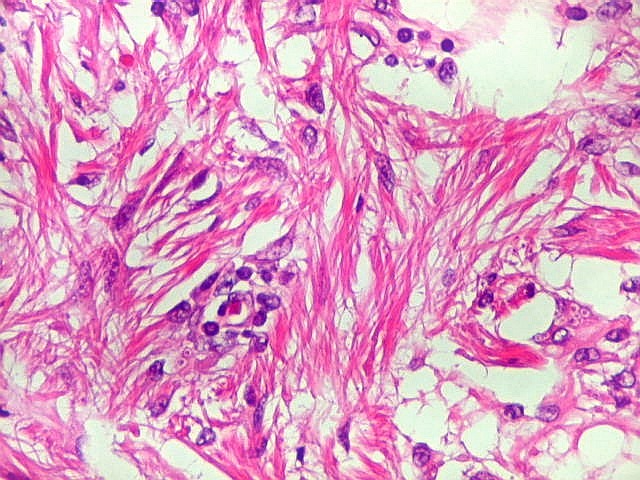
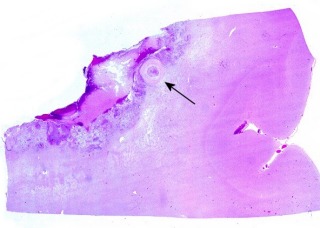
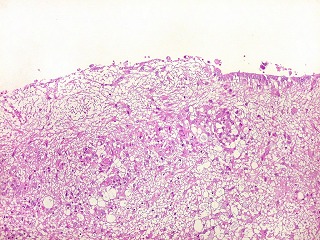
| Lesões ependimárias supratentoriais. Nódulo fibrótico calcificado | Ependimite granulosa, petéquias | Vasculite subependimária |
 |
 |
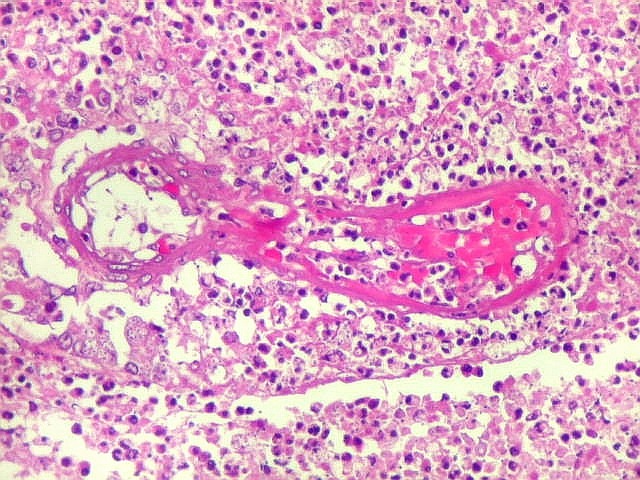 |
| Lesões no IV ventrículo. Plexite coróide | Cerebelite, arterite | Ependimite |
 |
 |
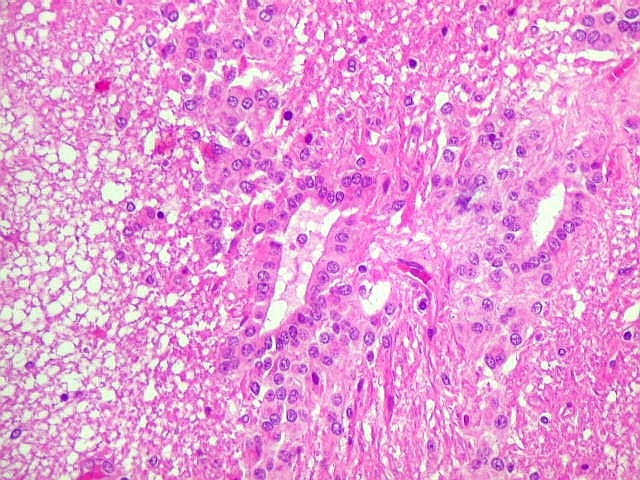 |
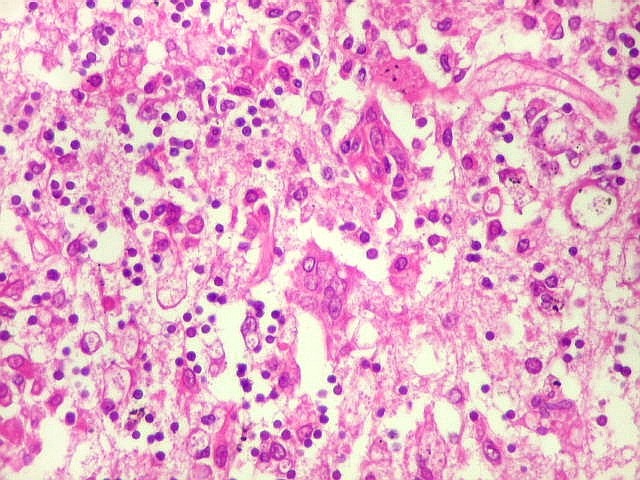
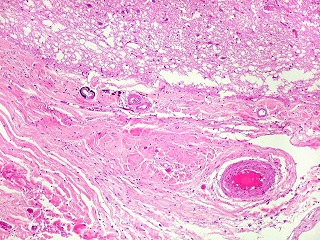
| Lesões nas meninges da base. Fibrose | Radiculite | Endarterite obliterante. Siderocalcinose |
 |
 |
 |
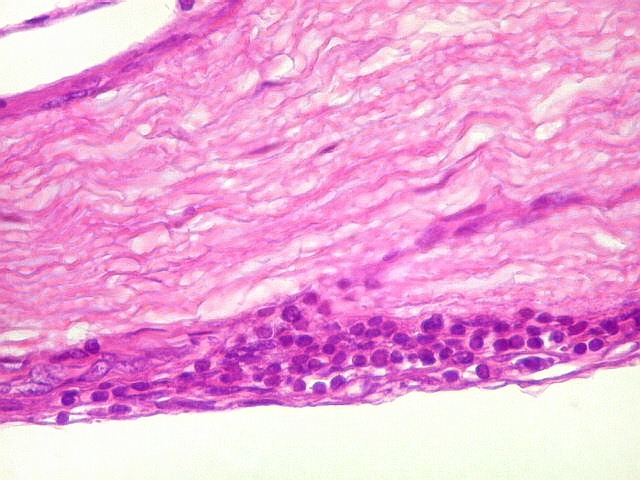
| Destaques das colorações especiais. | ||
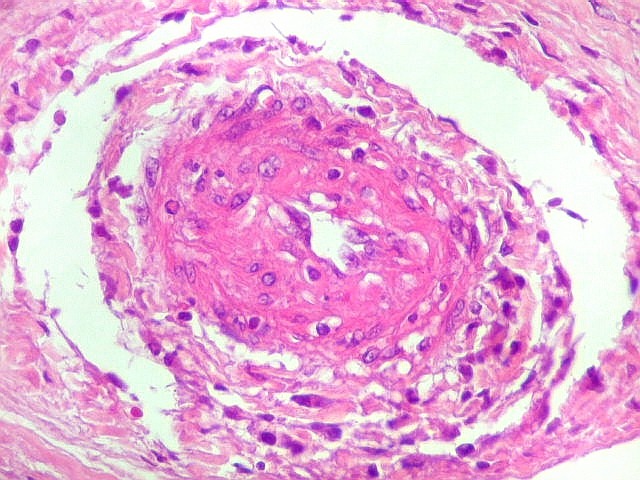
| Tricrômico de Masson. Lesão gliótica - fibrótica na comissura anterior | Histoplasmas | Fibrose das leptomeninges da base. |
 |
 |
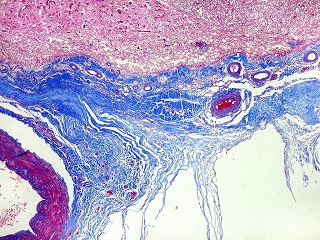 |
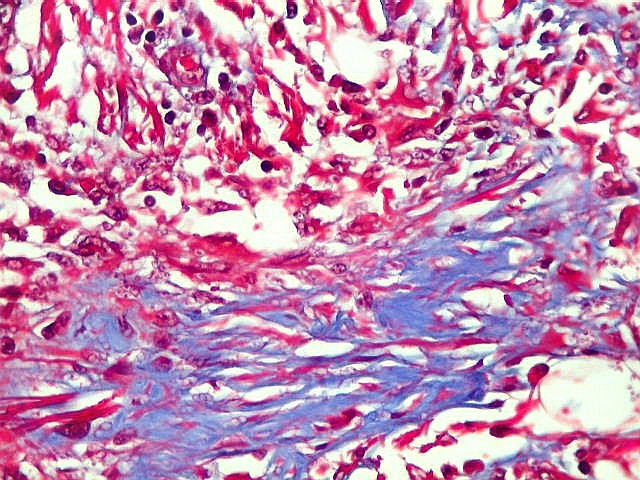
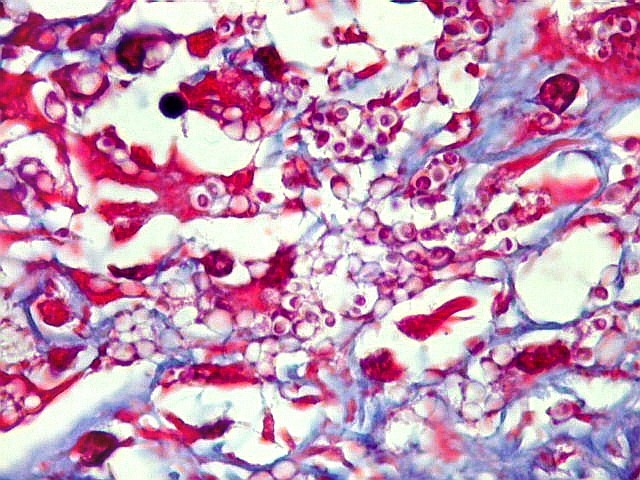
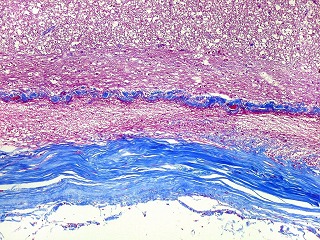
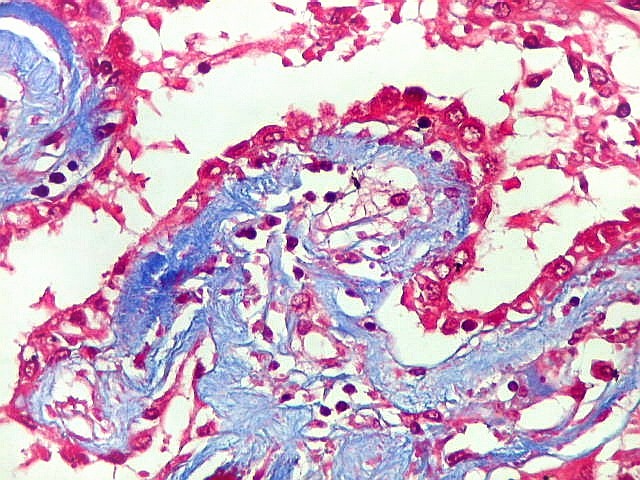
| Reação glial entre a pia e a aracnóide | Plexite coróide do IV ventrículo | Reticulina. Lesão gliótica - fibrótica na comissura anterior |
 |
 |
 |
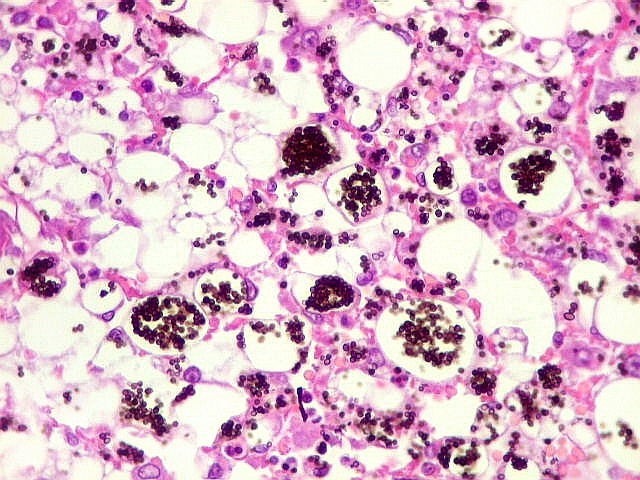
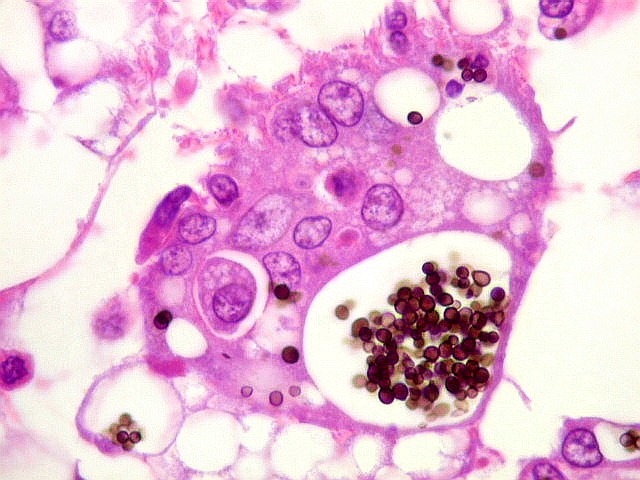
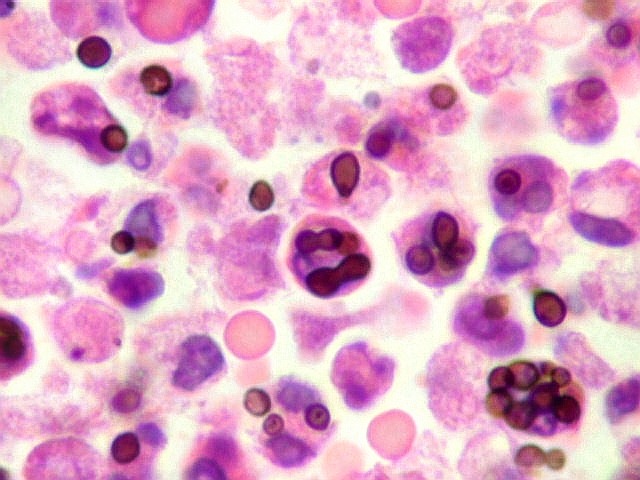
| Grocott + HE. Excepcional riqueza de parasitas na lesão em torno do III ventrículo | Fungos em fagossomos de macrófagos | Fungos no citoplasma de neutrófilos |
 |
 |
 |
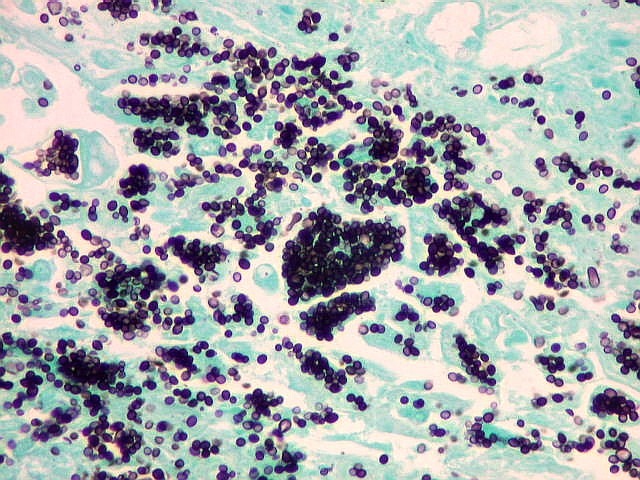
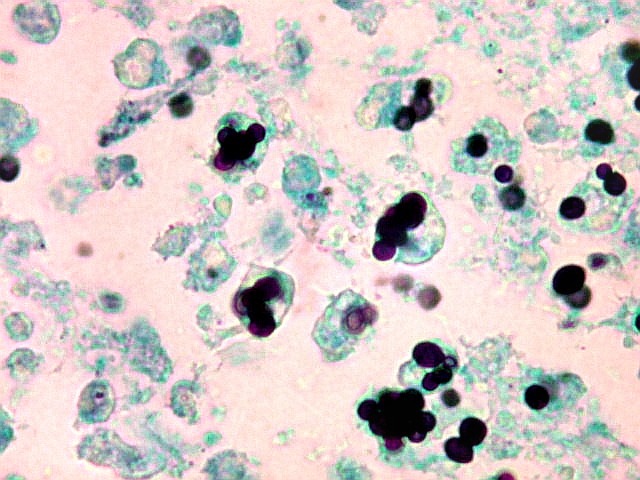
| Grocott + Verde Luz. Histoplasmas no tecido em torno do III ventrículo, na lesão da comissura anterior | Histoplasmas em neutrófilos | PAS + hematoxilina. Fungos em fagossomos de macrófagos |
 |
 |
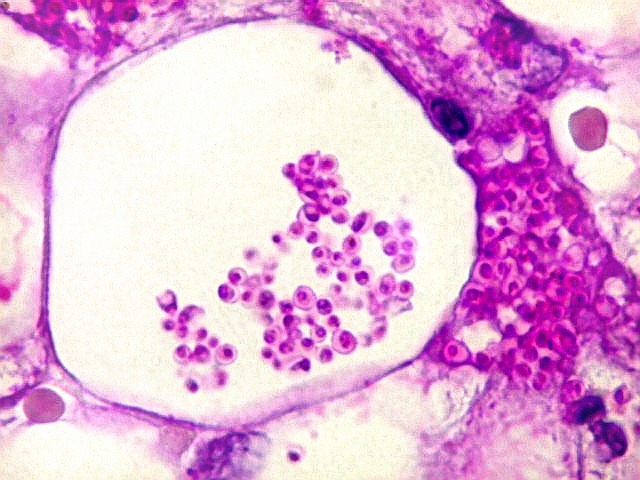 |
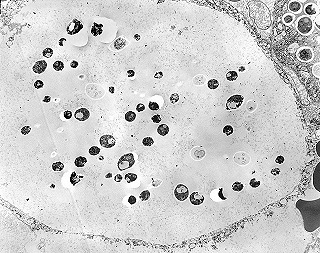
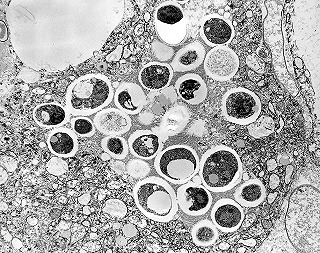
| Destaques da microscopia eletrônica. | ||
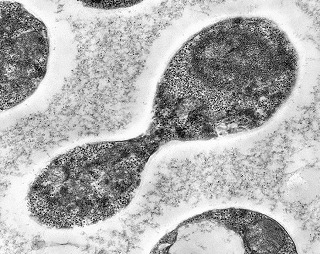
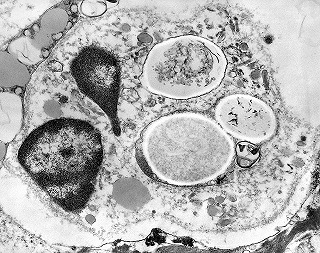
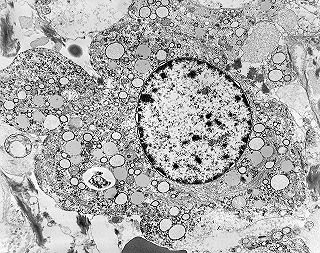
| Histoplasmas em fagossomos de macrófagos | Variações morfológicas | Ultraestrutura dos histoplasmas |
 |
 |
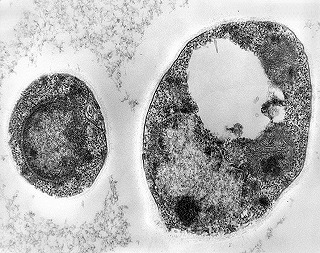 |
| Divisão celular | Fungos degenerados | Astrócitos gemistocíticos |
 |
 |
 |
| HISTOPLASMOSE
Histórico. Descoberta por S. Darling em 1906 ao necropsiar 3 pacientes na região do Canal do Panamá. O agente etiológico foi considerado um fungo em brotamento por Rocha Lima em 1912. De Monbreun (1933-34) confirmou a natureza fúngica obtendo culturas a partir de material clínico. Demonstrou que o Histoplasma capsulatum é um fungo difásico, que cresce na forma de micélio filamentoso a 28ºC, em cultura em materiais comuns. Em agar sangue a 37ºC, apresenta-se na forma de micélio unicelular em brotamento (ou gemulante, a mesma encontrada nos tecidos parasitados). Primeira observação na América do Sul Baliña et al (1941) em Buenos Aires. Em 1949, Emmons conseguiu o isolamento do fungo a partir do solo, demonstrando ser esta a fonte de infecção para homem e animais. Etiologia. No continente americano a histoplasmose tem um único agente, o Histoplasma capsulatum. É encontrado nos tecidos parasitados na forma de células esféricas ou ovóides (leveduras), de 3 a 4 mm de diâmetro, às vezes com um único brotamento em um dos polos. Na maioria, são encontrados no citoplasma de macrófagos. Em preparações por HE ou Giemsa, mostram a parede celular descorada, que aparece como um halo claro. No interior, observa-se uma única massa cromática, de forma semilunar, corada em violeta ou azul escuro. Com PAS, tomam cor vermelha ou magenta. O melhor método de coloração é a metenamina-prata de Grocott, que cora a parede celular do fungo em marrom a negro. Uma breve contracoloração por HE revela as células do tecido em tons suaves, permitindo estudar a localização predominantemente intracelular dos parasitas. Epidemiologia. Infecção por Histoplasma capsulatum é adquirida por inalação de partículas de poeira a partir de solo contaminado por fezes de pássaros ou morcegos. Estas contêm os esporos (microconidia) que são a forma infecciosa do fungo. A doença não é transmissível homem a homem, nem de animais para o homem. O fungo vive saprofiticamente no solo, em sua fase filamentosa, e seus esporos são inalados ou ingeridos pelo homem ou animais. É freqüentemente isolado de terras ricas em dejetos de aves, que não se infectam. O fungo foi também encontrado em porões ou grutas habitadas por morcegos frugívoros e de hábitos noturnos. A infecção pelo fungo é comum (estimada em 25% da população nos Estados Unidos), mas a doença é rara. Inquéritos epidemiológicos com a reação de hipersensibilidade cutânea à histoplasmina (análoga ao teste de Mantoux com tuberculina) revelaram que os casos de histoplasmose diagnosticados clinica- ou micologicamente correspondem de 1:1000 a 1:2000 do total de infectados (que tiveram contato com o parasita). A grande maioria das pessoas que habitam zonas endêmicas apresenta infecções assintomáticas ou subclínicas que se curam espontaneamente, deixando calcificações pulmonares em 1/3 dos casos. Ambos sexos, e todas idades e raças podem ser afetadas. Há dois picos de incidência, um na infância, com maior envolvimento do sistema linfo-reticular, e outro na 5a. 6a. décadas. Formas clínicas.
Como o Mycobacterium tuberculosis, o Histoplasma capsulatum
é um parasita intracelular de macrófagos. As apresentações
clínicas e lesões patológicas da histoplasmose são
notavelmente semelhantes às da tuberculose. As principais
formas da doença incluem :
Patogênese. O macrófago é o principal alvo do fungo, que é internalizado (fagocitado) após opsonização por anticorpos. Além disso, o fungo expressa a proteína de choque térmico 60 (heat shock protein 60 ou HSP60) na superfície celular, que se liga a beta-2 integrinas na superfície dos macrófagos. Os histoplasmas que são fagocitados por macrófagos não previamente estimulados multiplicam-se nos fagolisossomos, levando à lise dos macrófagos. Após o primeiro contato, linfócitos T helper CD4+ passam a reconhecer os antígenos e as HSP na superfície do fungo e secretam intérferon gama que ativa os macrófagos a matar os parasitas intracelulares. Os macrófagos também secretam TNF (tumor necrosis factor), que recruta mais macrófagos e também os estimula a lisar os fungos. Pacientes com AIDS, deficientes em imunidade celular, são presas freqüentes da infecção. Anatomia Patológica. Em pulmões de adultos sadios, infecção por Histoplasma produz granulomas de células epitelióides, que sofrem necrose caseosa e podem confluir, formando grandes áreas de consolidação. Liquefação da necrose e eliminação por brônquios resulta em cavernas como as da tuberculose, mas menos freqüentemente que naquela. Quando a doença é controlada espontaneamente ou por drogas, as lesões evoluem a fibrose. As lesões são muito parecidas às da tuberculose, sarcoidose e outras micoses. A diferenciação requer a demonstração dos fungos, que se apresentam como leveduras pequenas de 3-5 mm, com paredes finas, que se coram fortemente pelo método de Grocott da metenamina prata. Reproduzem-se por brotamento simples. Com HE aparecem bem menores, lembrando leishmânias, pois só a parte central do fungo se cora. Os parasitas podem persistir no tecido por anos. Na forma disseminada em imunosuprimidos não há formação de granulomas. Os macrófagos estão ingurgitados por incontáveis parasitas que preenchem todo o citoplasma das células, e são encontrados em todos órgãos e tecidos. Outros métodos de diagnóstico incluem a cultura do fungo e testes sorológicos. Anticorpos são formados já entre 2 a 6 semanas da infecção. Neurohistoplasmose. Envolvimento do sistema nervoso central é raro na histoplasmose (cerca de 7% dos casos) e secundário a doença pulmonar. De 26 pacientes em uma série, 15 tinham meningite, geralmente limitada à base do cérebro. Principais fontes.
|
| Agradecimento. Caso estudado com a médica residente R1, Dra. Ana Kame de Souza Uejo, Depto de Anatomia Patológica, FCM-UNICAMP, Campinas, SP. |
| Página
de resumo do caso.
Mais imagens deste caso: |
RM 26/9/2011 | RM 29/3/2012 | TC 30/3/2012 | |
 |
 |
 |
||
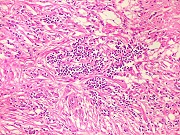
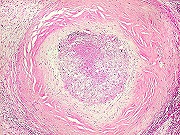
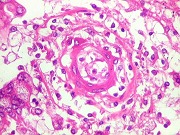
| Macro | HE, lesões no III ventrículo | HE, lesão gliótica / fibrótica na comissura anterior | HE, nódulo necrótico no corno anterior do ventrículo lateral D. | HE, lesões no IV ventrículo |
 |
 |
 |
 |
 |
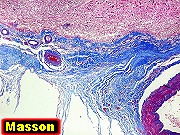
| Tricrômico de Masson, meninges da base | Grocott + HE, Grocott + verde luz, PAS | CD68, HAM-56, CD3, CD20 | GFAP, NF | Microscopia eletrônica |
 |
 |
 |
 |
 |
| Neuropatologia
- Graduação |
Neuropatologia -
Estudos de casos |
Neuroimagem
- Graduação |
Neuroimagem -
Estudos de Casos |
Roteiro
de aulas |
Textos
de apoio |
Correlação
Neuropatologia - Neuroimagem |
| Índice alfabético - Neuro | Adições recentes | Banco de imagens - Neuro | Textos ilustrados | Neuromuscular | Patologia - outros aparelhos | Pages in English |
|
|
|