|
|
1. Macro, HE, Masson, Reticulina |
|
|
|
1. Macro, HE, Masson, Reticulina |
|
| Masc. 12 a. Clique para RM, Macro, HE, Masson, Reticulina, CD68, VIM, 1A4, CD34, Ki67, Texto (granuloma). Texto (miofibroblastos) |
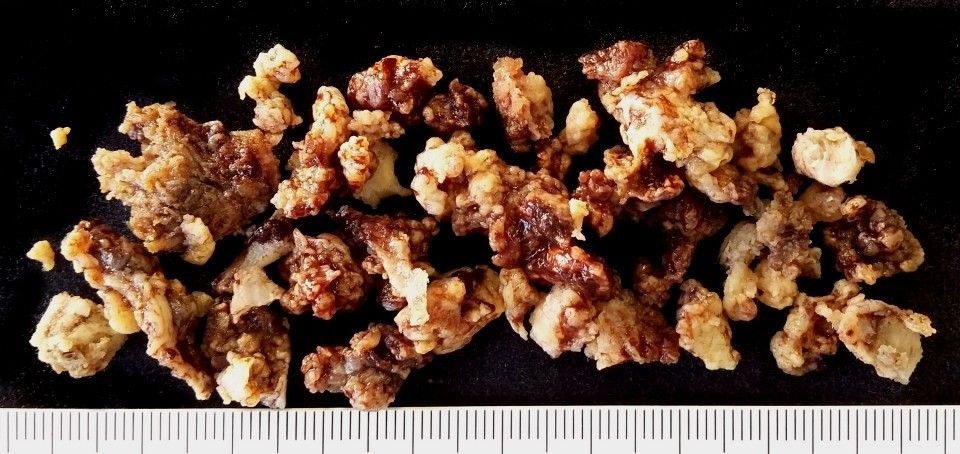
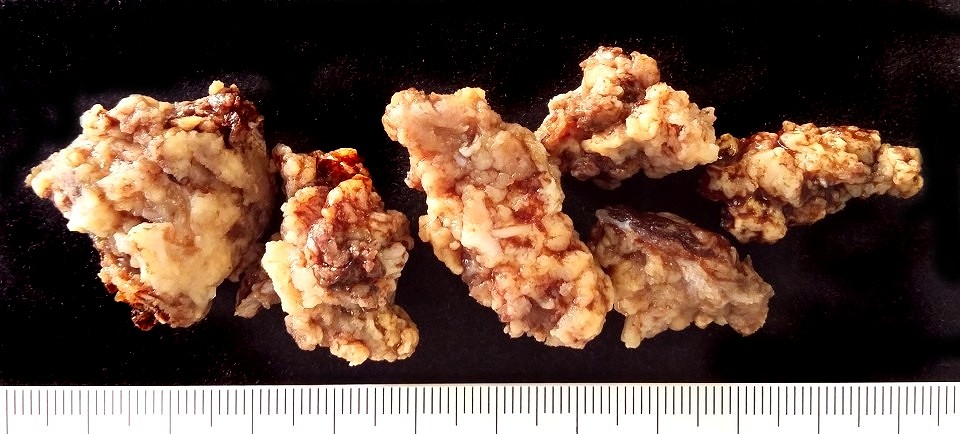
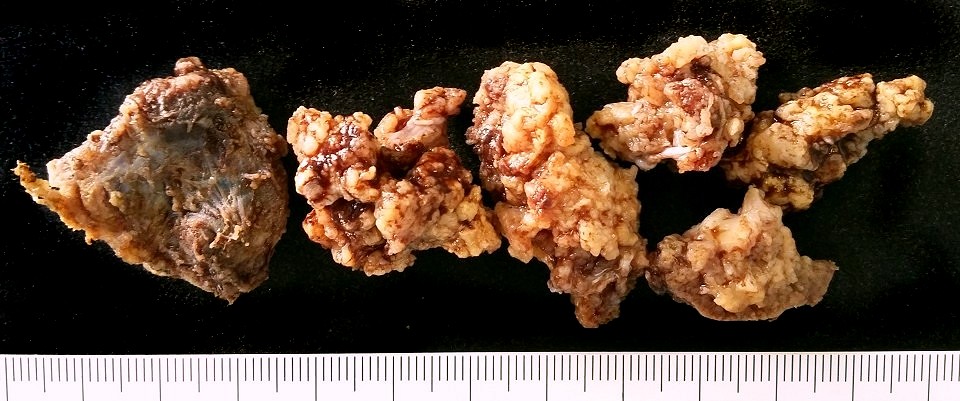
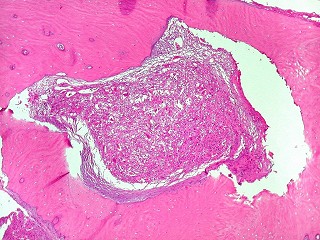
| Espécime
cirúrgico.
Após uma pequena biópsia que revelou a natureza da lesão,
foi executada ampla exérese com curetagem. Os fragmentos eram
irregulares, branco-amarelados a pardo-acastanhados, macios, friáveis,
e mostravam tecido finamente lobulado. Alguns necessitaram descalcificação.
Mediam em conjunto 7,5 x 5 x 2 cm.
Fotos por obséquio dos macroscopistas do Centro Infantil Boldrini, Srs. Irineu Mantovanelli Neto e Aparecido Paulo de Moraes. |
 |
 |
 |
| Destaques da microscopia. | ||
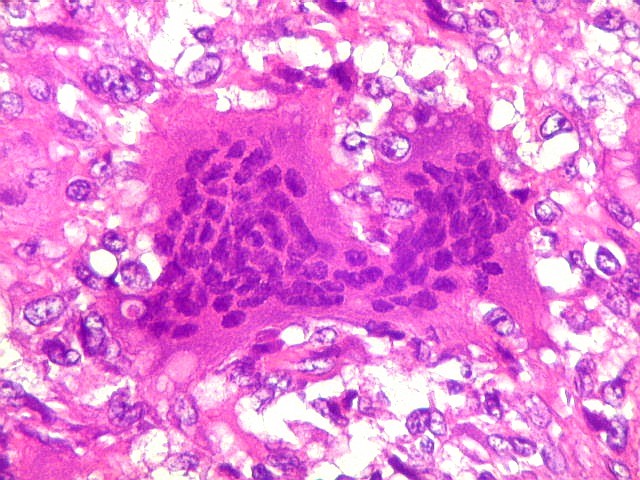
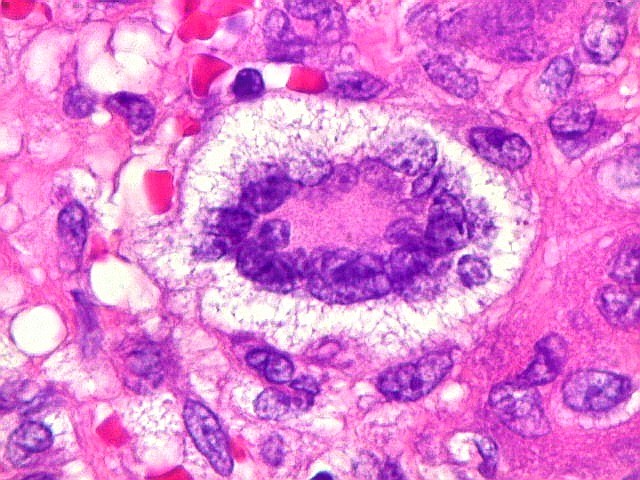
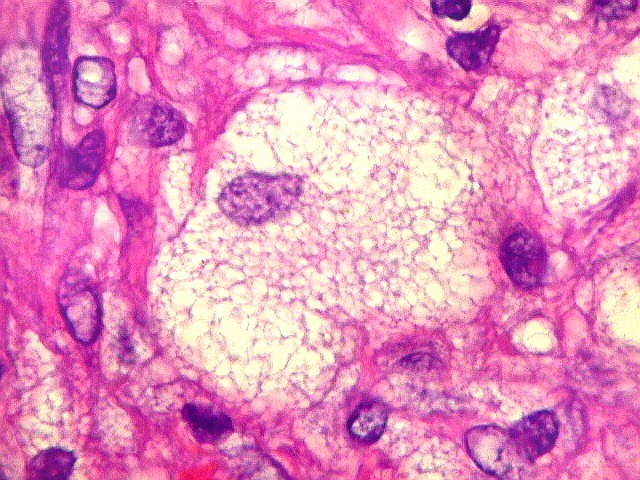
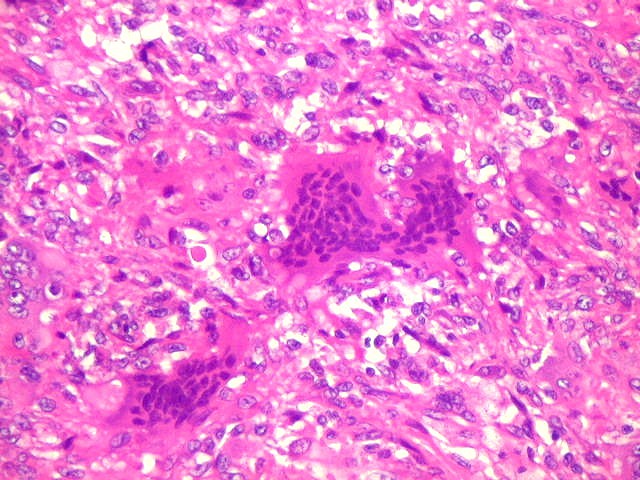
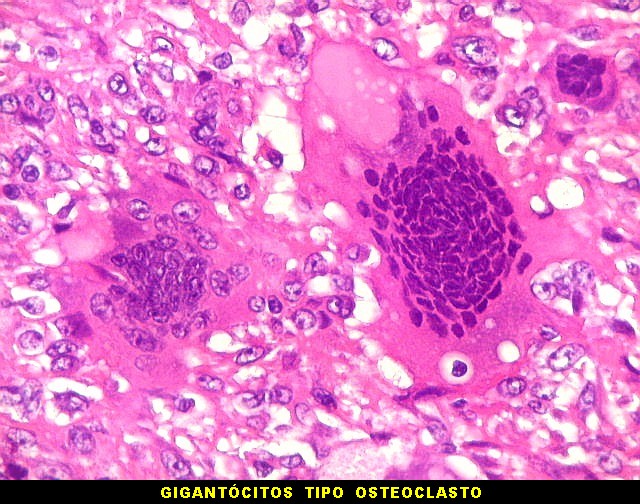
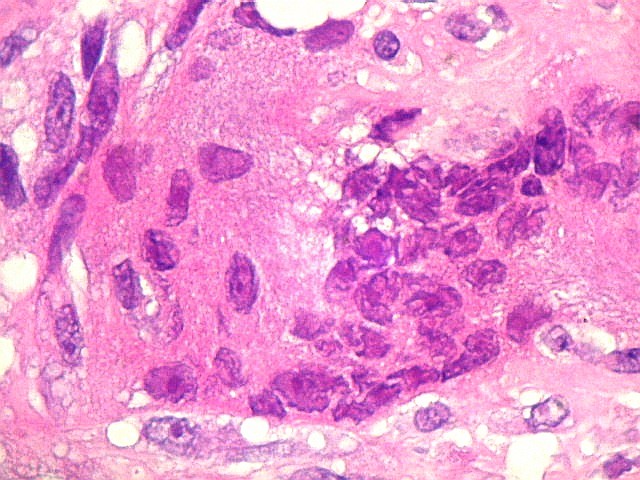
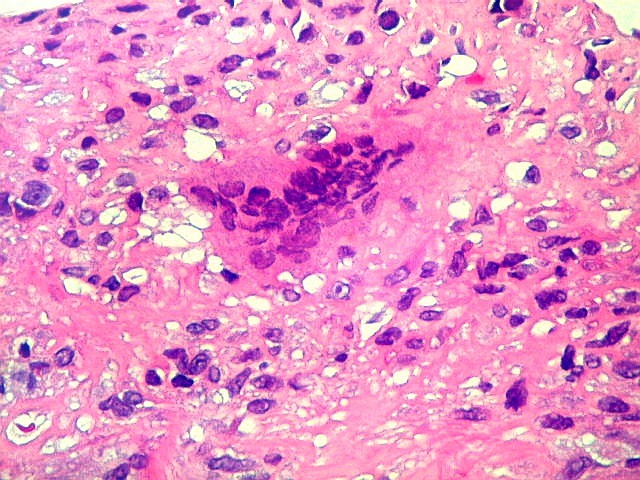
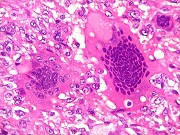
| HE. Lesão composta de células fusiformes estromais semelhantes a fibroblastos e células gigantes multinucleadas, na maioria de padrão osteoclasto | Células gigantes multinucleadas do tipo osteoclasto | Células gigantes multinucleadas do tipo Touton (núcleos em anel, gotículas lipídicas na periferia) |
 |
 |
 |
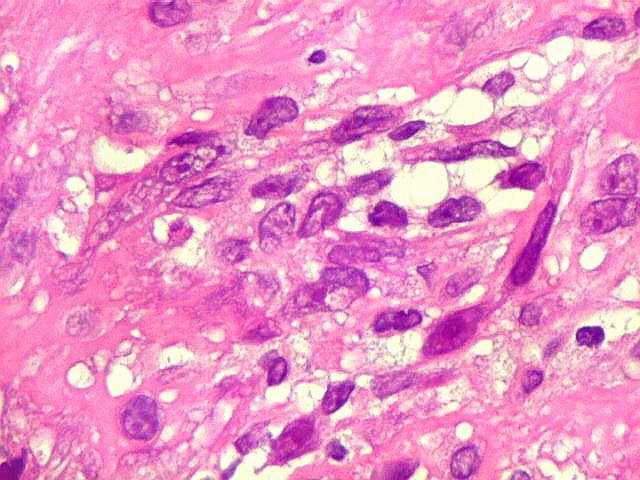
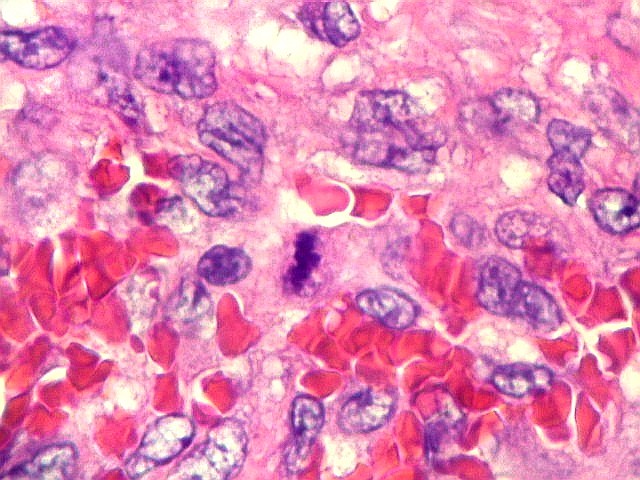
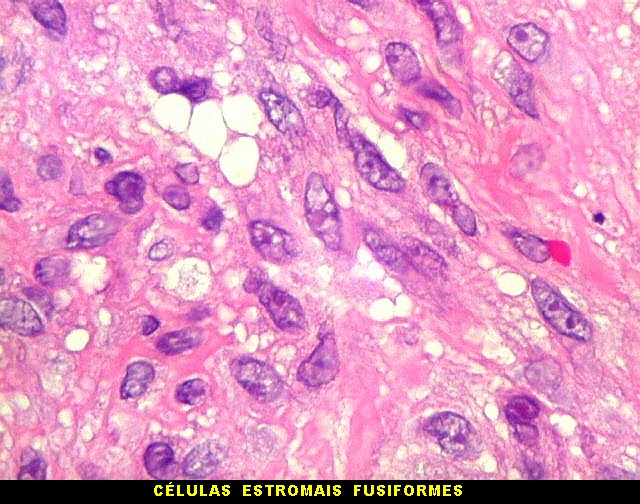
| Células fusiformes estromais semelhantes a fibroblastos (na realidade, miofibroblastos, ver 1A4) | Mitoses típicas esparsas | Macrófagos xantomatosos |
 |
 |
 |
| Infiltração tumoral dos espaços medulares do osso temporal | Metaplasia / neoformação óssea (focos isolados) | Necrose coagulativa e cristais de colesterol |
 |
 |
 |
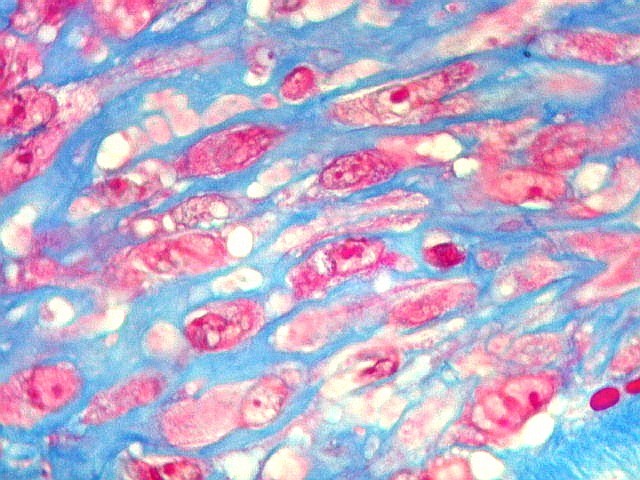
| Masson. Colágeno entre as células fusiformes estromais | Células gigantes multinucleadas | Reticulina. Abundantes fibras reticulínicas permeando entre as células estromais e gigantes |
 |
 |
 |
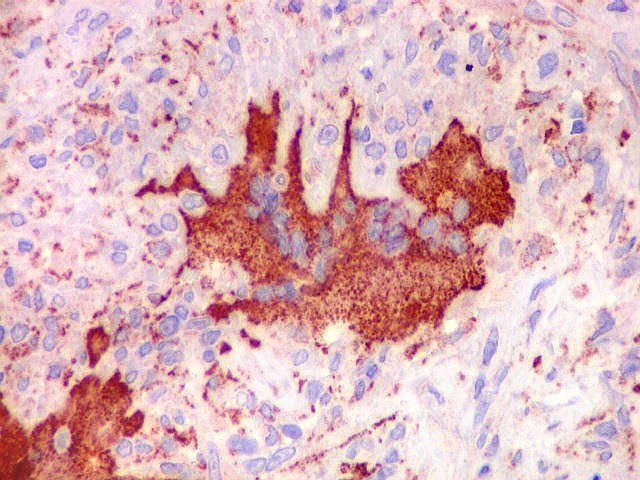
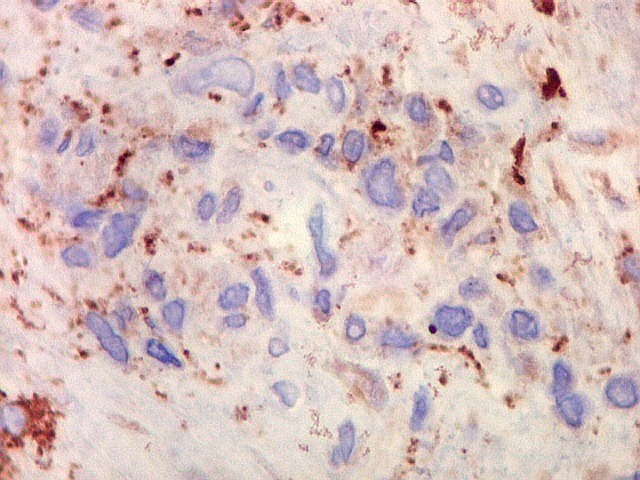
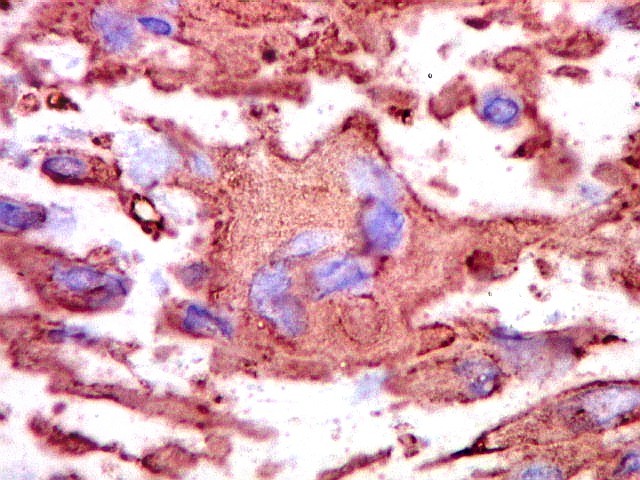
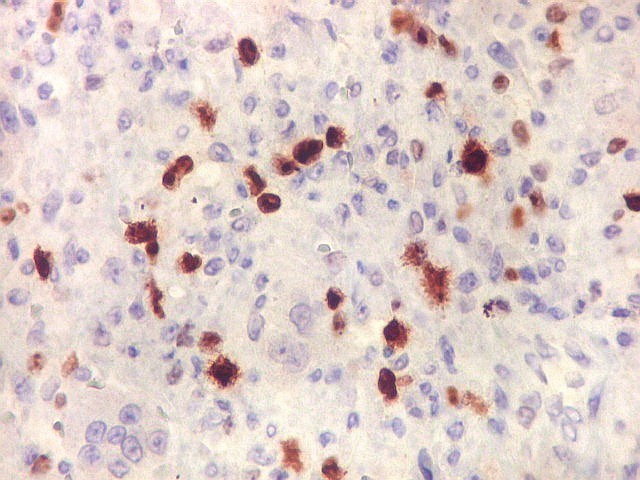
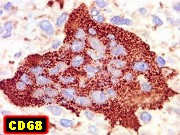
| CD68. Marcador de macrófagos, positivo nas células gigantes. | Negativo nas células fusiformes estromais | VIM. Positiva no citoplasma nos dois tipos celulares |
 |
 |
 |
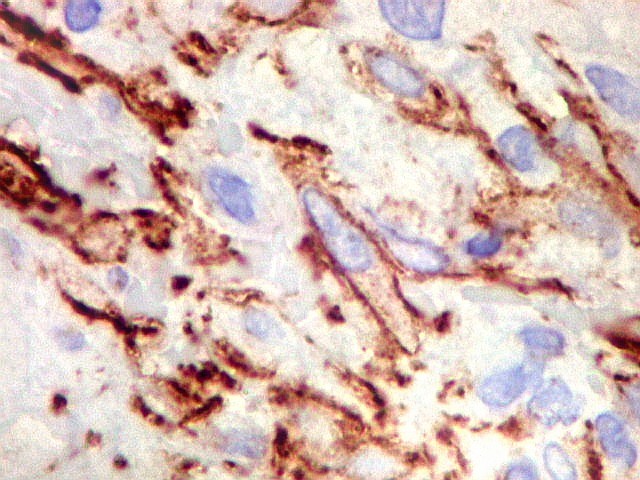
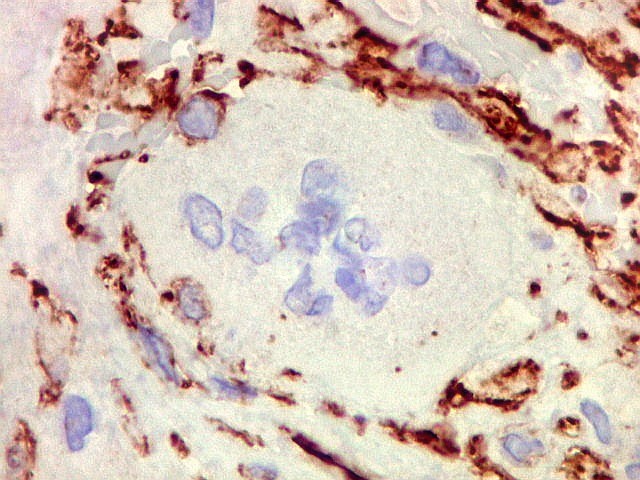
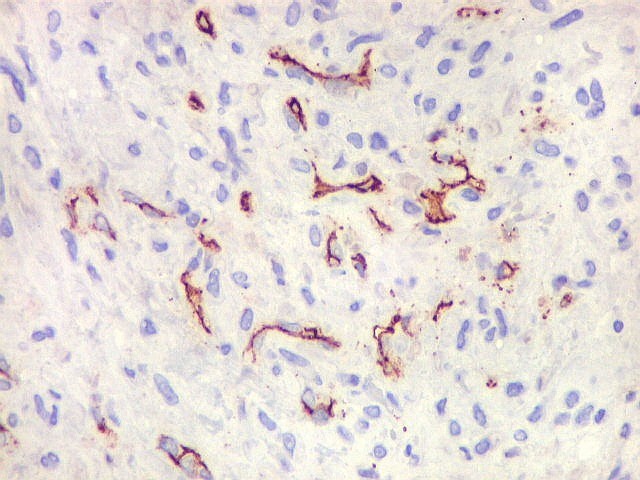
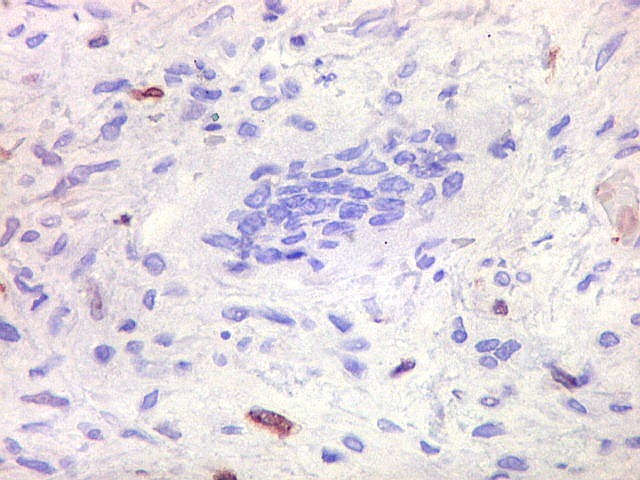
| 1A4. Anticorpo para actina de músculo liso, positivo no citoplasma das células fusiformes estromais, indica natureza miofibroblástica destas | Negativo nas células gigantes multinucleadas | CD34. Positivo nos capilares, negativo no tumor |
 |
 |
 |
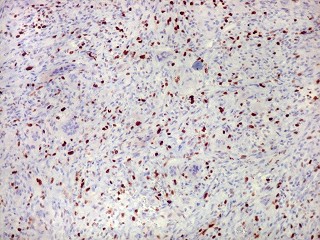
| Ki-67. Positividade em cerca de 20% dos núcleos, | restrita às células fusiformes estromais, indicando que são o elemento proliferante da lesão | Sempre negativo nas células gigantes multinucleadas |
 |
 |
 |
|
|
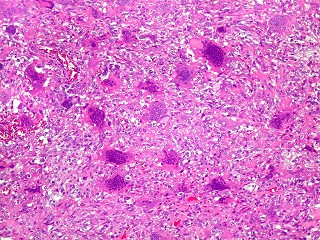
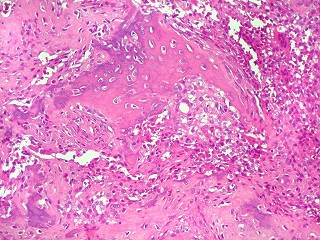
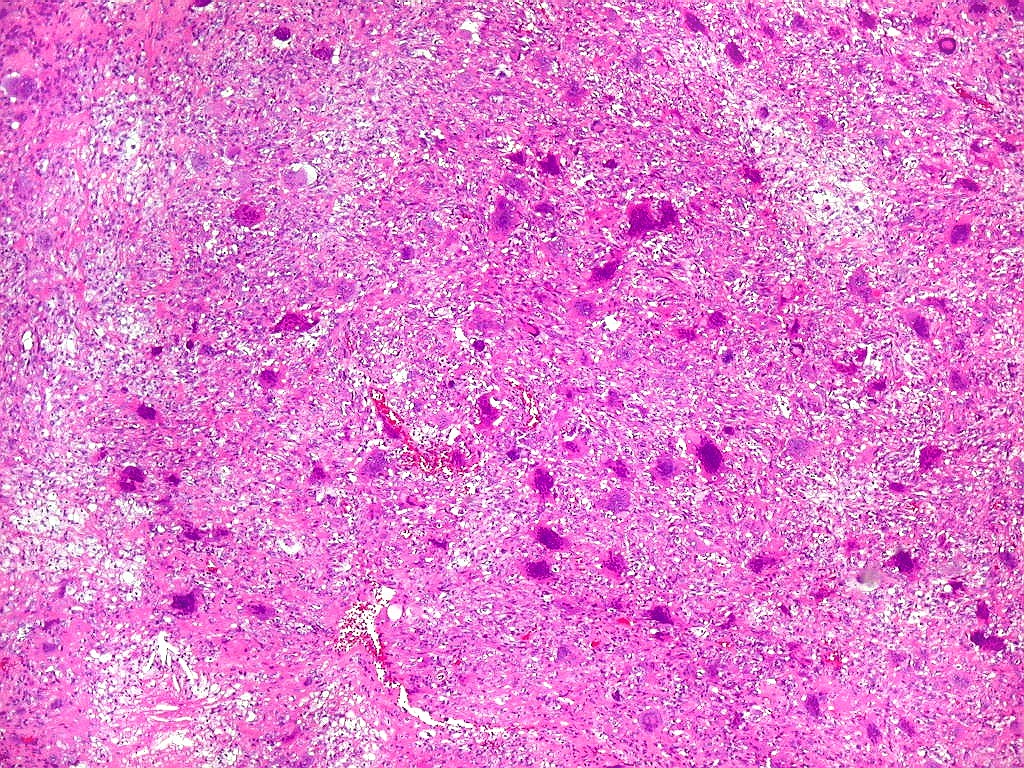
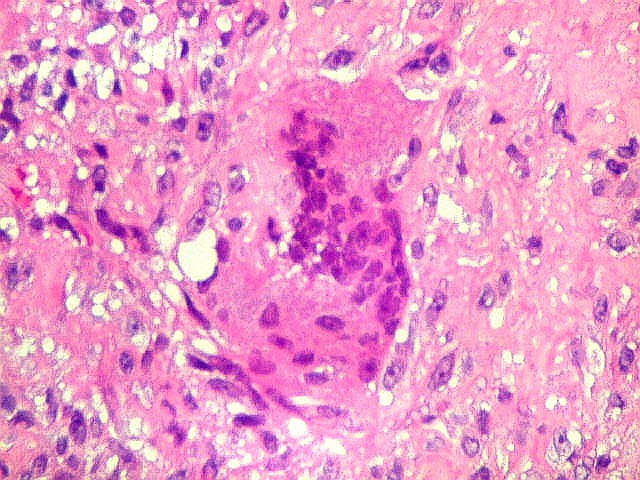
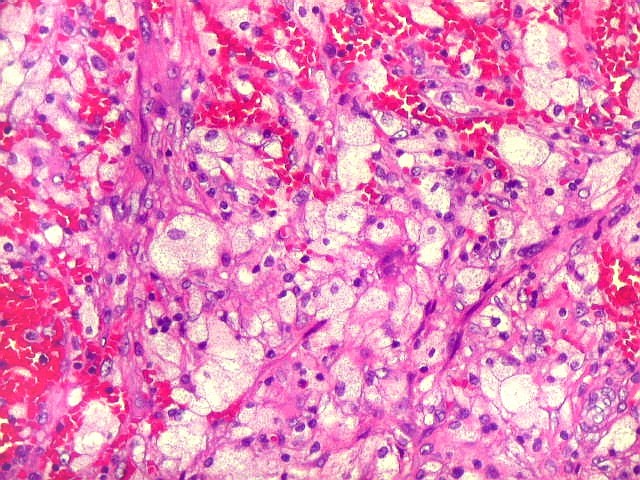
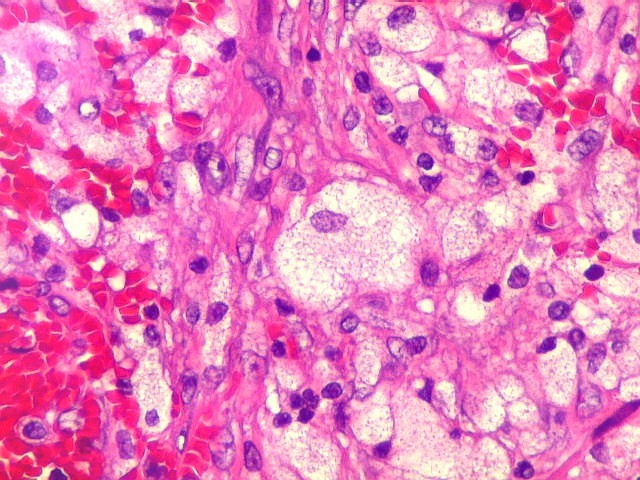
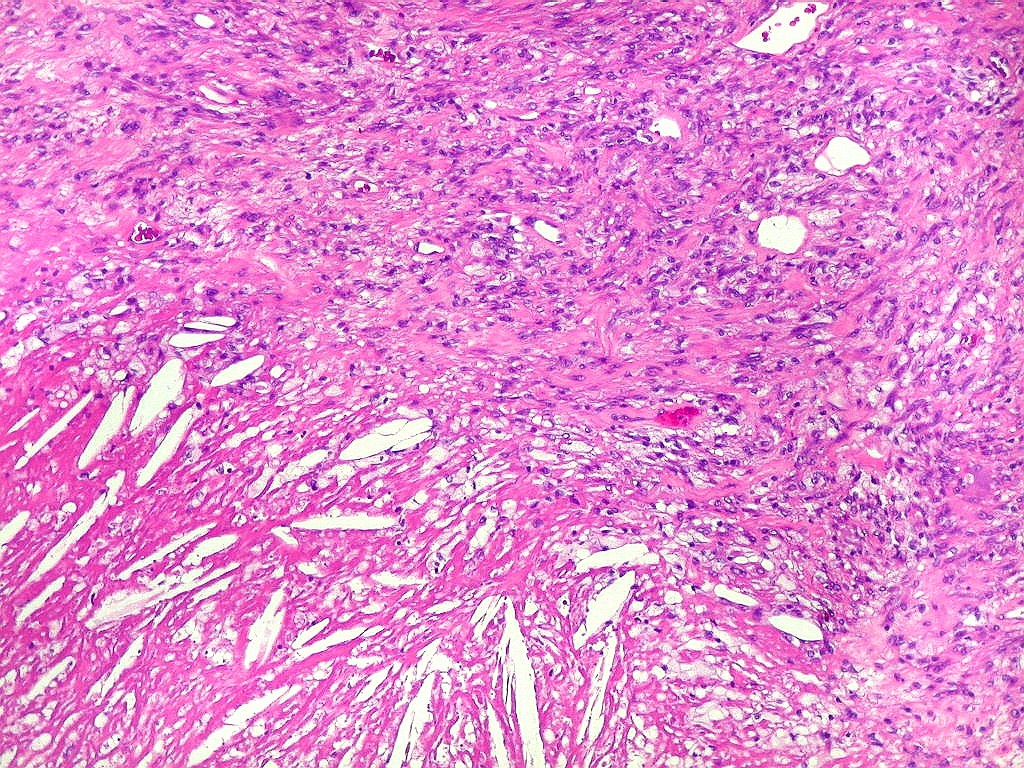
| Aspecto geral da lesão. Tecido de aspecto neoplásico, sólido, com dois componentes celulares distintos. A maior parte é formada por células fusiformes vagamente arranjadas em feixes, em meio às quais distribuem-se aleatoriamente células gigantes multinucleadas de padrão osteoclástico. Há grande regularidade nas diversas áreas, mas observam-se em outros campos regiões ricas em macrófagos xantomatosos, e áreas de necrose com cristais de colesterol. Os aspectos morfológicos são virtualmente indistinguíveis do tumor de células gigantes, cabendo o diagnóstico diferencial à idade e localização (ver texto). Para exemplo de TCG, clique. |
 |
 |
 |
 |
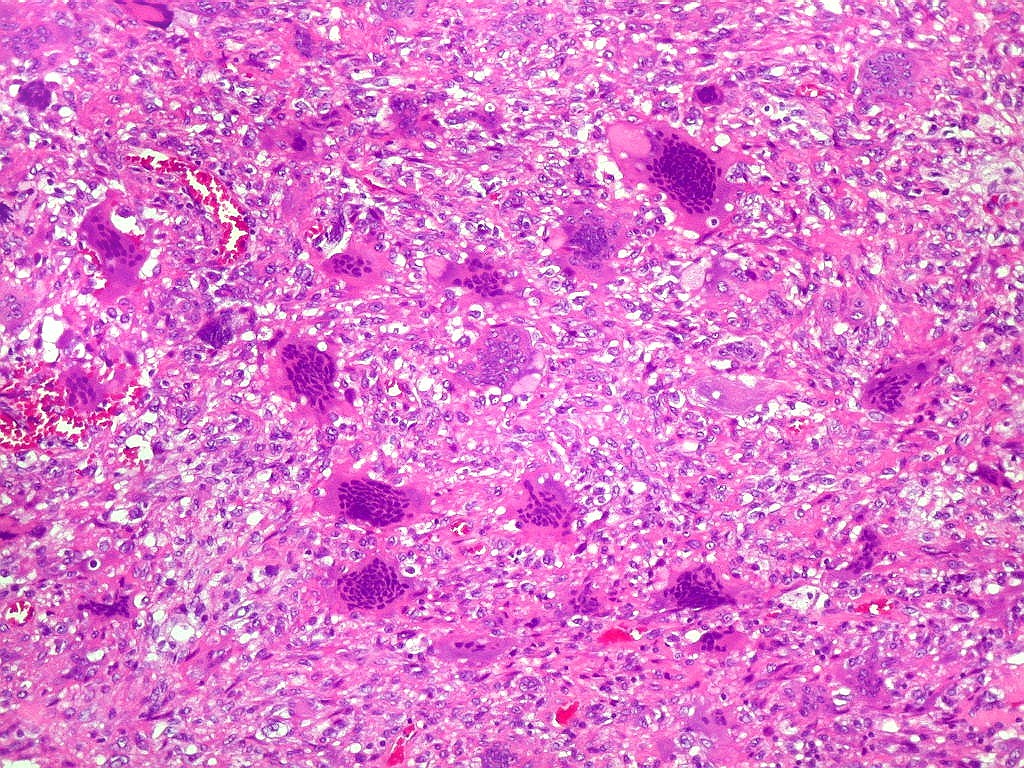
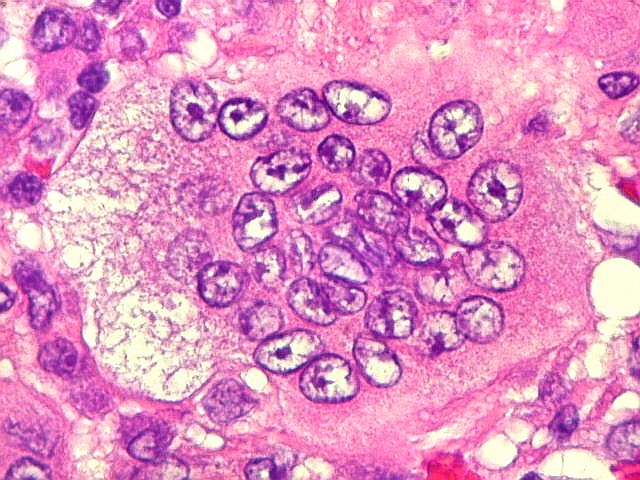
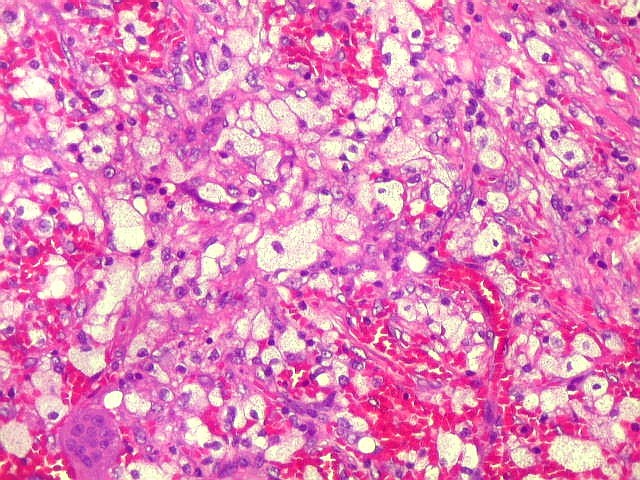
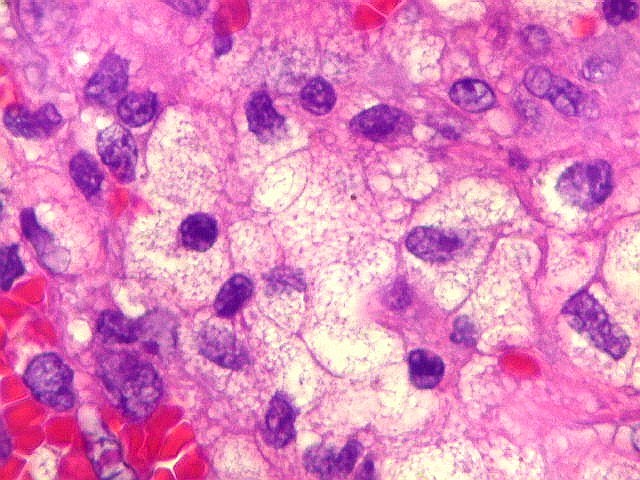
| Células gigantes multinucleadas. Eram, na grande maioria, de padrão osteoclasto, com núcleos hipercromáticos, regulares, tendendo a ocupar a parte mais interna do abundante citoplasma róseo. Em alguns, os núcleos continham nucléolos proeminentes. | |
 |
 |
 |
 |
 |
 |
 |
 |
 |
 |
 |
 |
 |
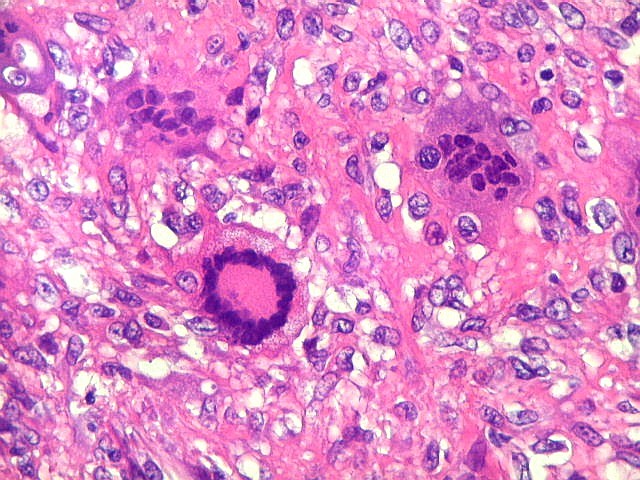 |
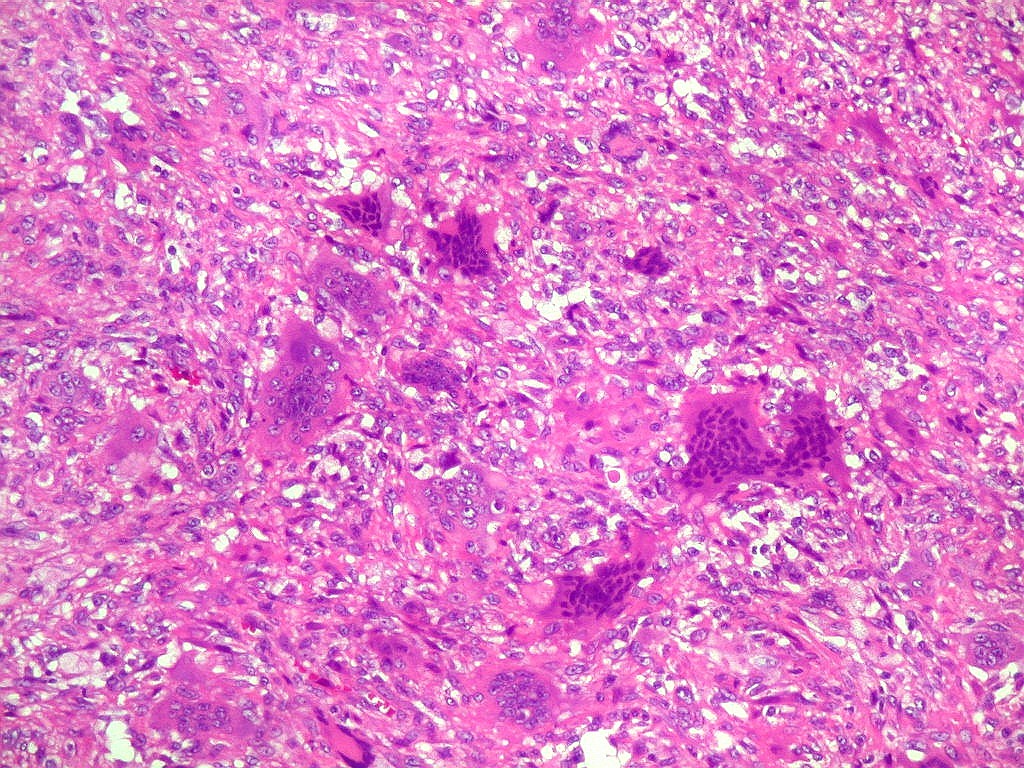
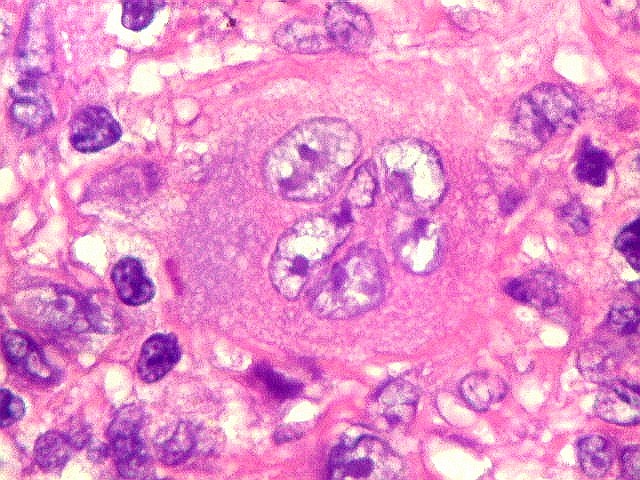
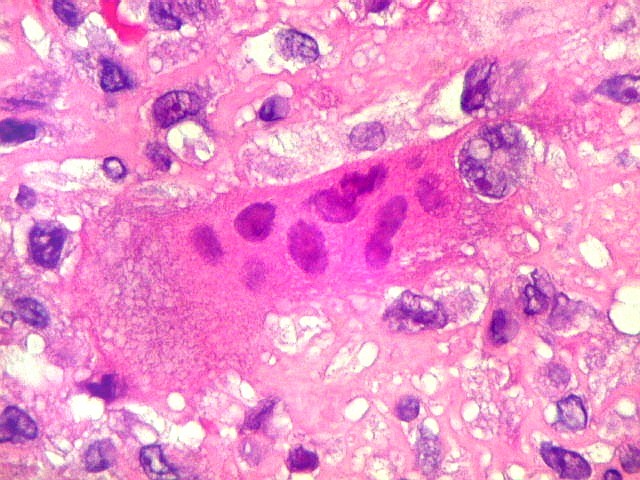
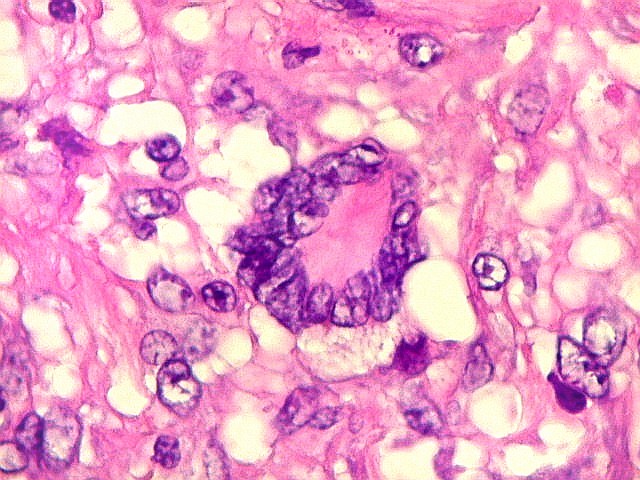
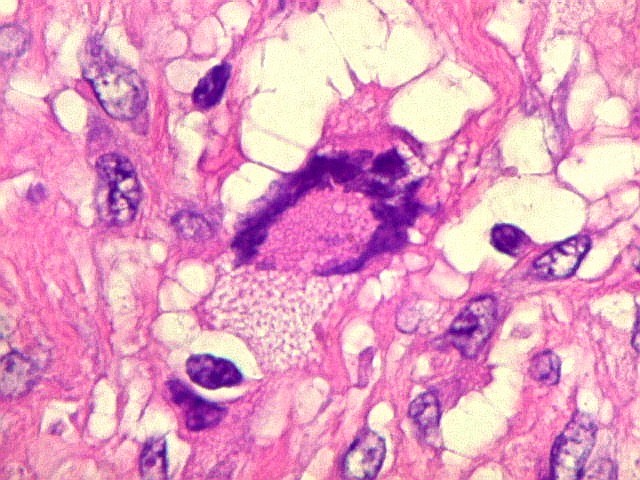
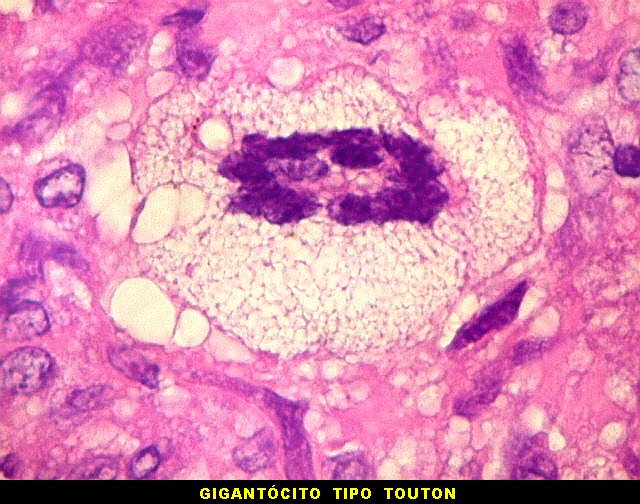
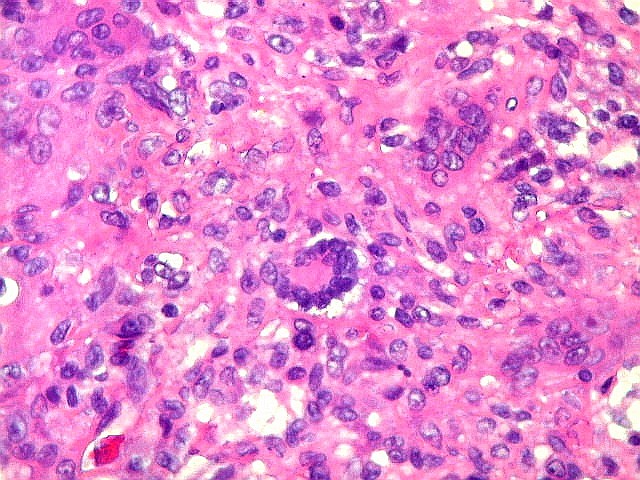
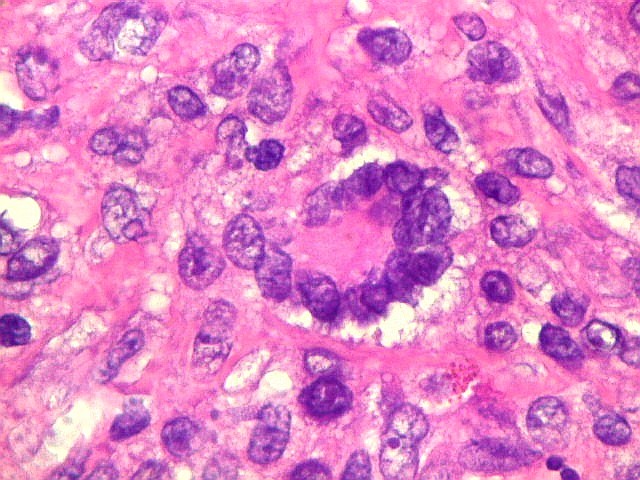
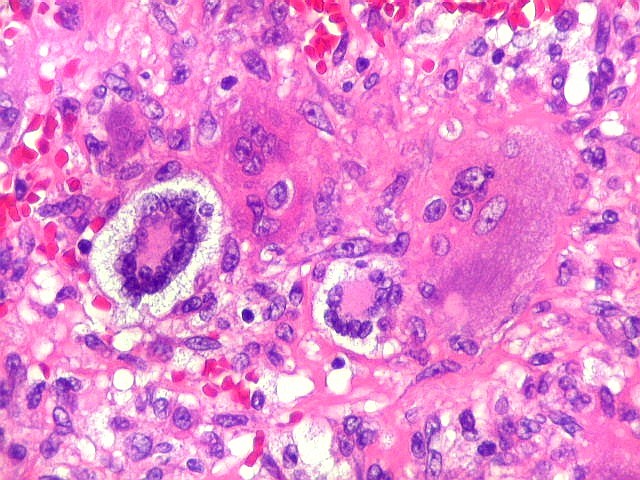
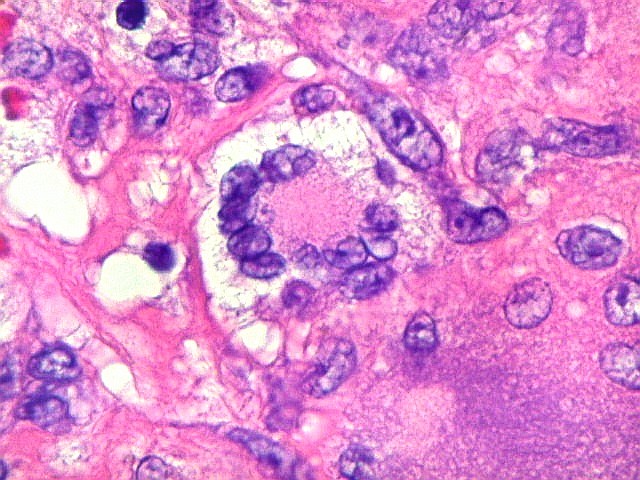
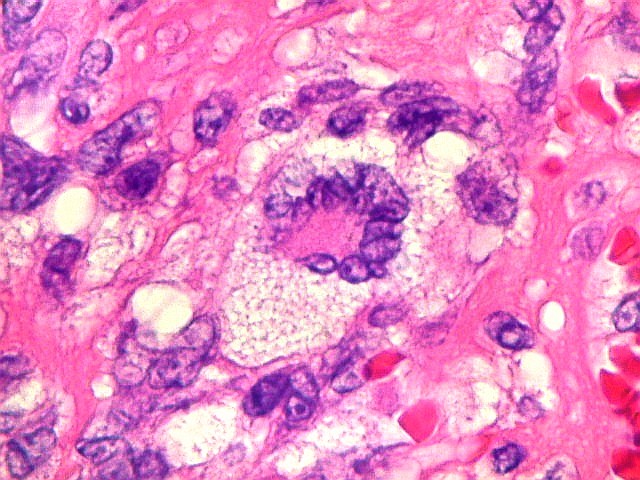
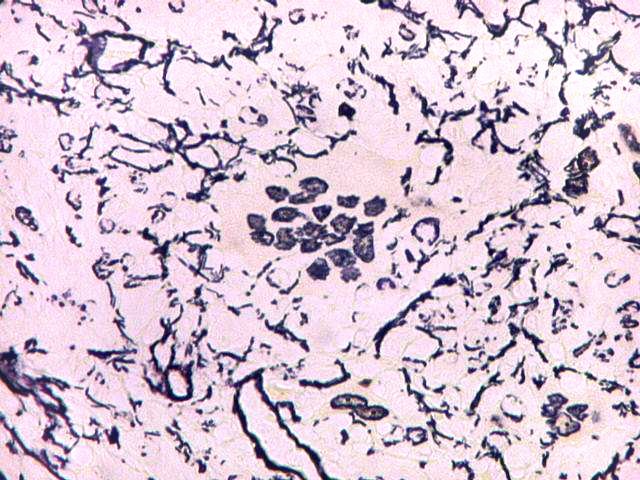
| Células gigantes tipo 'Touton'. Células gigantes multinucleadas cujos núcleos dispõem-se como anel em torno de um centro róseo. Freqüentemente há também gotículas lipídicas na periferia, entre os núcleos e a membrana celular. Células de Touton são vistas em lesões ricas em lípides, mas também ocorrem em tumor de células gigantes do osso. Para exemplo, clique. | |
 |
 |
 |
 |
 |
 |
 |
 |
 |
 |
| Para mais sobre gigantócitos de Touton. | |
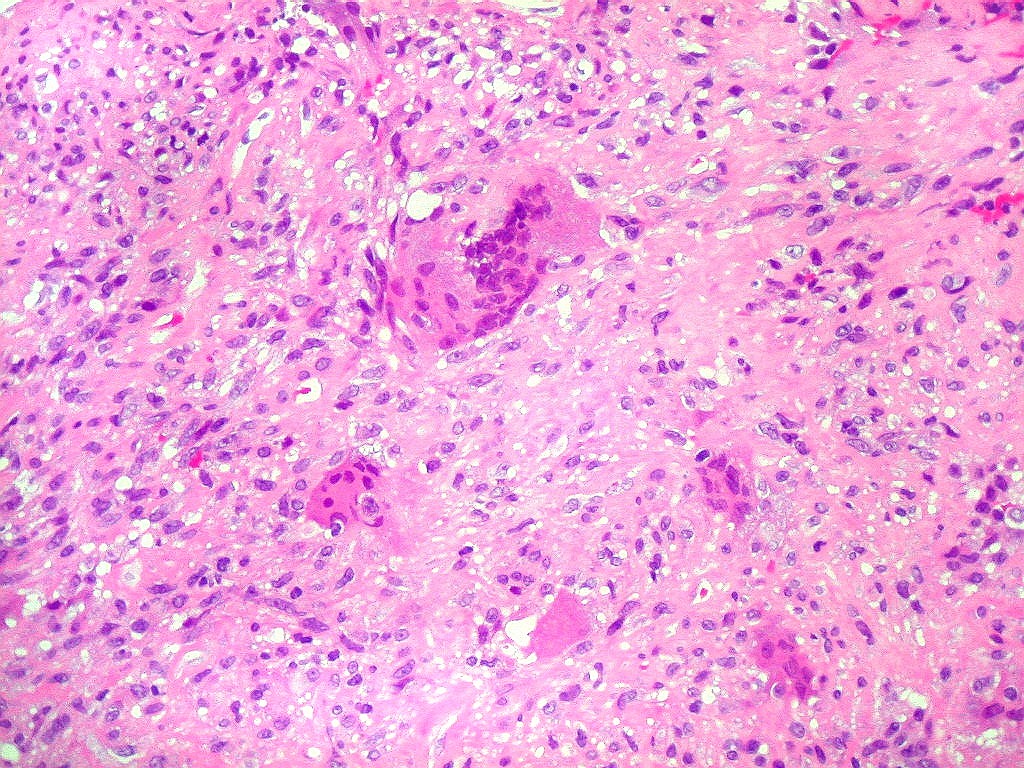
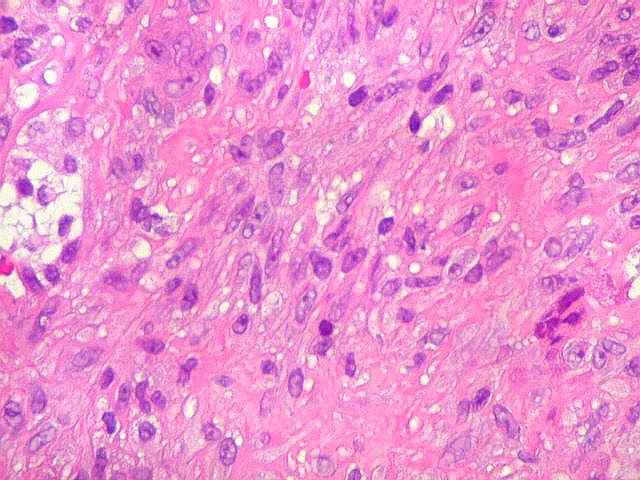
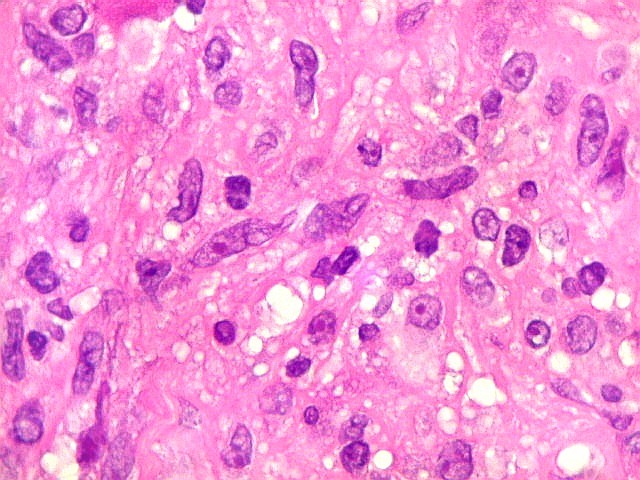
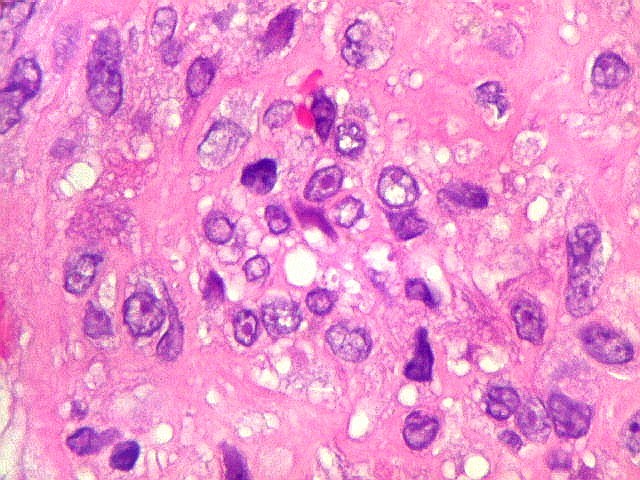
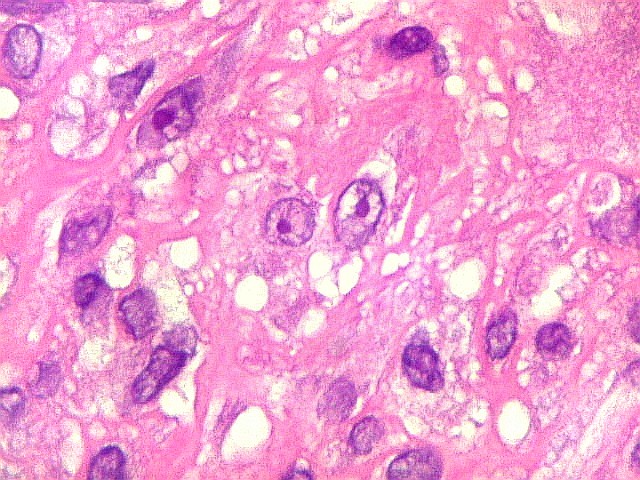
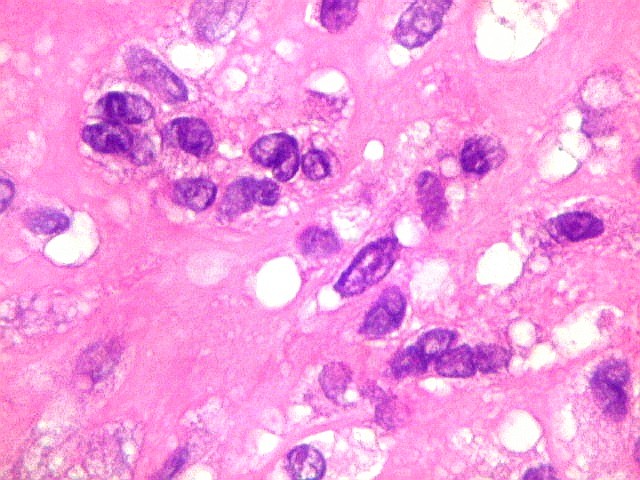
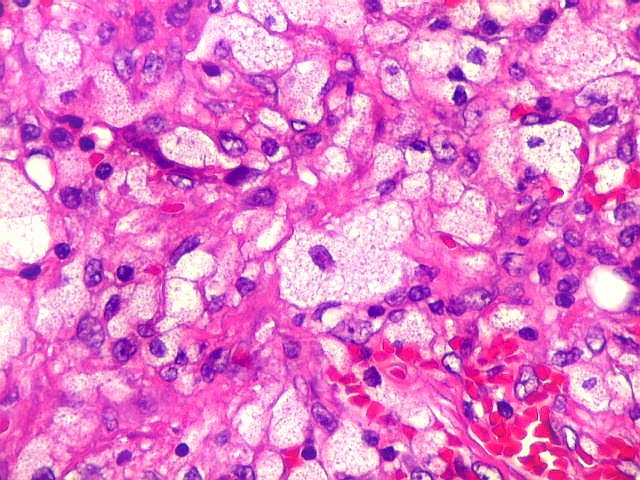
| Células estromais fusiformes. Células estromais fusiformes constituem o elemento propriamente proliferativo da lesão, como documentado com Ki67, que é positivo apenas nelas. Os gigantócitos são sempre negativos. A linhagem mais provável das células é miofibroblástica, pois reagem positivamente para 1A4, um anticorpo que reconhece actina de músculo liso. | |
 |
 |
 |
 |
 |
 |
 |
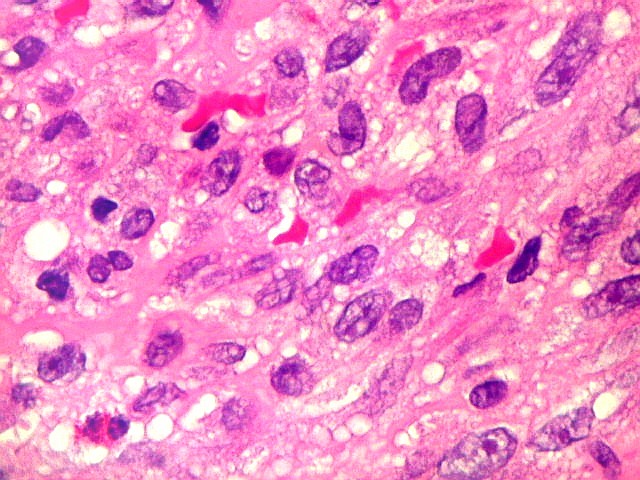 |
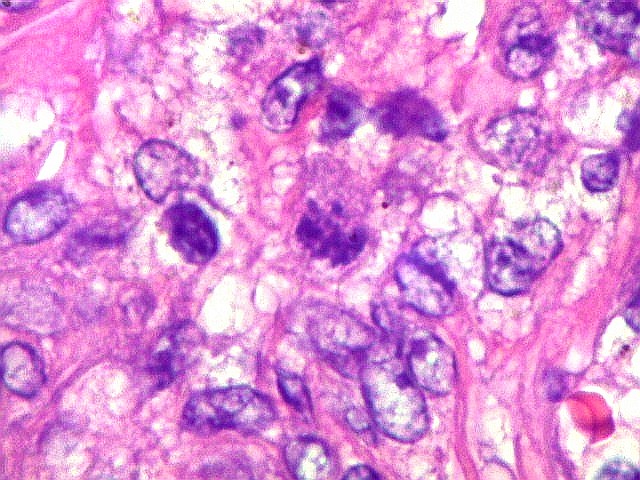
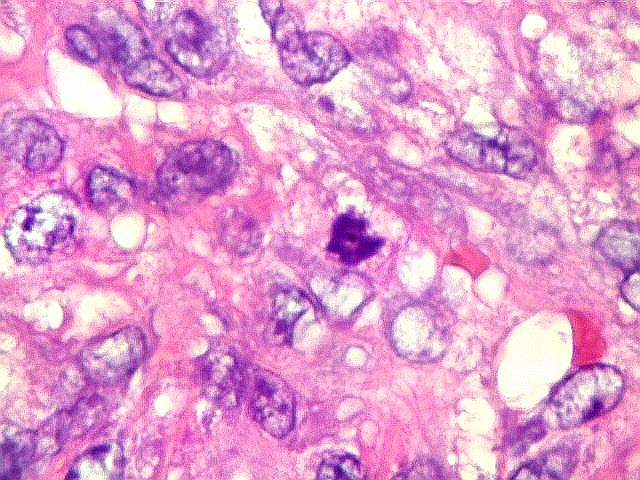
| Mitoses. Poucas mitoses, todas típicas, foram encontradas apenas nas células estromais, nunca nos gigantócitos. | |
 |
 |
 |
 |
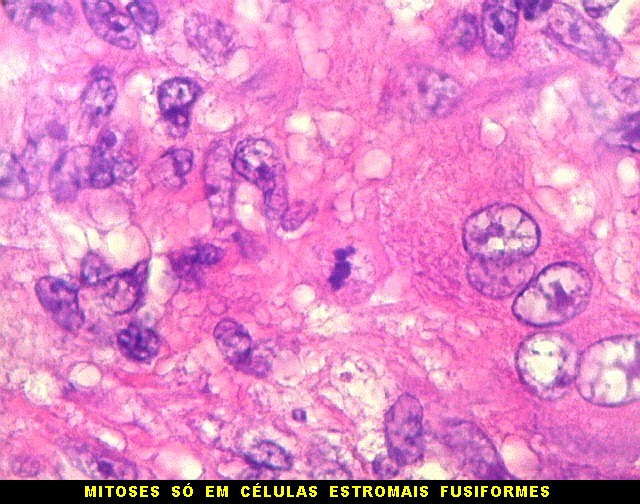 |
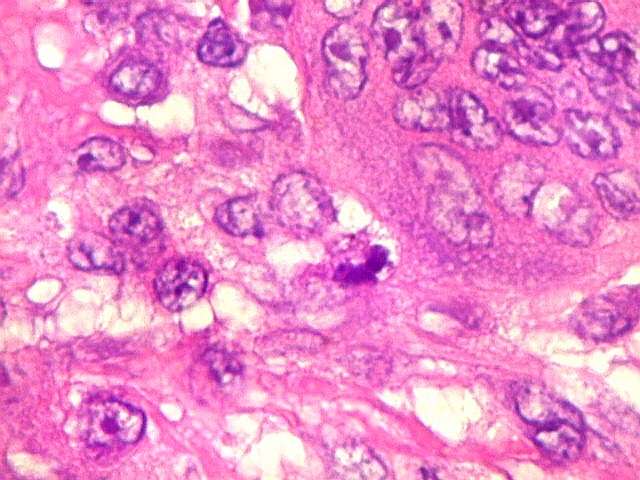 |
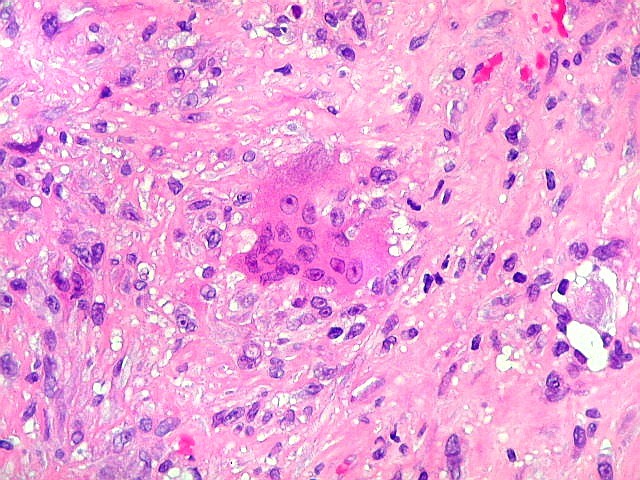
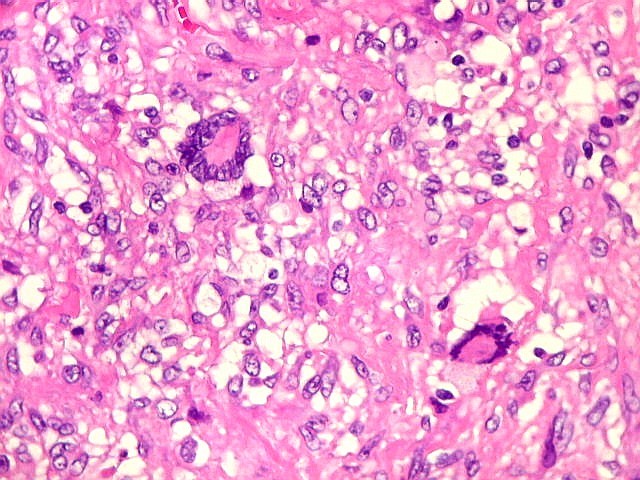
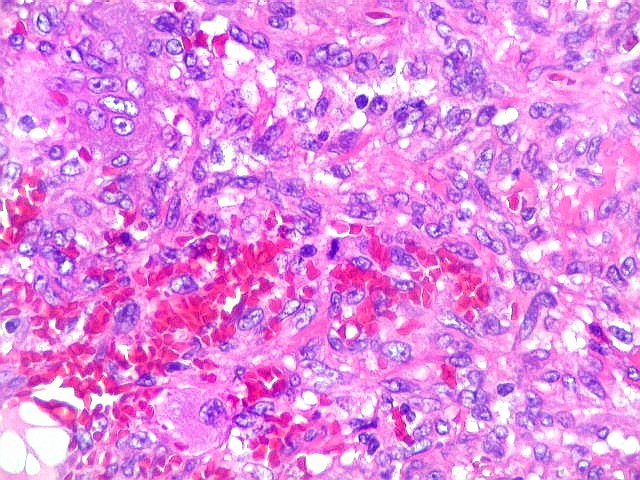
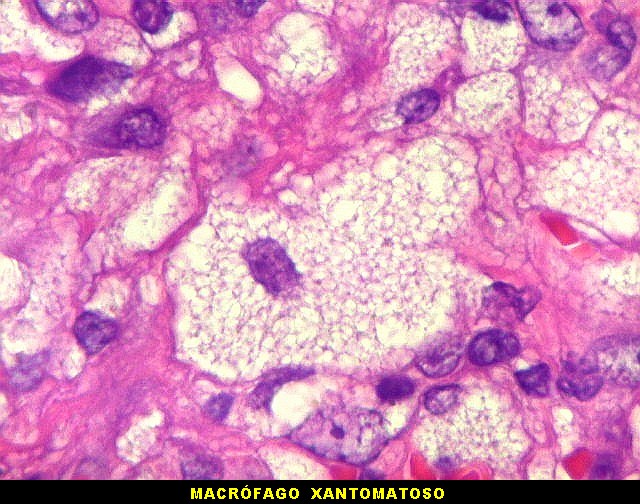
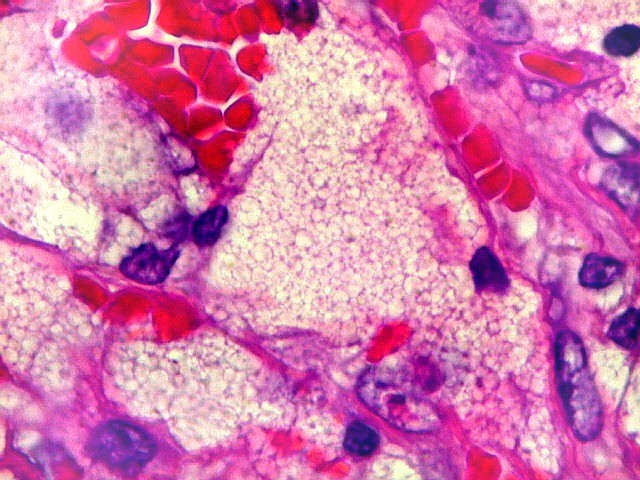
| Macrófagos xantomatosos. Observados em certas áreas, sugerem riqueza em lípides na lesão. |
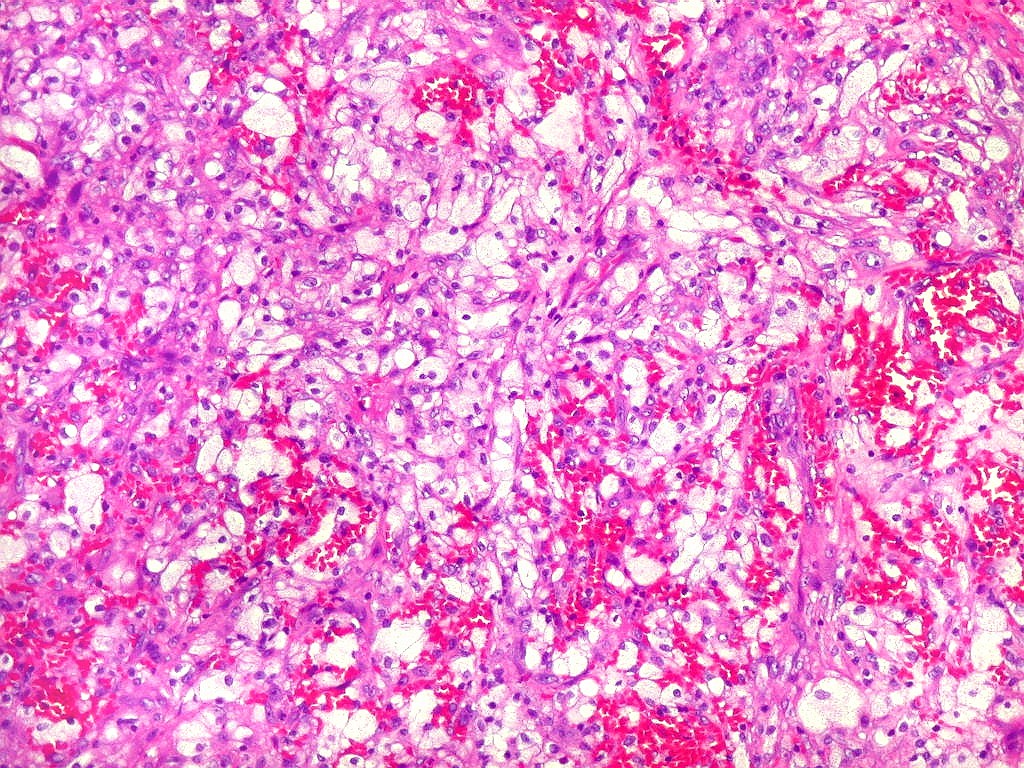 |
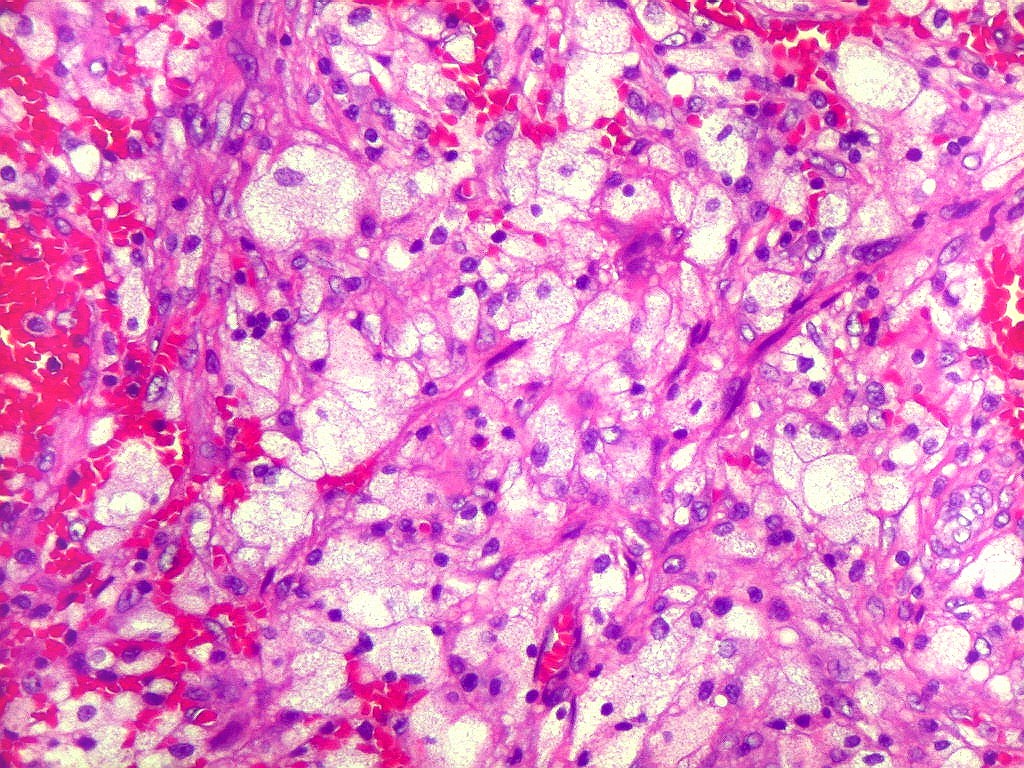 |
 |
 |
 |
 |
 |
 |
 |
 |
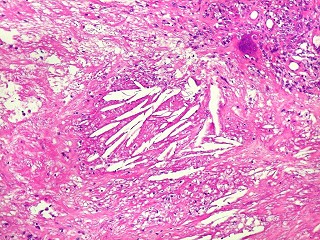
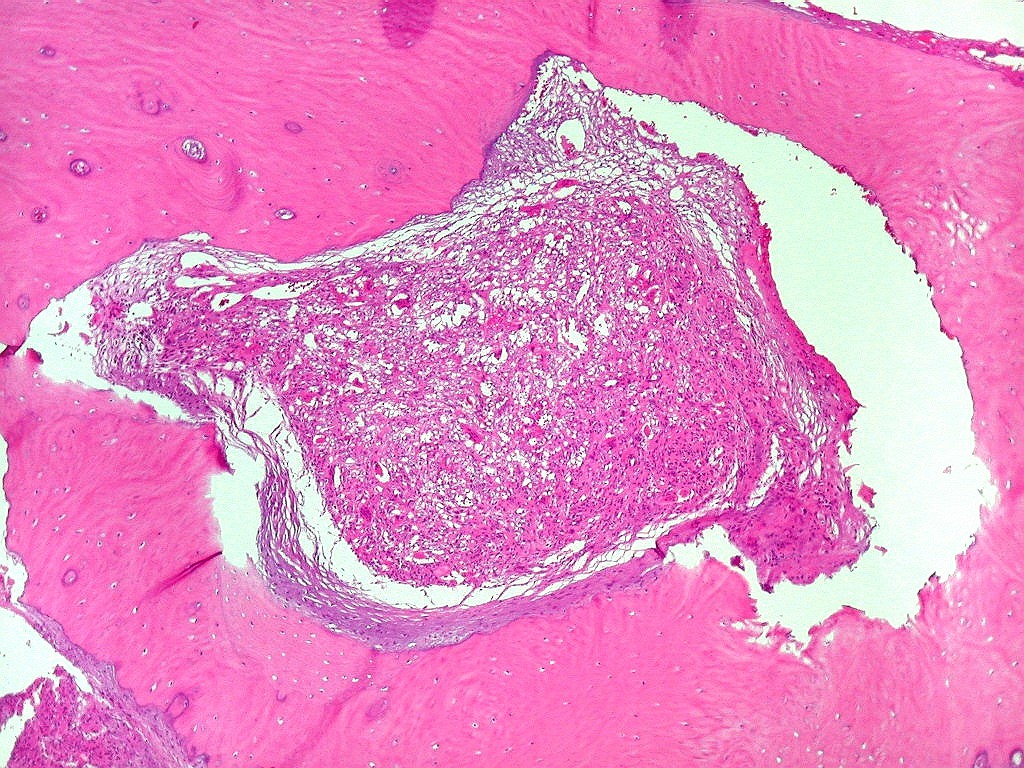
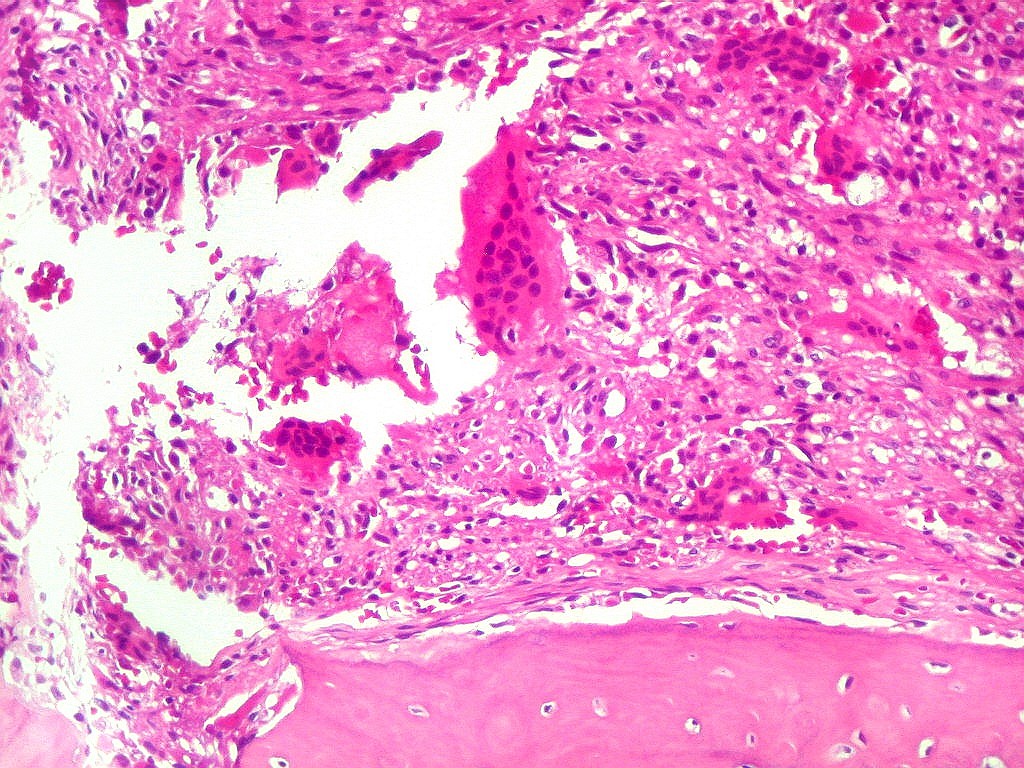
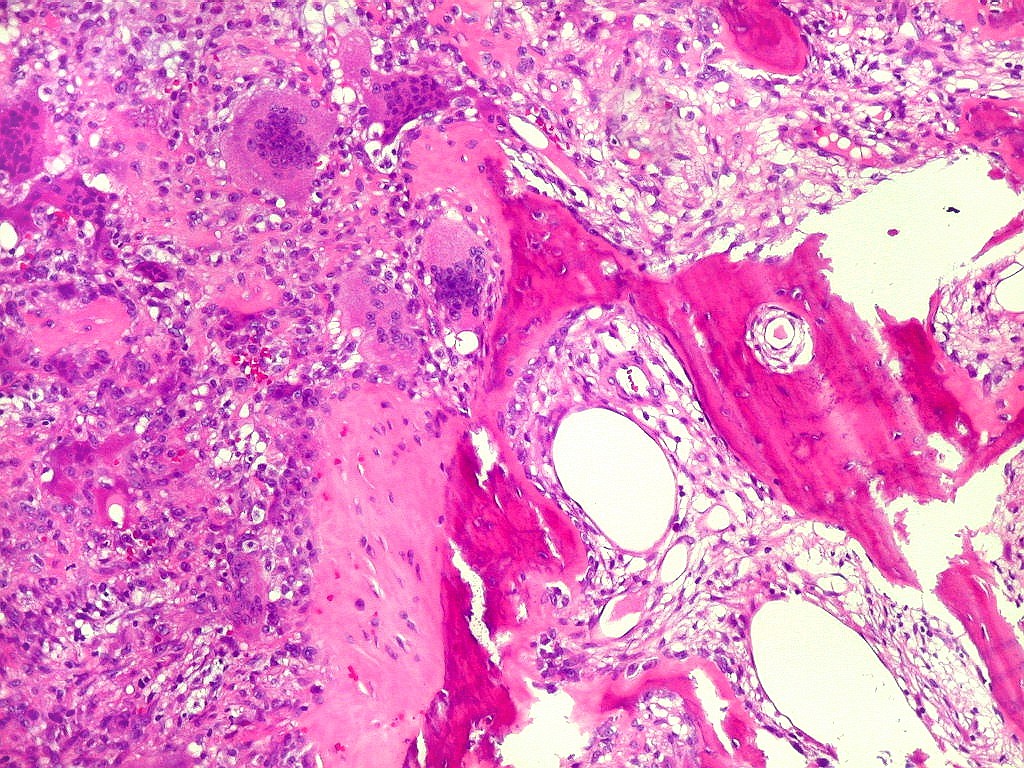
| Infiltração óssea. Alguns fragmentos ósseos mostravam tecido neoplásico penetrando nos espaços medulares. |
 |
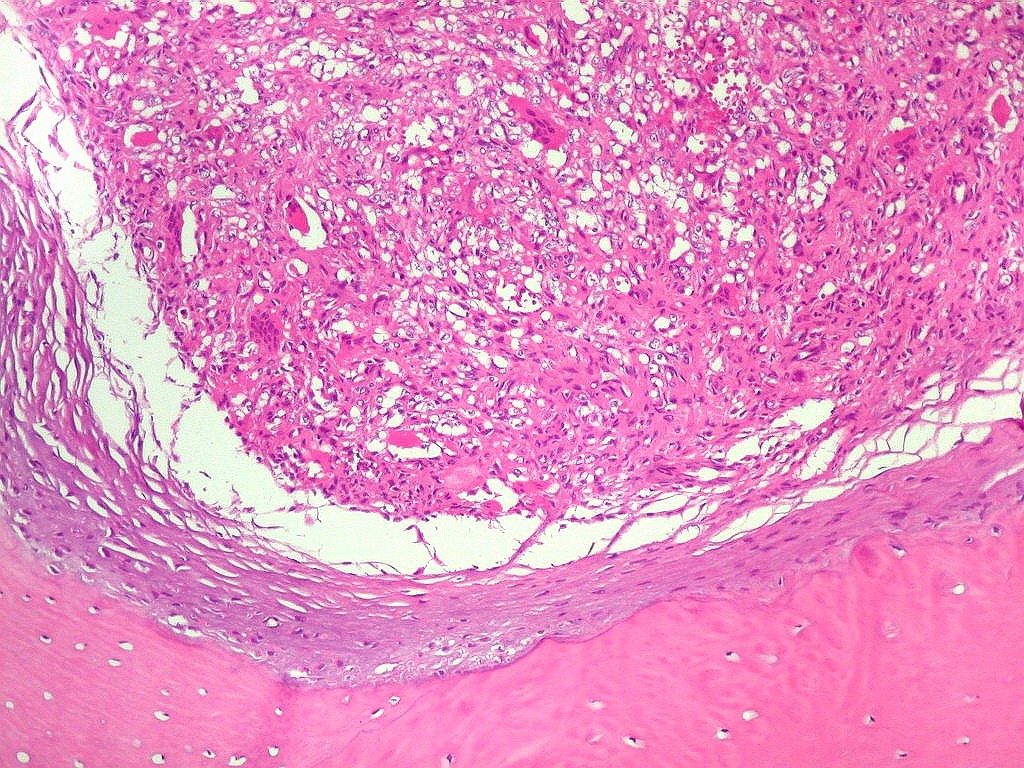 |
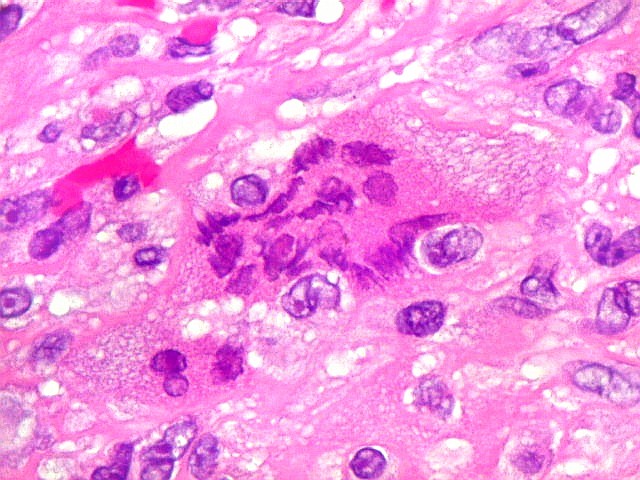
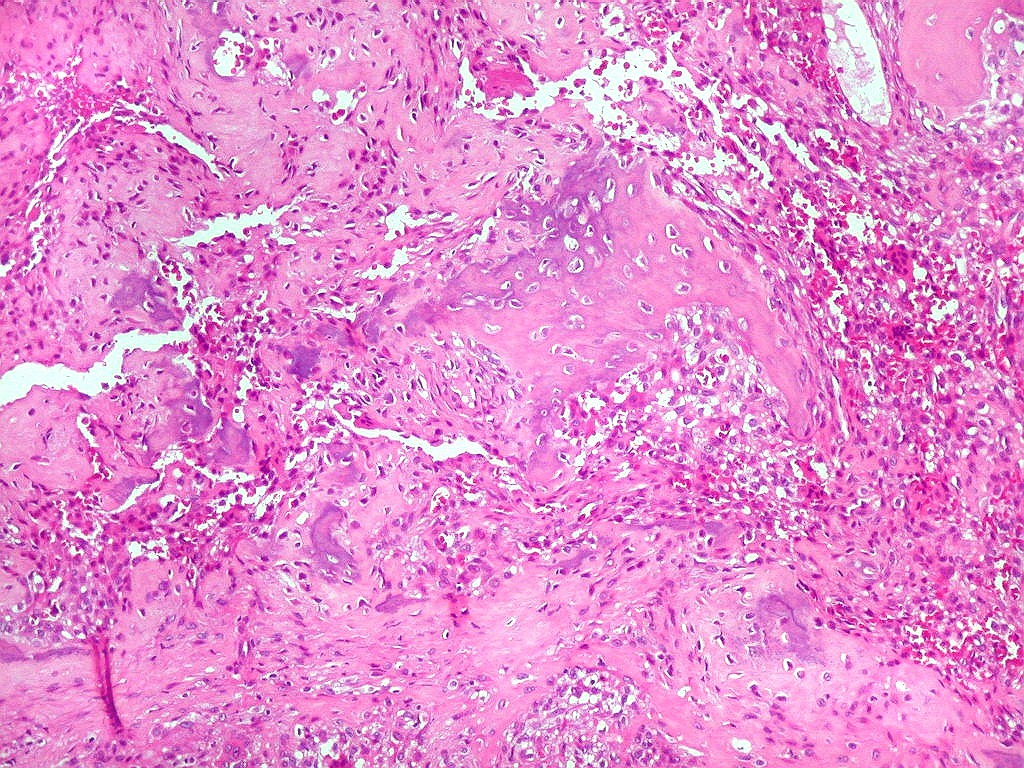
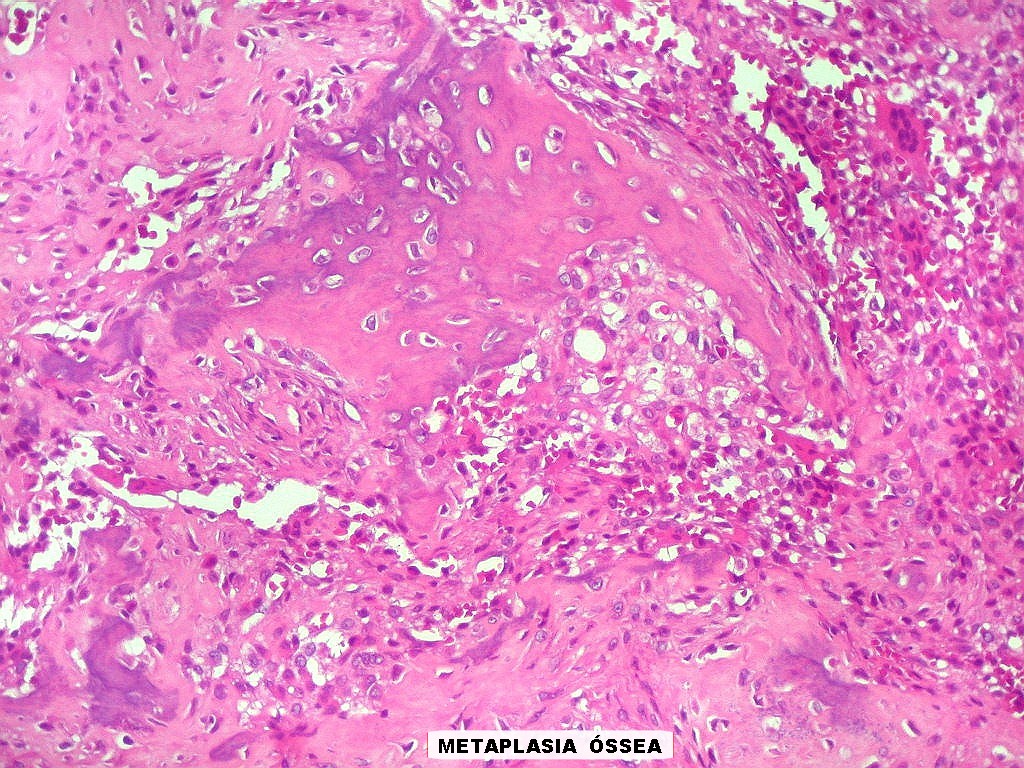
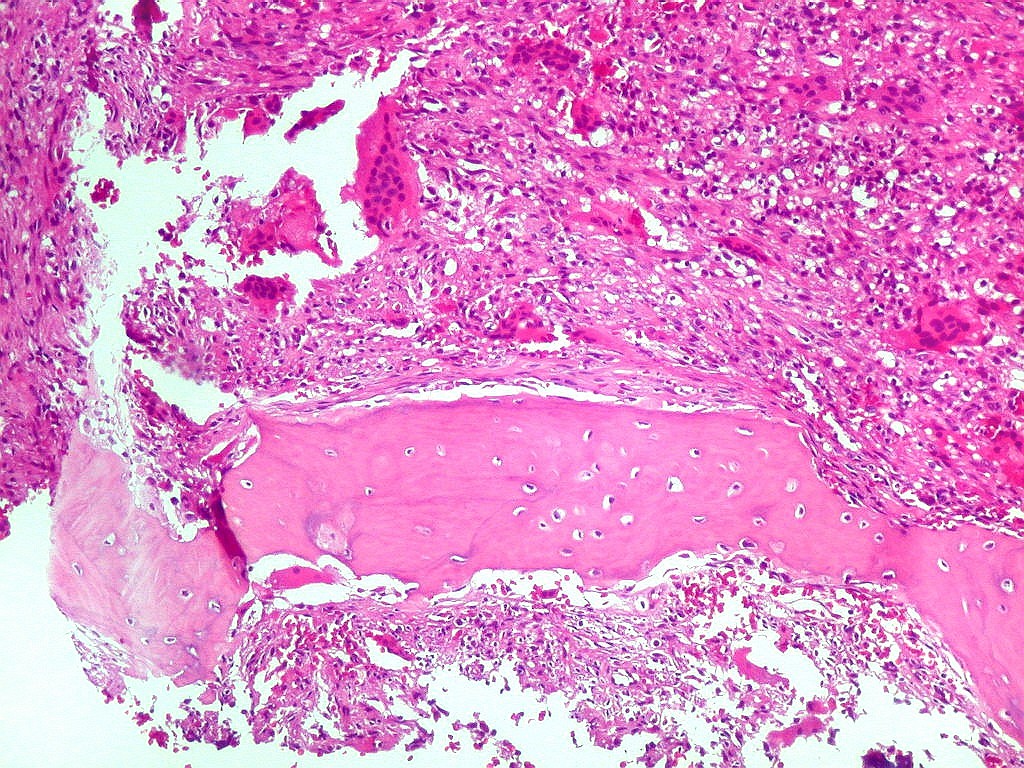
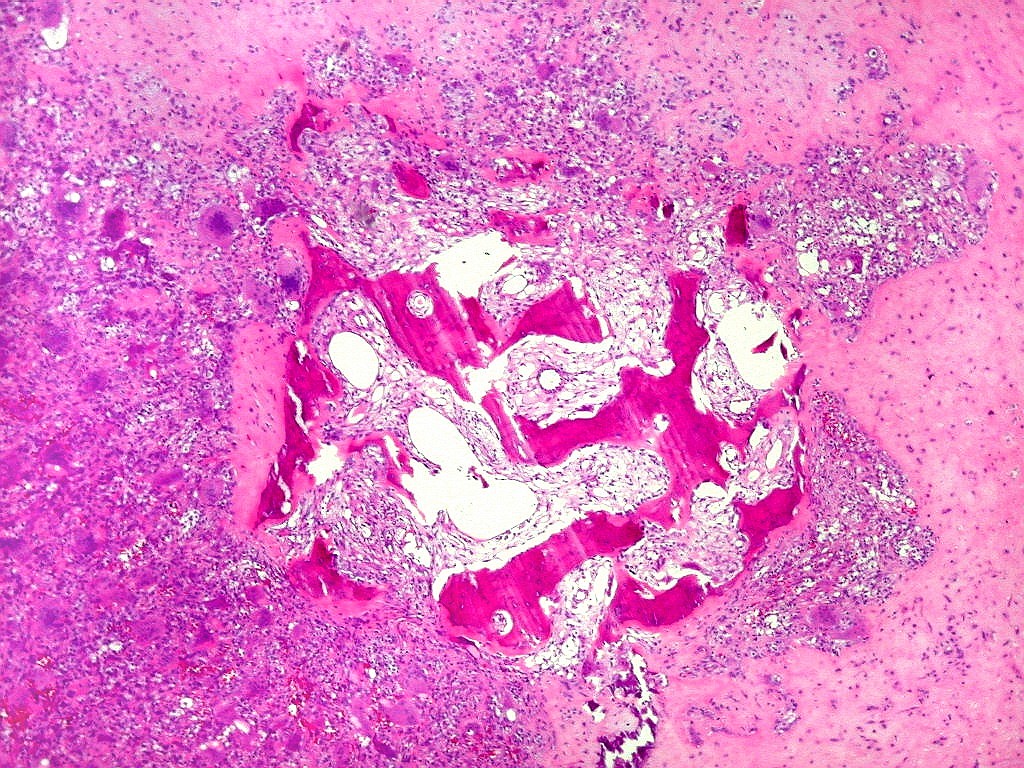
| Metaplasia óssea. Em alguns focos no tumor, observava-se deposição de osso novo (trabéculas ósseas neoformadas). |
 |
 |
 |
 |
 |
 |
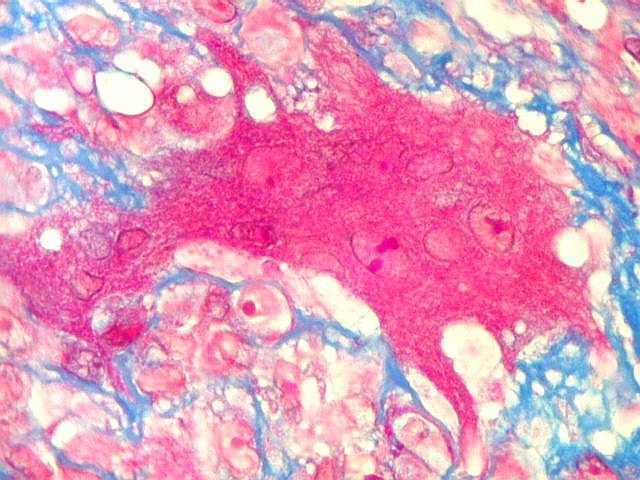
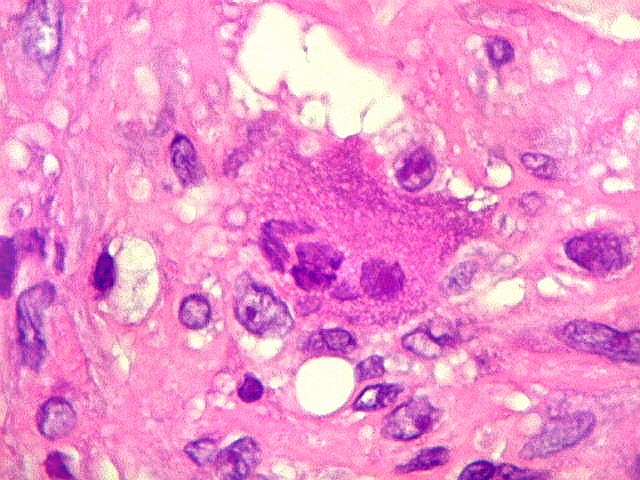
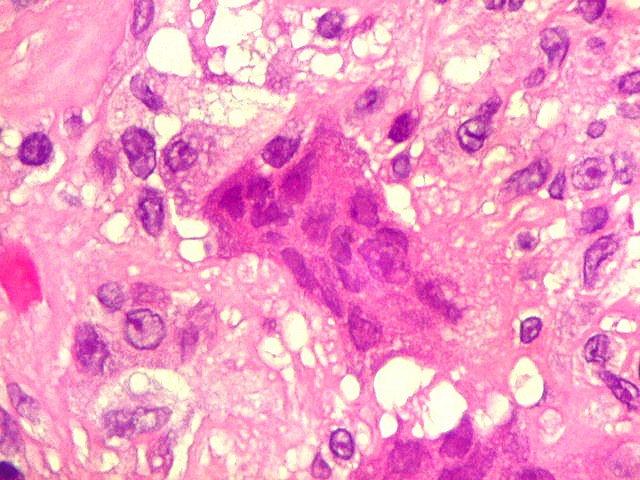
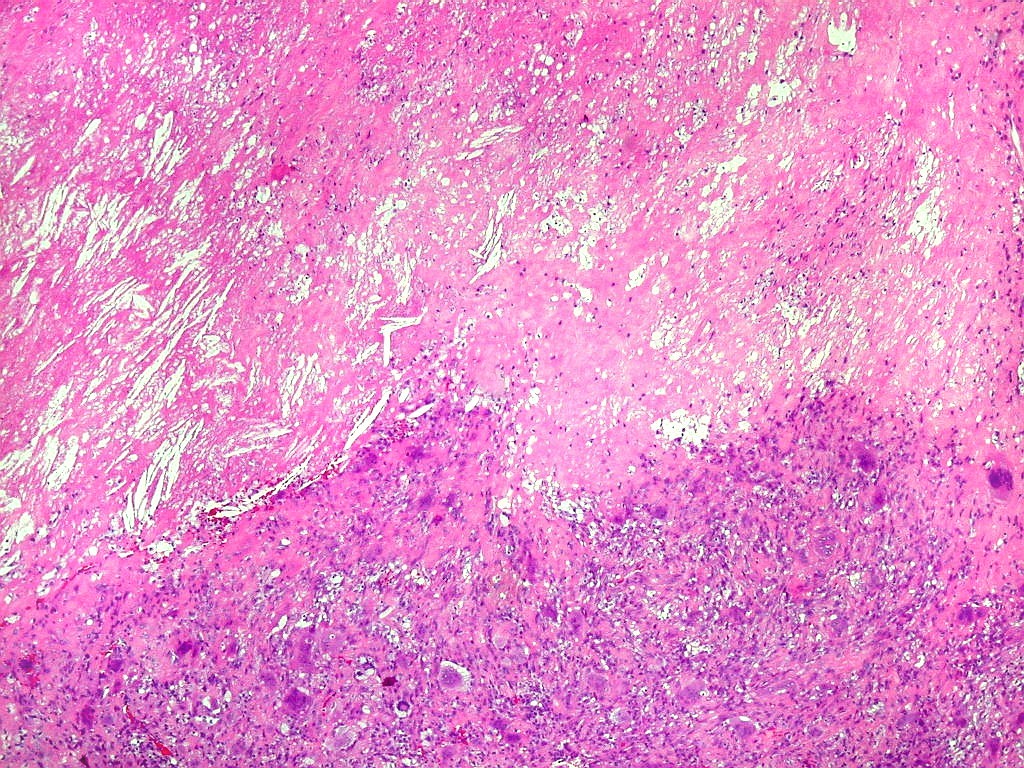
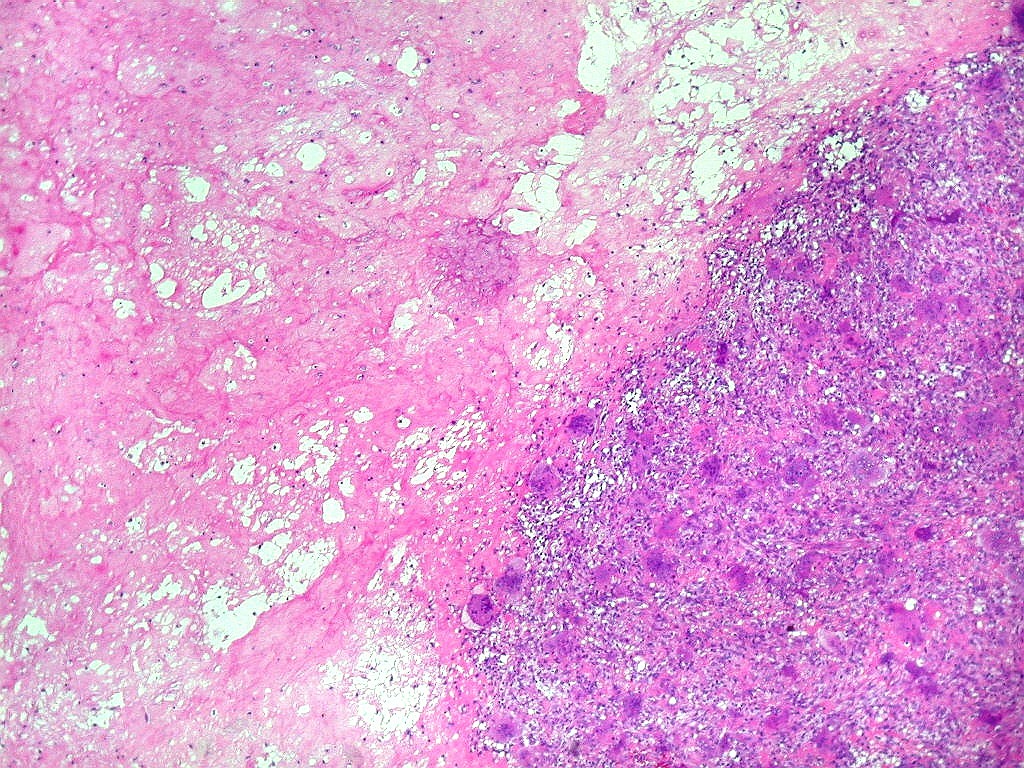
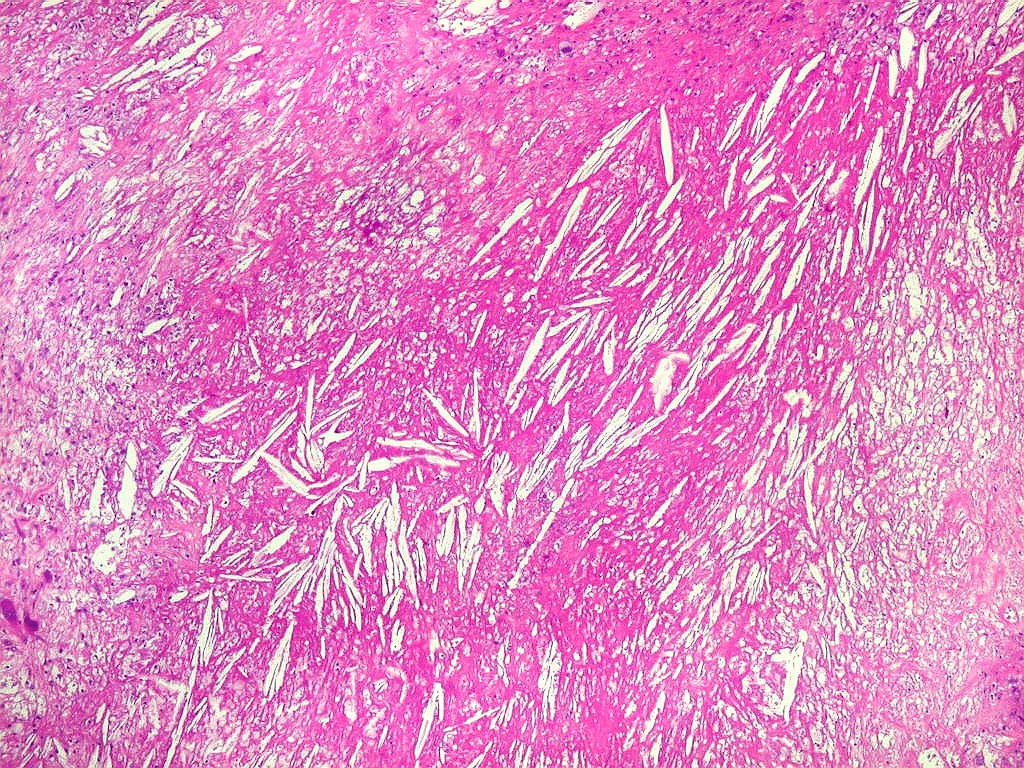
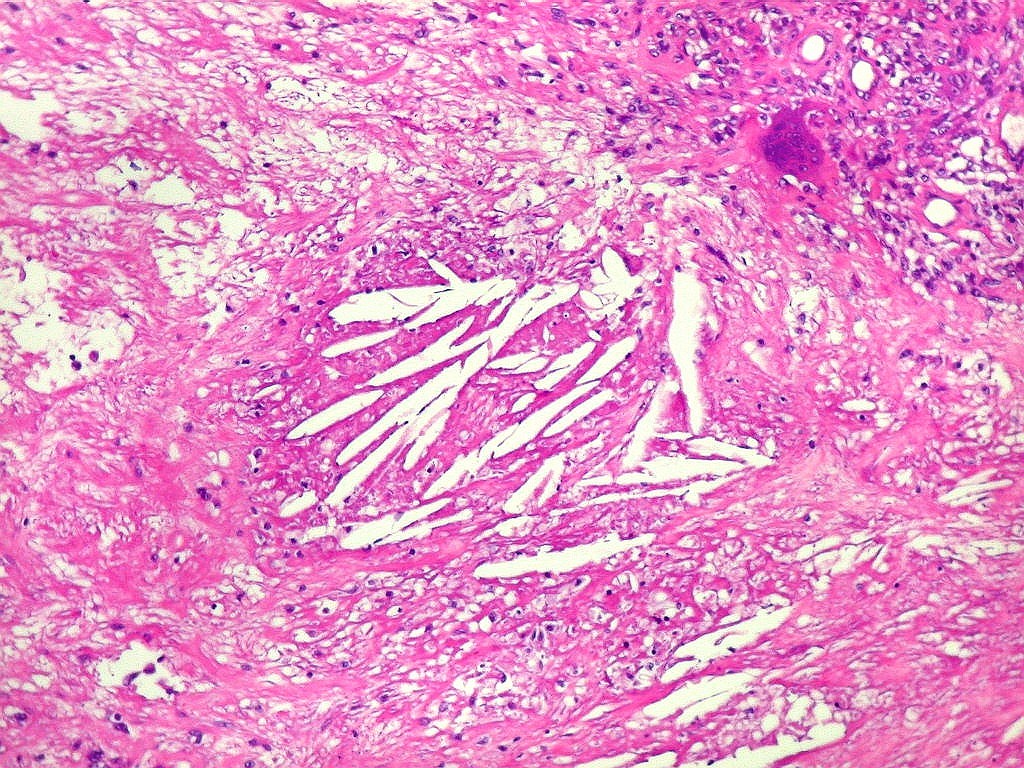
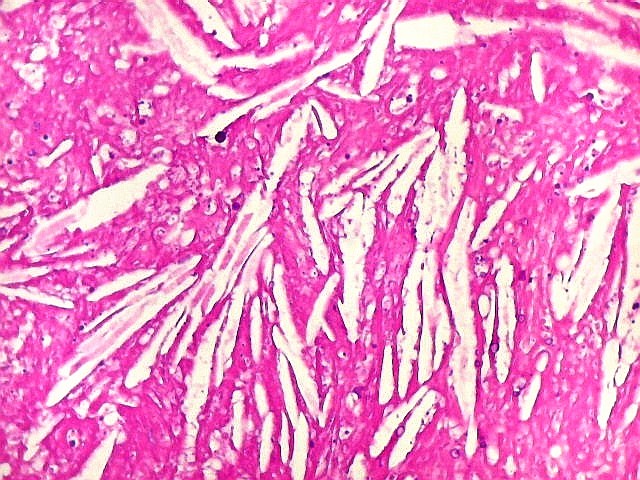
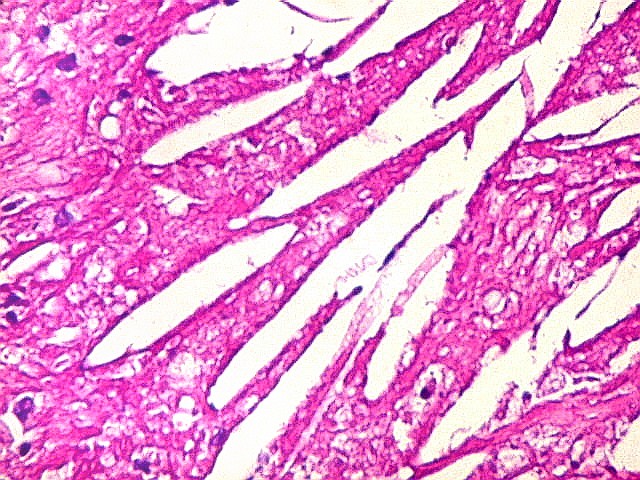
| Necrose coagulativa. Áreas de necrose coagulativa eram observadas esparsamente, não raro com fendas deixadas por cristais de colesterol (estes, removidos durante o processamento). |
 |
 |
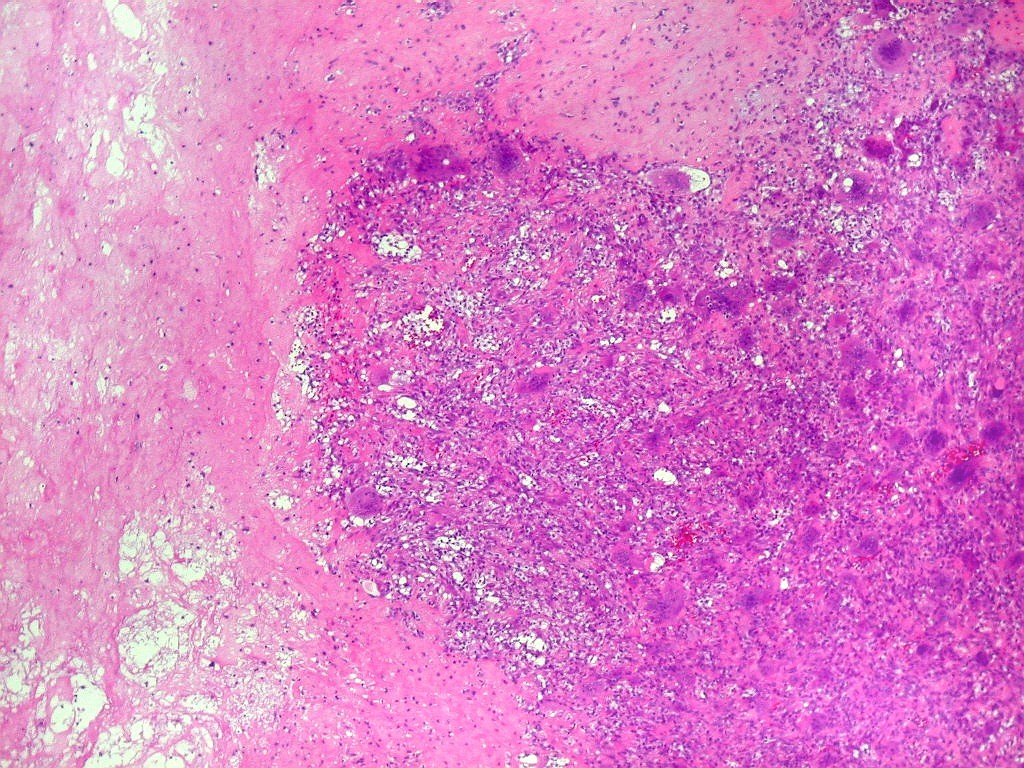 |
| Necrose e fendas de cristais de colesterol. Fendas de colesterol sugerem alto conteúdo lipídico do tecido antes da necrose. |
 |
 |
 |
 |
 |
|
|
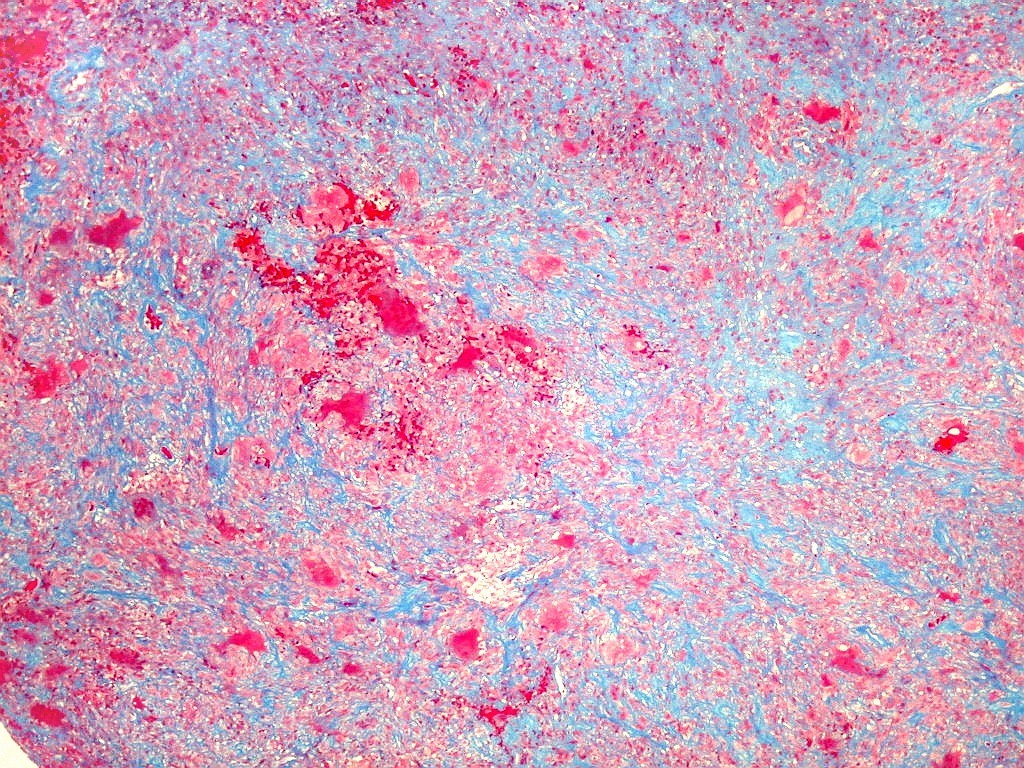
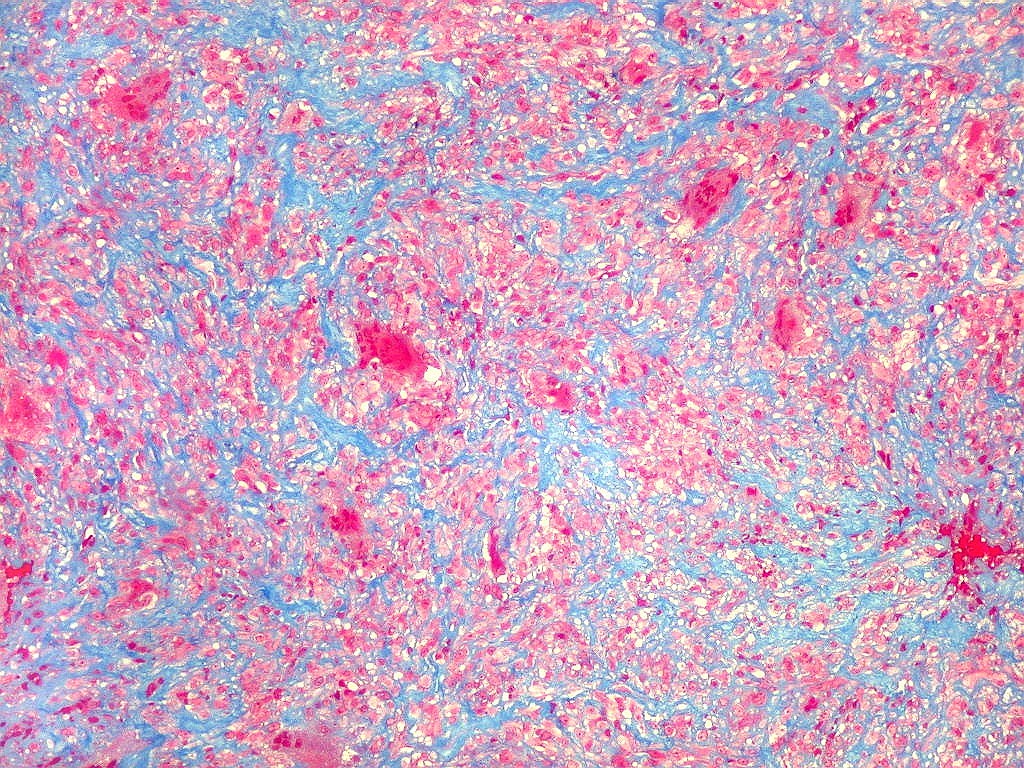
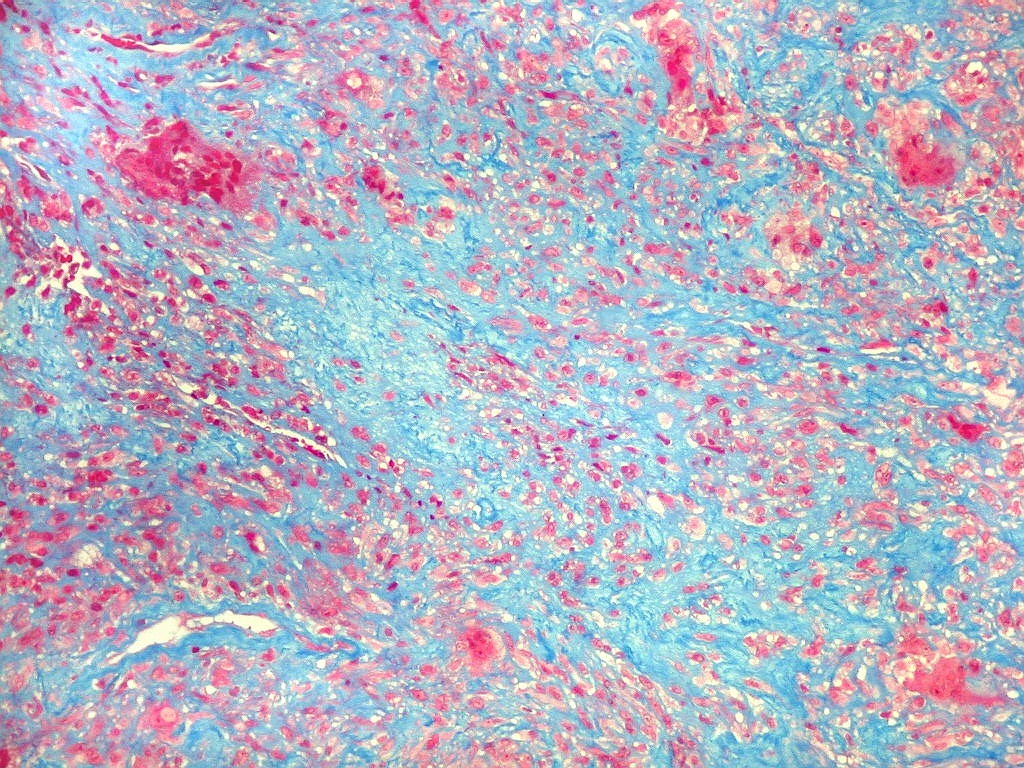
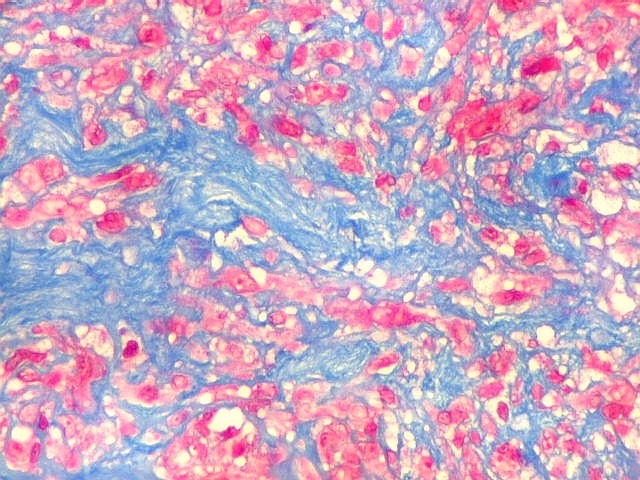
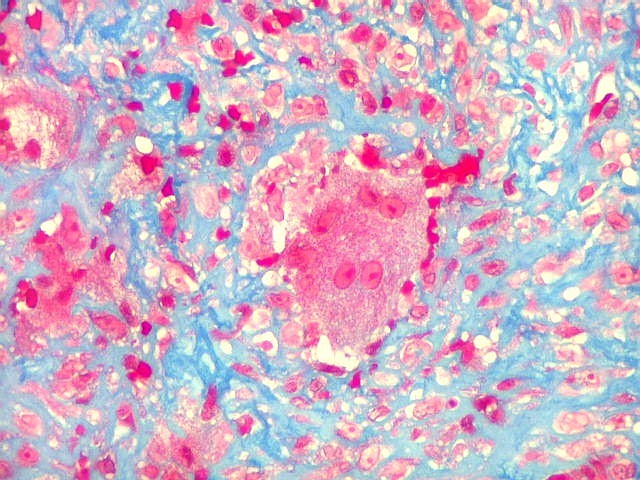
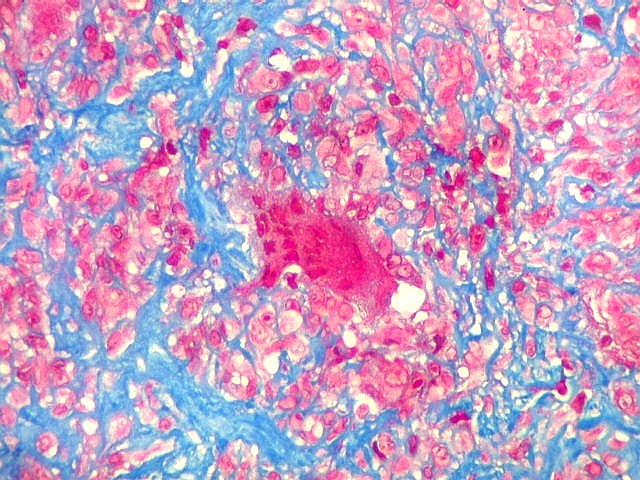
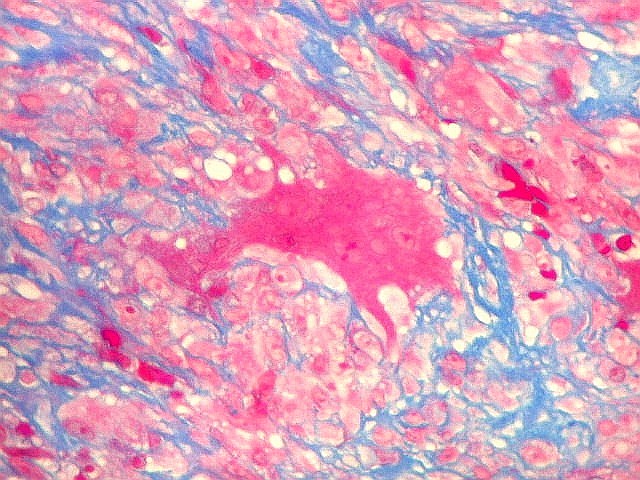
| Tricrômico de Masson. Esta coloração para tecido conjuntivo destaca fibras colágenas em azul contra os elementos celulares em vermelho. Assim, colabora para avaliar a quantidade de interstício em tumores, especialmente os do tecido conjuntivo. Em HE, isto não é possível, pois tanto as fibras intersticiais como o citoplasma das células coram-se em róseo. No presente material, cerca da metade do tecido é constituído por colágeno, claramente produzido pelas células neoplásicas ou, mais exatamente, pelas células fusiformes estromais, que são de natureza miofibroblástica, como demonstrado na reação para actina 1A4. |
 |
 |
 |
 |
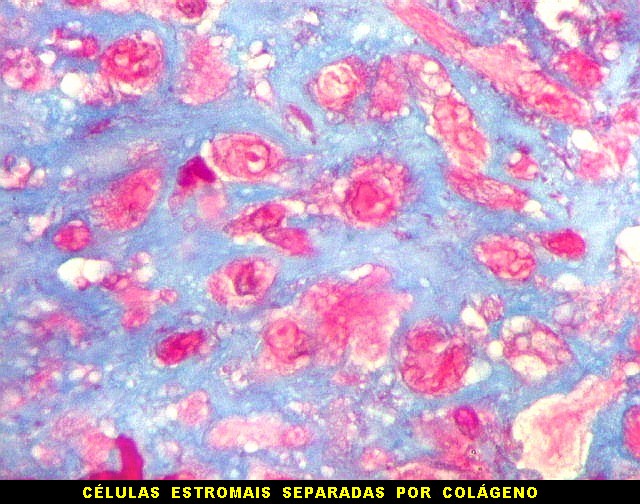
| Masson. Células estromais fusiformes. O Masson mostra que as células estromais são separadas umas das outras por fibras colágenas, indicando que esta proteína fibrilar intersticial é produzida por estas mesmas células. | |
 |
 |
 |
 |
 |
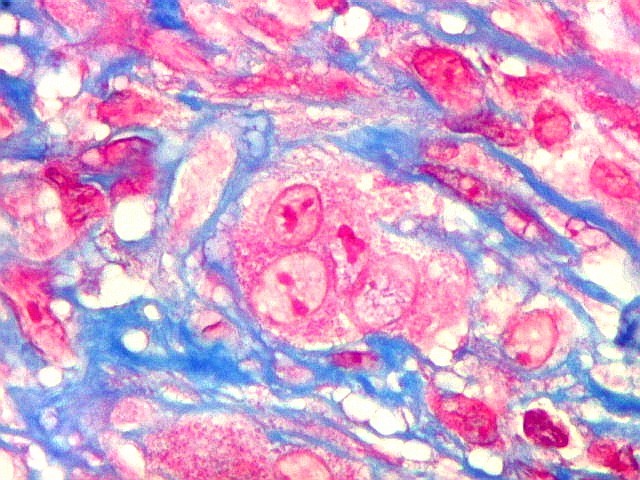 |
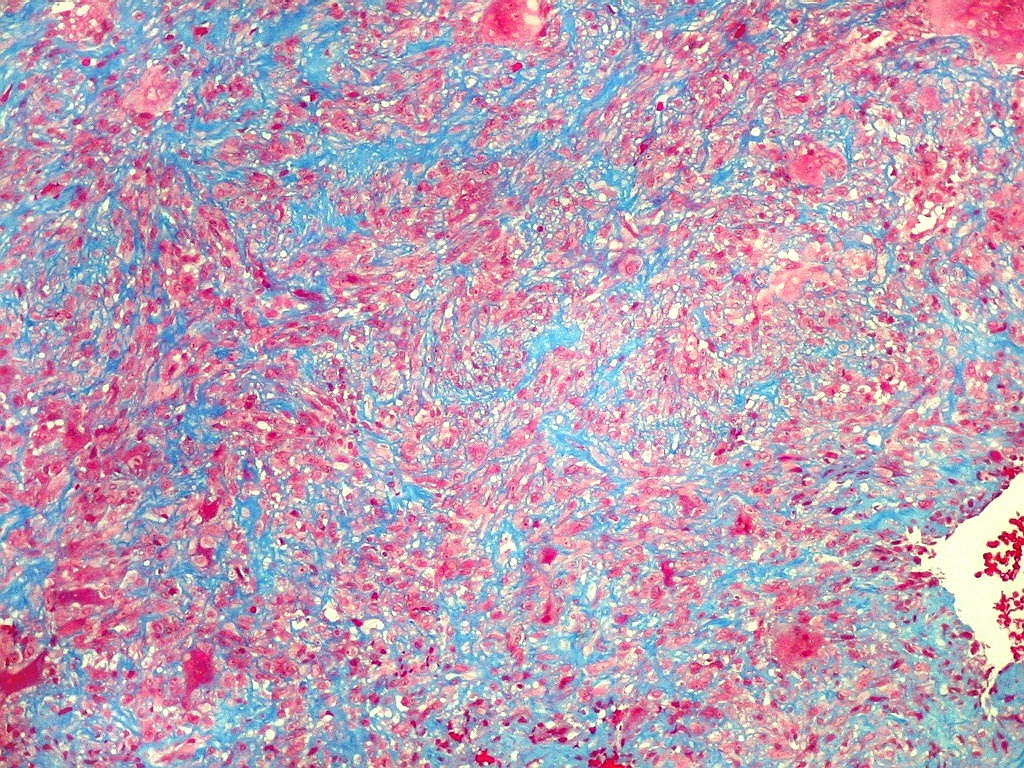
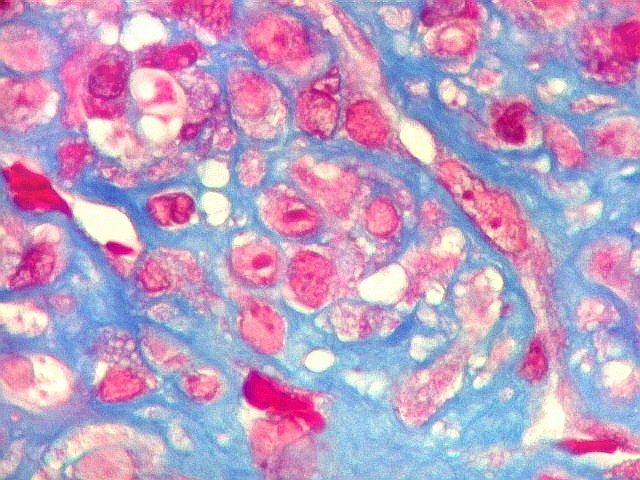
| Masson. Gigantócitos. As células gigantes chamam a atenção no Masson por seu citoplasma vermelho abundante e prolongamentos citoplasmáticos. | |
 |
 |
 |
 |
 |
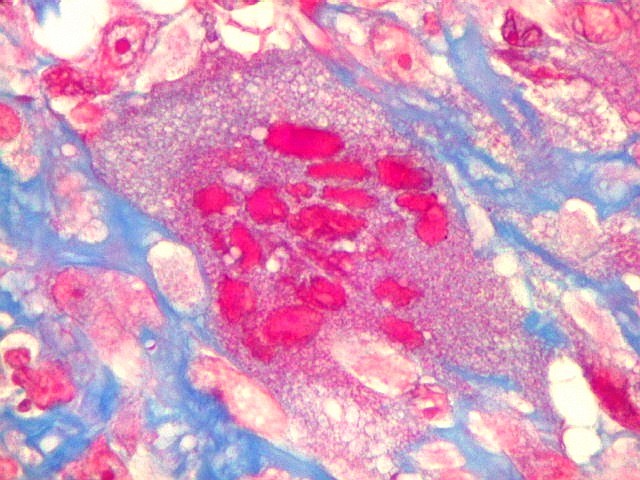 |
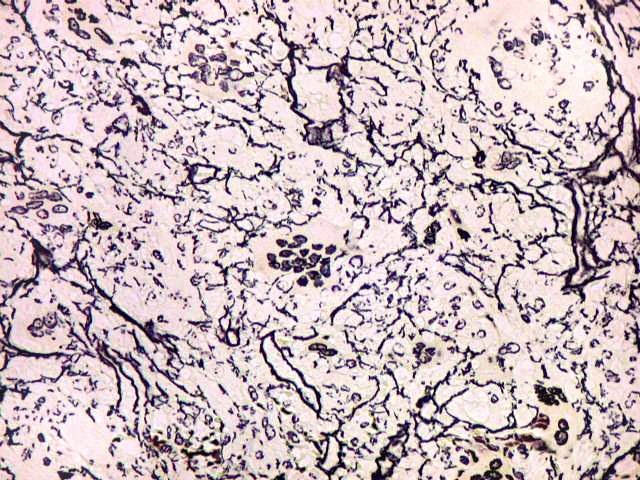
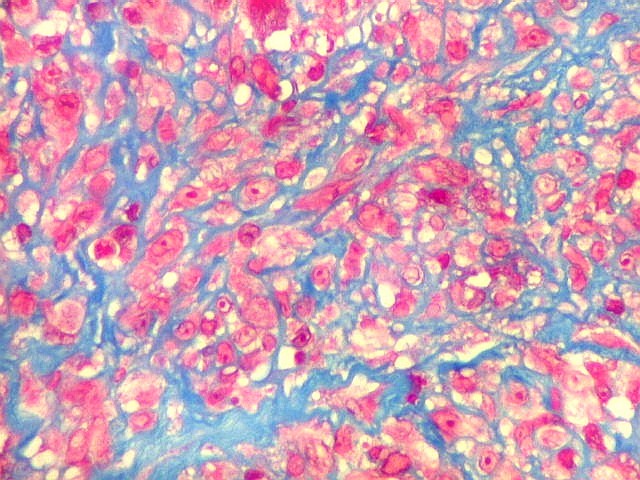
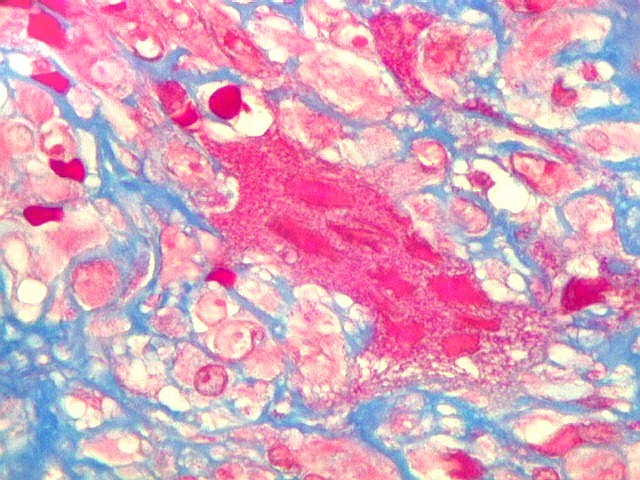
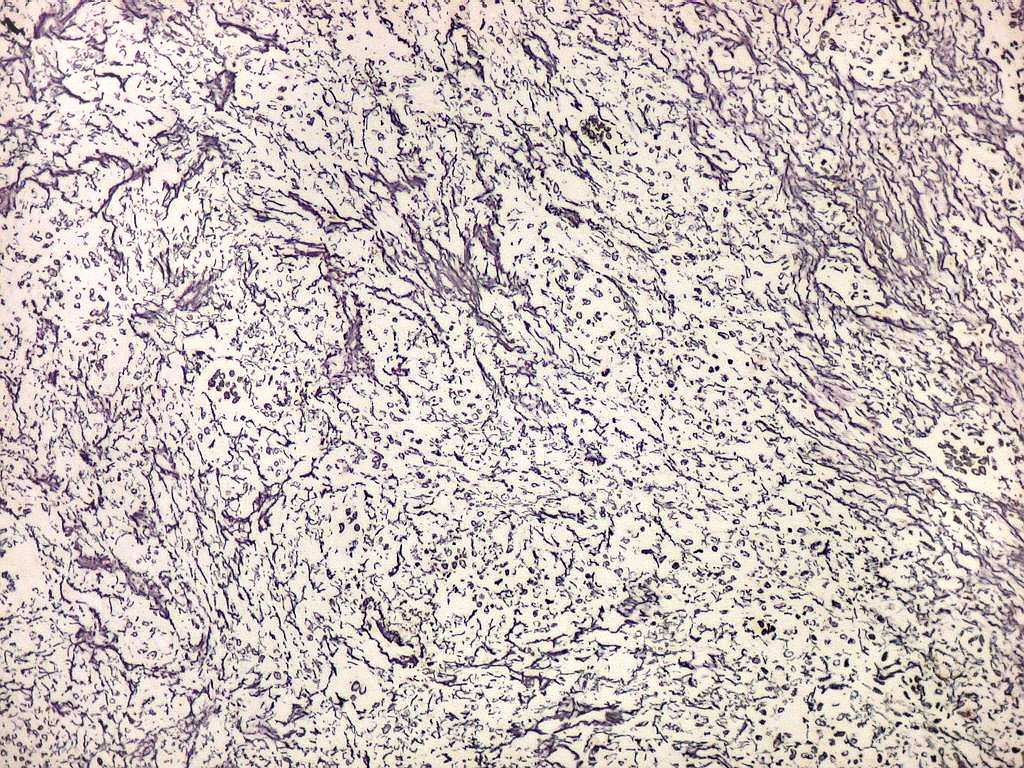
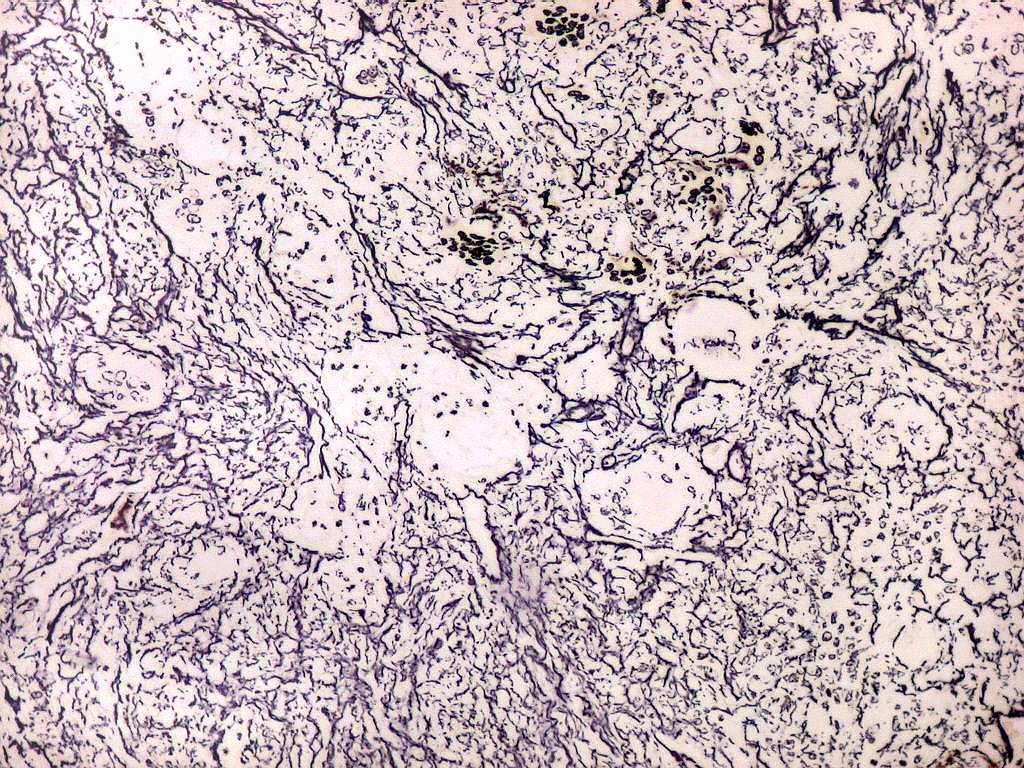
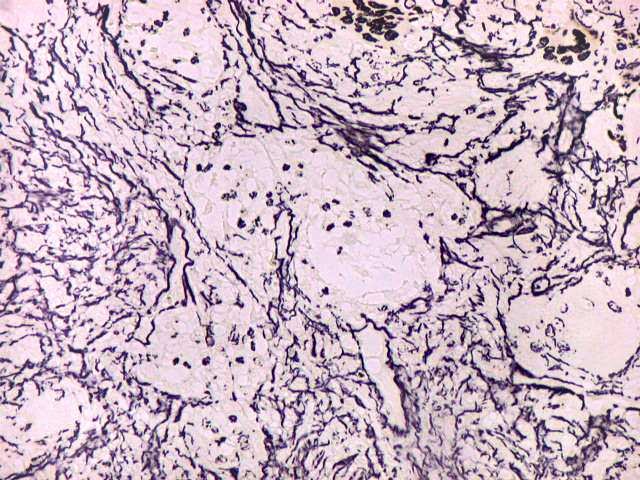
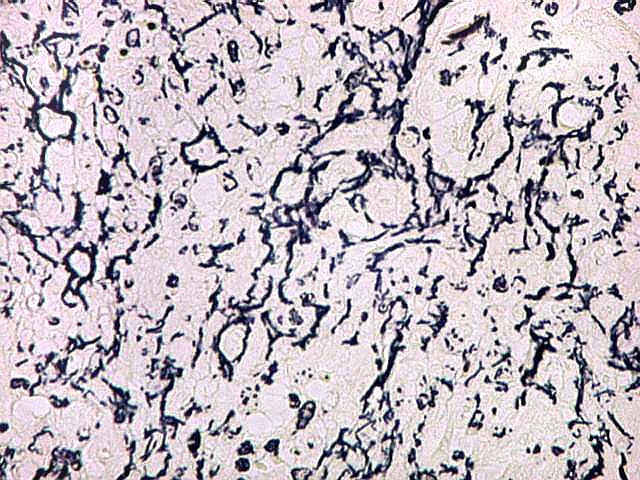
| Reticulina. A impregnação argêntica para fibras reticulínicas revela grande abundância destas fibras do tecido conjuntivo neste granuloma reparador de células gigantes, o que não surpreende, dada a analogia entre as fibras colágenas e reticulínicas, produzidas pelas mesmas células. |
 |
 |
 |
 |
 |
 |
| Granuloma
reparador de células gigantes.
Definição. São lesões benignas incomuns, com predileção por ossos crânio-faciais e ossos tubulares das mãos e pés. Descritos originalmente por Jaffe em 1953. Dados atuais sugerem que granulomas reparadores de células gigantes em diferentes topografias têm patogênese e fundamentos genéticos distintos. Microscopicamente têm feições superponíveis, com células gigantes multinucleadas distribuídas irregularmente num estroma fibroso com áreas de formação de osso reacional. Incidência e localização. Pico de incidência na 2ª. década. Maioria dos pacientes tem entre 10-25 anos. Localização principal na mandíbula e maxila. Na mandíbula são caracteristicamente na linha média, com alguma lateralização. No osso temporal, há vários relatos de casos isolados. Uma segunda localização é nos ossos tubulares pequenos das mãos e pés. São extremamente raros nos ossos longos e vértebras. Na grande maioria são lesões isoladas. Radiologia. Nos ossos crânio-faciais produzem área arredondada ou ovalada de radiolucência com bordas nítidas e mínima esclerose reacional. Microscopia. Tecido estromal fibroso com fibroblastos fusocelulares, de celularidade moderada a alta e quantidade variável de colágeno. Mitoses típicas são raras. A feição chave são células gigantes multinucleadas formando agrupamentos separados por feixes de tecido estromal. Há quase sempre evidência de hemorragia recente ou antiga (hemossiderina). Essas alterações podem ser intensas a ponto de simular um cisto ósseo aneurismático. Há poucas células inflamatórias mononucleares e trabéculas de osso neoformado com rimas de osteoblastos. Microscopia eletrônica. as células gigantes multinucleadas expressam feições de osteoclastos. As células estromais fusiformes tipicamente mostram diferenciação miofibroblástica. Citogenética. em alguns casos demonstrou-se rearranjo clonal envolvendo vários cromossomos, o que sugere que sejam neoplasias, não proliferação reacional. Diagnóstico diferencial. envolve o tumor marrom do hiperparatiroidismo, tumor de células gigantes, fibroma não ossificante e tenossinovite vilonodular pigmentada. A lesão é microscopicamente indistinguível do tumor marrom do hiperparatiroidismo, o que indica estudos laboratoriais de cálcio e fósforo e estudo clínico e radiológico das paratiróides. Há forte superposição também com o tumor de células gigantes, mas as diferenças em idade e topografia ajudam no diagnóstico diferencial. No tumor de células gigantes, o pico de incidência é entre 20 e 45 anos (são raros em esqueleto imaturo, mas cerca de 10% ocorrem na 2ª. década). A localização típica é nas extremidades de ossos longos, fêmur distal, tíbia proximal, rádio distal e úmero proximal. Na coluna a maioria se origina nos corpos vertebrais do sacro, seguindo-se coluna lombar, torácica e cervical em ordem decrescente de freqüência. Ossos chatos são pouco envolvidos, sendo o íleo o mais comum. Tratamento. curetagem completa da lesão, que pode necessitar repetição em recidivas. Fontes. Czerniak B. Dorfman and Czerniaks Bone Tumors. 2nd Ed. 2016 Elsevier Saunders, pp 742-52. Neville BW, Damm DD, Allen CM, Bouquot JM. Oral and Maxillofacial Pathology. 3rd Ed. 2009 Elsevier Saunders, pp 626-9. Athanasou NA, et al. Giant Cell Tumour of Bone. In WHO Classification of Tumours of Soft Tissue and Bone. Fletcher CDM, Bridge JA, Hogendoorn PCW, Mertens F (editors). 4th Ed. International Agency for Research on Cancer, Lyon, 2013. pp 321-4. |
| Agradecimentos.
Caso do Centro Infantil Boldrini, Campinas, SP. Preparações
de HE pelos membros do Laboratório de Patologia - Aparecido Paulo
de Moraes, Irineu Mantovanelli Neto e Adriana Worschech.
Fotos macro, Irineu Mantovanelli Neto e Aparecido Paulo de Moraes. Colorações especiais realizadas no Depto de Anatomia Patológica da FCM-UNICAMP (Sra. Tayna Takahashi Santos). |
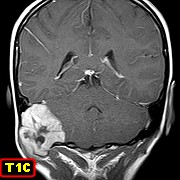
| Para mais imagens deste caso e | TC, RM | Macro, HE, Masson, Reticulina | IH - CD68, VIM, 1A4, CD34, Ki67 |
 |
 |
 |
|
imagem, patologia |
|
|
|
|
| Neuropatologia
- Graduação |
Neuropatologia -
Estudos de casos |
Neuroimagem
- Graduação |
Neuroimagem -
Estudos de Casos |
Roteiro
de aulas |
Textos
de apoio |
Correlação
Neuropatologia - Neuroimagem |
| Índice alfabético - Neuro | Adições recentes | Banco de imagens - Neuro | Textos ilustrados | Neuromuscular | Patologia - outros aparelhos | Pages in English |
|
|