|
|
5 - Células 'plumiformes' em CD34 |
|
|
|
5 - Células 'plumiformes' em CD34 |
|
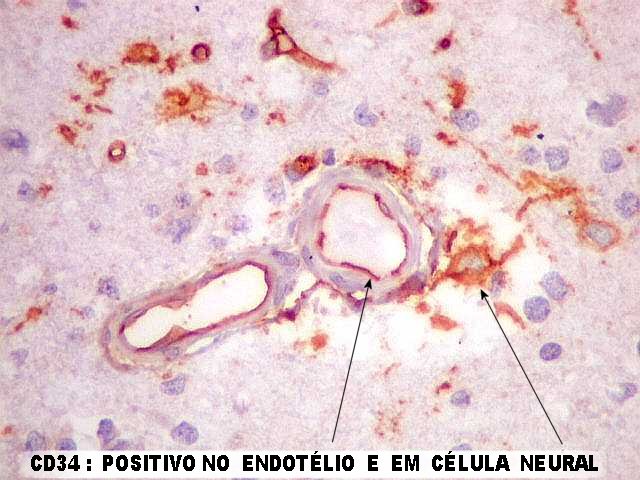
| O encontro casual de células neurais com morfologia não usual na lâmina para o antígeno CD34 motivou estudo mais detalhado, vazado nesta página. Achado semelhante já havia ocorrido anteriormente em um caso de ganglioglioma e outro de xantoastrocitoma pleomórfico. |
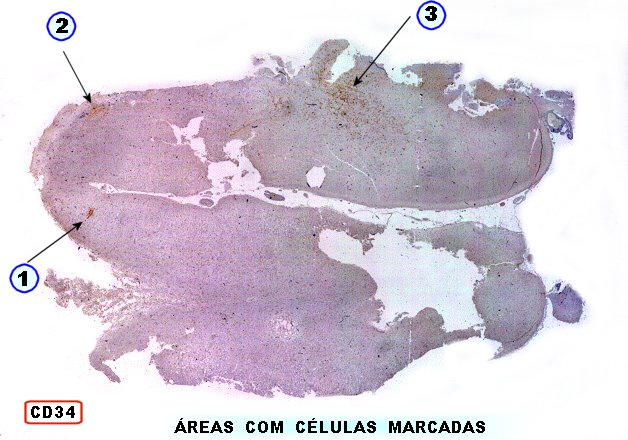
| CD34.
Áreas com células
'plumiformes'. Este corte de IH para CD34 foi escaneado com exagero de contraste para tentar mostrar as áreas com células reativas para CD34, cujos detalhes são dados abaixo. As áreas marcadas aparecem em marrom e são escassas em relação ao restante, onde só capilares são positivos. |
 |
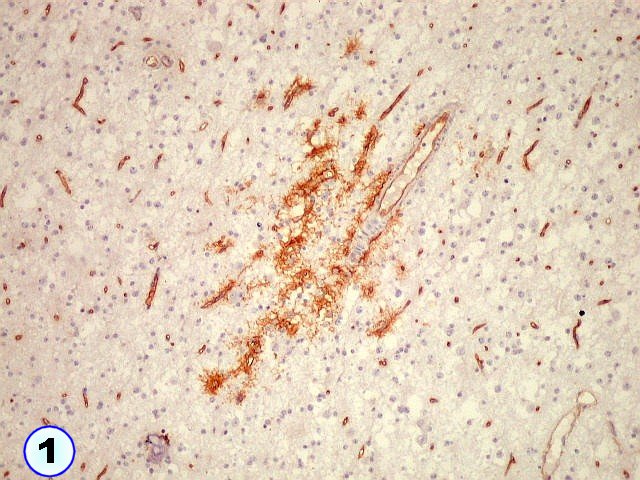
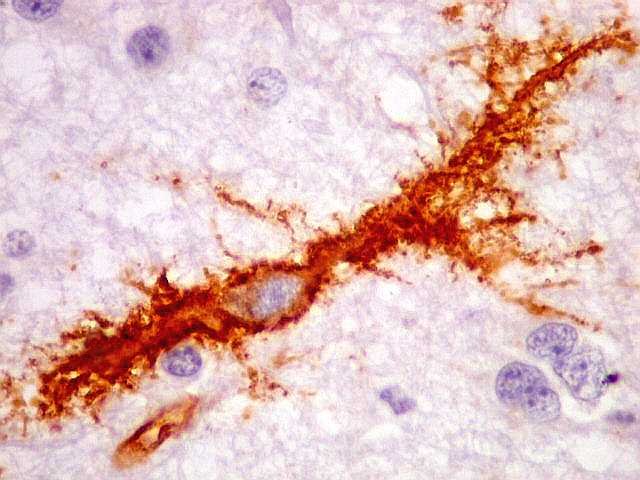
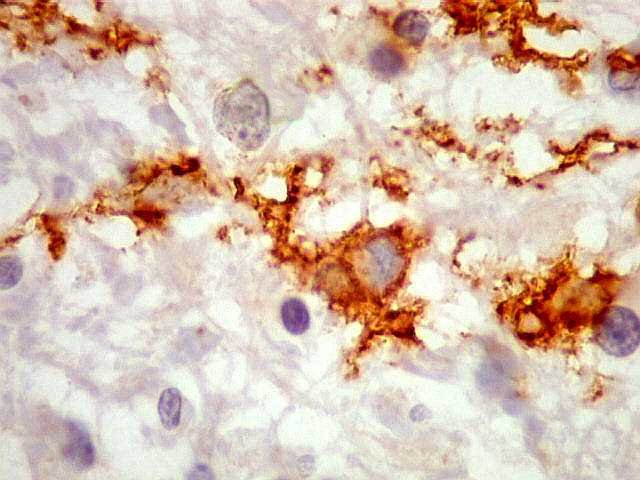
| Células 'plumiformes'. Estas curiosas células com positividade para CD34 destacam-se em alguns focos no tecido. Lembram astrócitos protoplasmáticos pela exuberante ramificação dos seus prolongamentos, semelhantes a plumas, e sua íntima relação com vasos. São claramente anormais em função do tamanho maior, citoplasma abundante e forma pouco usual, mas a sua real natureza é incerta (ver comentário no fim da página). Abaixo, detalhes da área 1. | |
 |
|
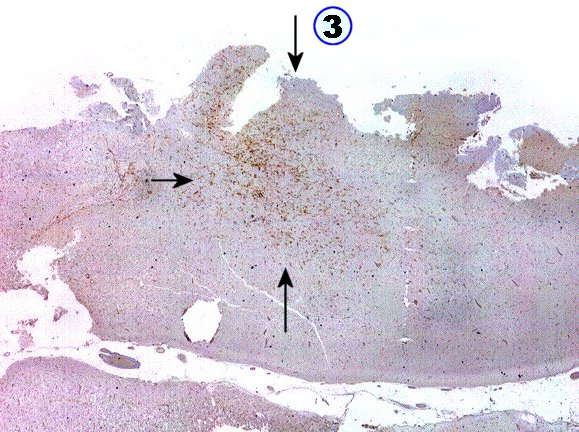 |
Área
3.
Esta é
a área mais extensa e rica nas células CD34 positivas e encontra-se
no limite entre córtex com DNT e a substância branca subjacente.
|
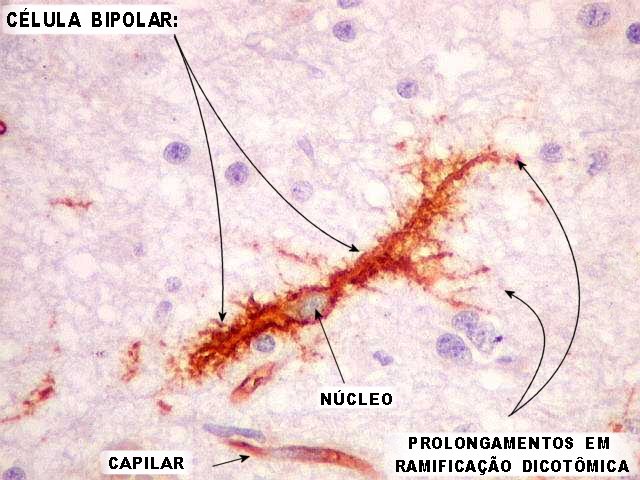
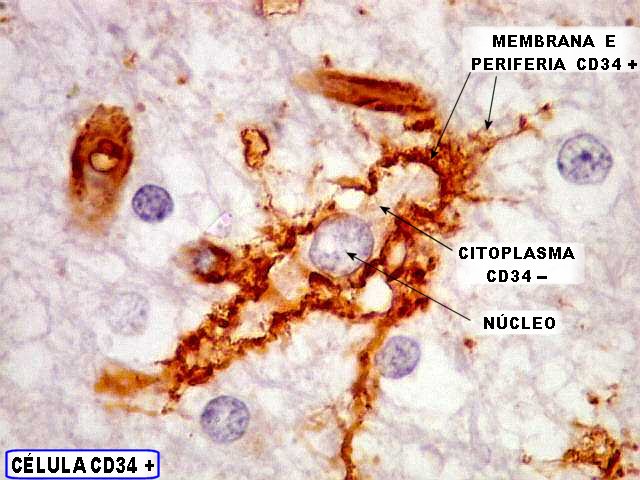
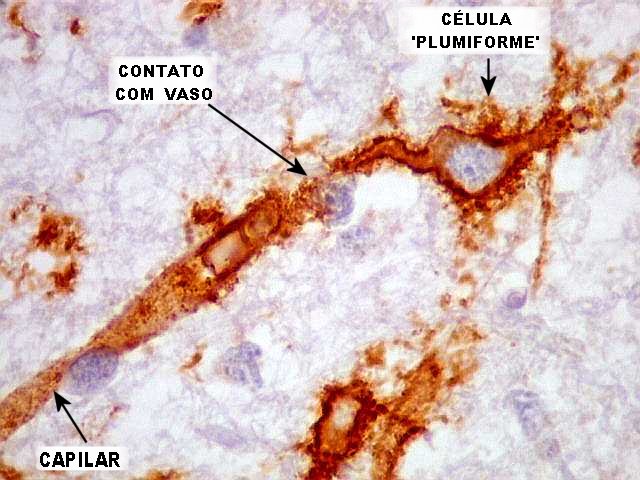
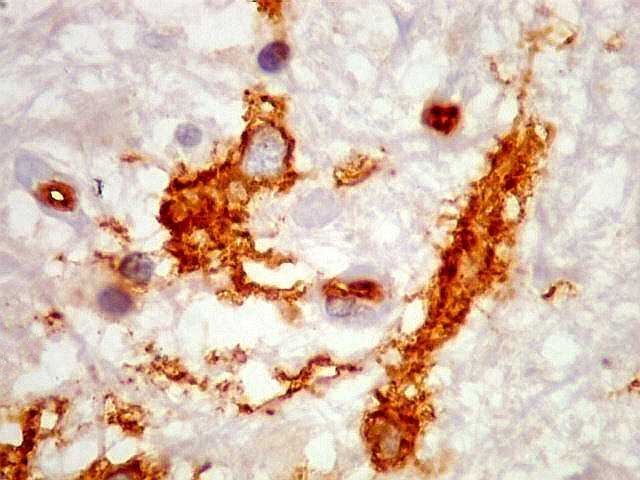
| CD34. Células anômalas 'plumiformes'. Estas células, que parecem de linhagem neuroectodérmica, têm estrutura peculiar não compartilhada pelas células normais do SNC. Não lembram neurônios ou oligodendrócitos. Parecem densamente ramificadas como astrócitos protoplasmáticos, mas sua forma bipolar as aproxima mais das células microgliais, que são, contudo, muito menores. Além disso, as células 'plumiformes' são CD68 negativas. Segundo Blümcke et al. (1999), poderiam ser originadas de precursores neurais displásicos ou com diferenciação atípica (ver discussão no fim da página). | |
 |
|
 |
|
 |
|
 |
|
 |
|
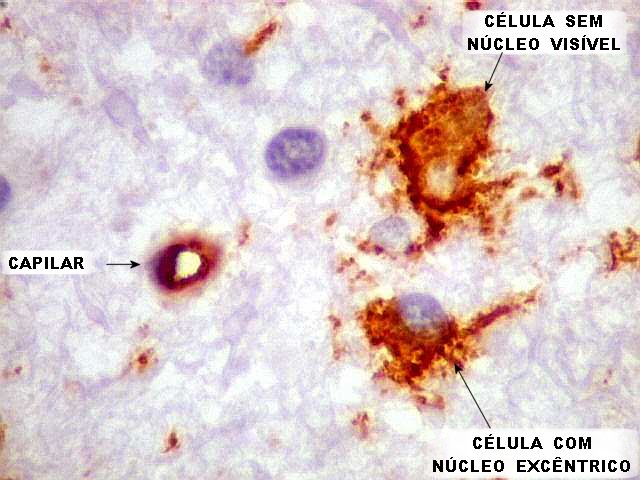
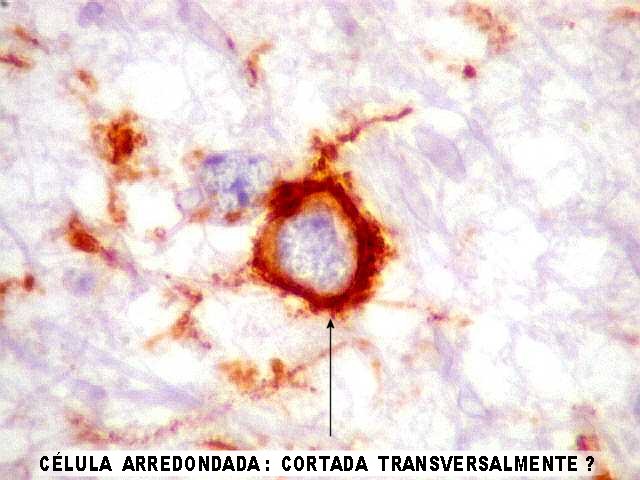
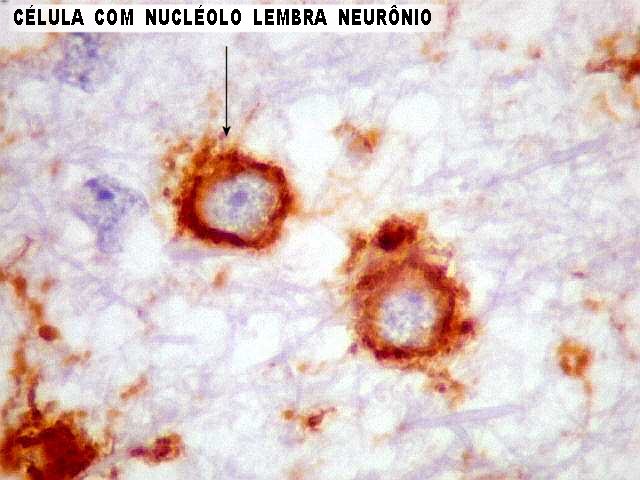
| Em algumas células não se identifica o núcleo (fora do plano de corte?) | |
 |
 |
 |
 |
 |
|
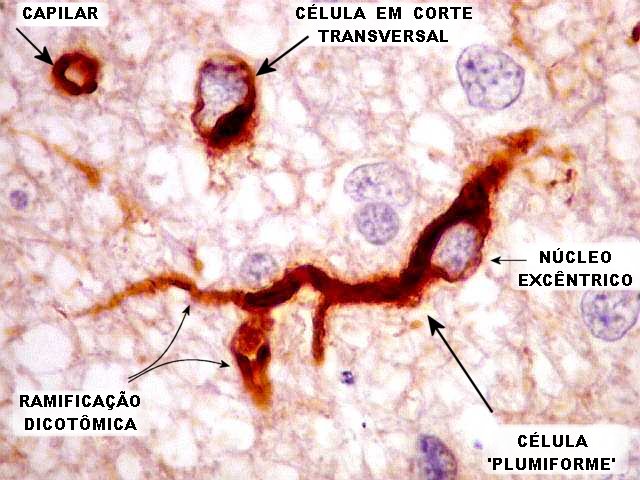
| VIM. O aspecto raro das células 'plumiformes' em CD34 nos despertou a curiosidade de reexaminar outras reações para tentar identificá-las. O melhor resultado foi com vimentina, onde se notaram várias células que corresponderiam às vistas com CD34. Têm prolongamentos grossos, aproximadamente retilíneos, freqüentemente bipolares, saindo de cada lado de um núcleo excêntrico em relação ao eixo da célula. Alguns destes prolongamentos espessos têm relação com vasos à maneira de pés sugadores, apoiando uma possível natureza astrocitária. | |
| VIM. Células 'plumiformes'. Admitimos que as células demonstradas abaixo correspondam às 'plumiformes' vistas com CD34. Como não fizemos estudos de co-localização antigênica, esta correspondência é hipotética, baseada na forma das células, diferente da dos astrócitos hipertróficos abundantes na lesão. Há um eixo de vimentina em forma de bastonete que percorre o centro da célula. A periferia seria revestida por uma membrana positiva para CD34. | |
|
|
|
 |
|
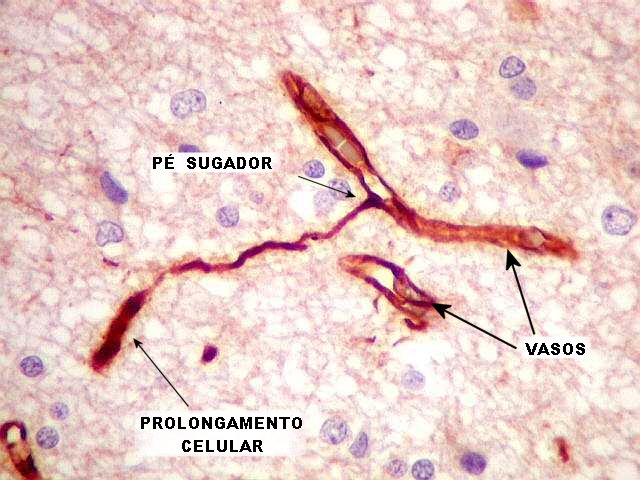
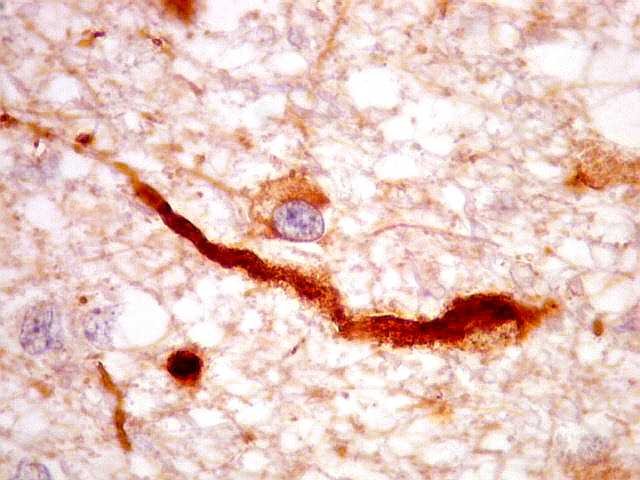
| VIM. Pés sugadores? Nas figuras abaixo, prolongamentos espessos, presumivelmente pertencentes às células em questão, parecem terminar em vasos, à maneira de pés sugadores de astrócitos. Estas imagens apoiam que as células sejam de natureza astrocitária. | |
 |
|
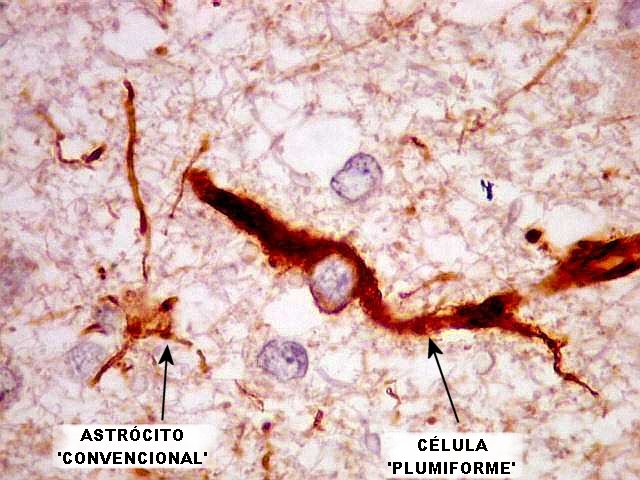
| VIM. Comparação com astrócitos 'convencionais'. Nas duas figuras abaixo, astrócitos hipertróficos multipolares do tipo habitual em lesões do tecido nervoso foram fotografados ao lado das células anômalas em pauta. Estas últimas diferem substancialmente deles, com seus prolongamentos grossos e disposição uni- ou bipolar. Nas células que parecem unipolares, o outro prolongamento pode estar fora do plano de corte. | |
 |
 |
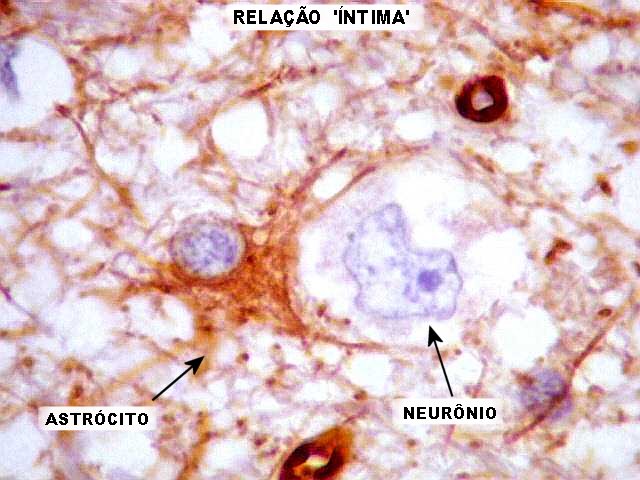
| VIM. Mais astrócitos 'convencionais'. São também anômalos. Alguns são binucleados, outros mostram a curiosa 'relação íntima' com neurônios, como também freqüentemente visto com VIM e S-100 neste caso e em outros de doenças associadas a epilepsia, como um raro caso de gangliocitoma com área de ganglioglioma e casos de displasia cortical (1) (2). | |
 |
|
 |
|
| CD34 vs. VIM. Células fotografadas no mesmo aumento e comparadas lado a lado. O quadro dá suporte a que sejam células análogas, com citoplasma vimentina positivo, e membrana CD34 positiva. Não fica claro se as delicadas excrescências reveladas com CD34 seriam ramificações do citoplasma ou só material proteico aderido à periferia da célula. | |
| CD34 | VIM |
 |
|
| HE. Exame da mesma área 3 em HE revelou neurônios e núcleos de células da glia, mas não foram idenficadas as células correspondentes às encontradas com CD34 e VIM. | |
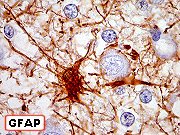
| GFAP. A impressão de que as células positivas para CD34 pudessem ser astrócitos levou a busca cuidadosa pelas mesmas usando GFAP. |
| Contudo, a pesquisa revelou-se infrutífera. Foram observados muitos astrócitos hipertróficos semelhantes aos vistos em outras áreas, e aos demonstrados com VIM nas áreas positivas para CD34. Porém, não foram encontradas células GFAP + que morfologicamente lembrassem as 'células plumiformes'. | |
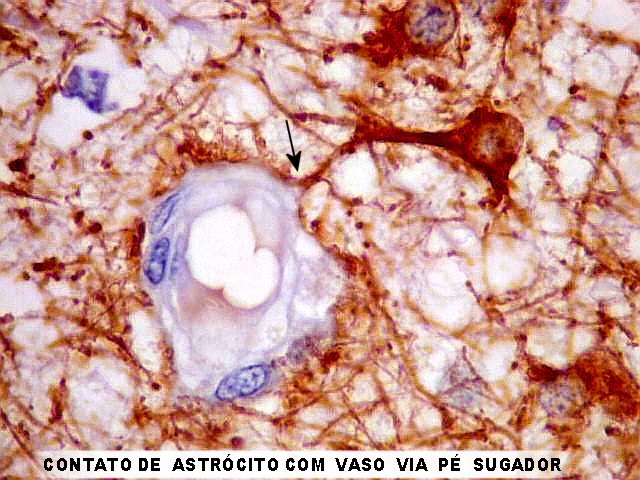
| GFAP. Relação íntima. O contato direto entre corpos celulares de neurônios e astrócitos já fora notado nas áreas de DNT deste caso (1) (2) (3) e de outras doenças associadas a epilepsia, como um raro caso de gangliocitoma com área de ganglioglioma e casos de displasia cortical (1) (2). | |
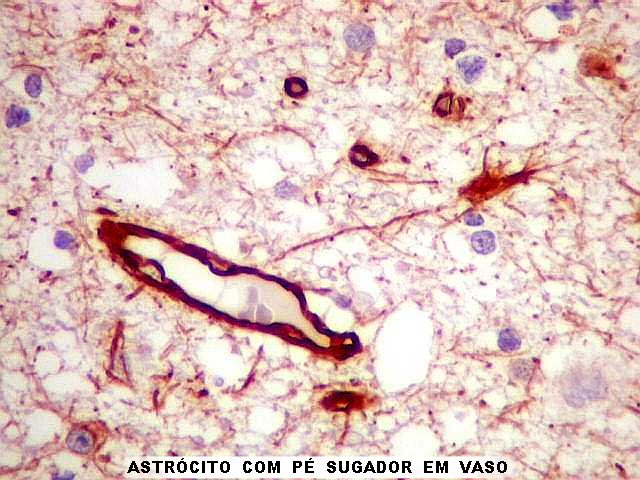
| GFAP. Relação com vasos. Os astrócitos hipertróficos comumente lançavam prolongamentos a vasos formando 'pés sugadores'. Aqui, porém, também foram notados astrócitos contactando vasos através de seu próprio corpo celular, em vez de prolongamentos. Aspecto semelhante já fora visto em um caso de displasia cortical. | |
 |
 |
| GFAP. Bi e trinucleação. Anomalias dos astrócitos 'convencionais' na área 3. O astrócito binucleado à E apresenta discariose e perda da relação núcleo-citoplasma. | |
| S-100. Nas áreas de células 'plumiformes' havia muitos astrócitos positivos para S-100, alguns muito volumosos, com citoplasma extensamente ramificado e multinucleação. É possível que alguns destes poderiam representar as células 'plumiformes' marcadas por CD34. A certeza exigiria estudos de colocalização antigênica (não disponíveis no momento). | |
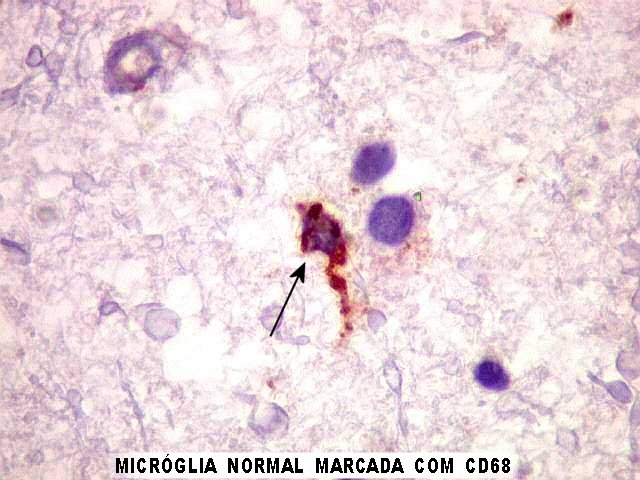
| CD68. Área de células 'plumiformes'. A pesquisa de CD68 foi feita porque algumas células 'plumiformes' lembravam micróglia, por seu caráter bipolar. Contudo, as células foram negativas para CD68, um marcador de macrófagos e, portanto, também de células microgliais. Abaixo, exemplos de micróglia normal na mesma área, servindo de controle interno positivo. | |
 |
|
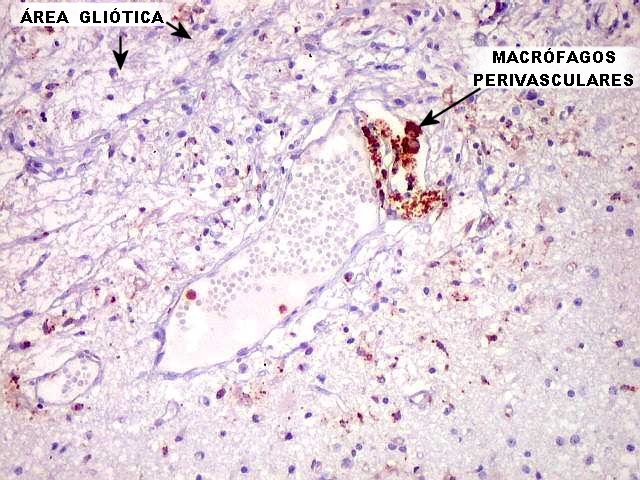
| CD68. Área lesada na cirurgia anterior. Uma pequena área de gliose densa, atribuível à lesão cirúrgica de 2 anos antes, apresentava células grânulo-adiposas (macrófagos xantomatosos) agrupados no tecido ou em localização perivascular. Essas células são fortemente CD68 positivas. | |
 |
|
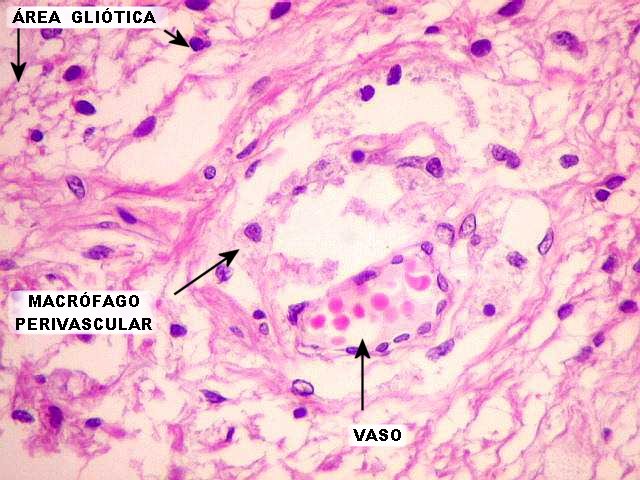
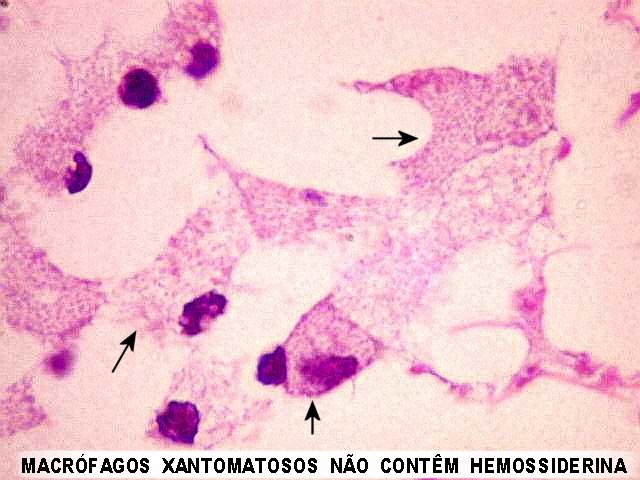
| HE. Mesma área para comparar. A mesma área foi localizada em HE para verificar se os macrófagos continham hemossiderina, que, pela cor marrom, poderia ter simulado positividade no CD68. Contudo, verifica-se que os macrófagos espumosos não abrigam pigmento, o que confirma que a reação para CD68 é, de fato, positiva. | |
 |
|
 |
|
| Comentário.
A natureza destas células, para as quais cunhamos o termo plumiformes
(em inglês seria 'feathery'), é incerta. Já
as havíamos encontrado um caso de ganglioglioma
e outro de xantoastrocitoma pleomórfico.
O fato de não serem reconhecidas na lâminas para GFAP torna
problemática, a nosso ver, sua classificação como
astrócitos.
Abaixo transcrevemos
trechos do trabalho de I Blumcke et al., que promoveram extenso estudo
de casos de diversas condições patológicas associadas
a epilepsia crônica e elaboraram uma discussão lúcida
sobre estas células. Os autores também evitam o termo
astrócito
para sua denominação.
Estudo imunohistoquímico de lesões focais associadas a epilepsia crônica, que demonstrou uma população de células neuroectodérmicas reativas para CD34, não previamente descritas no sistema nervoso central de humanos adultos. CD34 marcou a superfície de células gliais protoplasmáticas, também reativas para S100, e algumas células com morfologia neuronal. CD34 é uma proteína marcadora oncofetal expressada na fase inicial do desenvolvimento. É um marcador de células tronco expressado transitoriamente na neurulação precoce. A associação de CD34 com tipos celulares imaturos em tumores indiferenciados de tecido hemopoiético e do TGI sugere que CD34 localiza-se em precursores neurais displásicos ou com diferenciação atípica em lesões malformativas ou tumores de pacientes com epilepsia. Não pode ser excluído que CD34 seria expressado transitoriamente em um estágio precoce de neurulação no cérebro humano. A função de CD34 é desconhecida, mas poderia estar envolvida em adesão celular e vias de transdução de sinal intracelulares. É expressa na superfície de células progenitoras de precursores mielóides, no endotélio vascular (nas fases embrionária, fetal e adulta), em tumores fibrosos indiferenciados da pleura, mediastino e TGI, tumor solitário das meninges, e schwannomas e neurofibromas. A expressão de CD34 parece diminuir em casos mais malignos. No camundongo, expressão de CD34 ocorre durante a neurulação e reação fraca pode ainda persistir no período pós-natal. Porém, em tecido nervoso humano normal ou em doenças degenerativas, inflamatórias e neoplásicas, CD34 é negativo. Células CD34 co-expressam S100, uma proteína intracelular ligadora de cálcio presente em várias populações de células gliais e em células de Schwann, células de Langerhans, células hemopoiéticas e alguns tumores de baixo grau. Isto sugere que o antígeno CD34 em lesões associadas a epilepsia seria expresso por uma população de células neurais displásicas ou atipicamente diferenciadas. Em 262 pacientes com epilepsia crônica focal, células não endoteliais reativas para CD34 foram encontradas em 48,6 % dos espécimes. A maioria das amostras de tecido mostrou células neurais positivas para CD34 em gangliogliomas (74%), astrocitomas de baixo grau (62%) e oligodendrogliomas (59%). Em lesões malformativas não neoplásicas, como hamartias glioneuronais, 52 % mostraram células positivas solitárias ou em pequenos grupos. DNT foi positivo em 17% dos casos (considerado raro). Tecidos adultos controles, espécimes de cérebro humano fetal e tumores de pacientes sem epilepsia foram todos negativos. Um teratoma maligno de ovário com diferenciação neural precoce apresentou positividade focal. As células CD34 positivas tinham um padrão de imunorreatividade em rede na sua membrana externa e a coloração era positiva também nos processos distais. Na morfologia ao MO, a maioria das células reativas para CD34 pareciam células neuroectodérmicas, principalmente astrócitos protoplasmáticos, mas algumas tinham aparência neuronal. As células estavam isoladas ou formavam pequenos grupos misturados com o córtex e a substância branca. Era comum a intensa ramificação dos processos celulares, as vezes contactando capilares. Este padrão foi considerado consistente com células gliais displásicas. A maioria das células CD34 positivas co-localizaram com proteína S100 em todos os casos, mas nunca com GFAP. Uma pequena subpopulação também foi positiva para antígenos neuronais (neuronal nuclear protein ou NeuN, e MAP2). Sinaptofisina e proteína de neurofilamento não mostraram co-expressão. Também não houve co-expressão com vimentina, CD31, fator VIII e antígeno leucocitário comum ou LCA. Algumas células foram positivas para Ki-67. Não foi observada reatividade para CD34 em células microgliais (reconhecidas por CD68). A maioria das lesões identificadas na área epileptogênica de pacientes com epilepsia refratária localiza-se no lobo temporal (uma área anatomicamente complexa) e é composta por neurônios e glia intimamente misturados. O índice de proliferação é baixo, dificultando a distinção entre entidades malformativas e neoplásicas, ambas possivelmente originadas em aberrações precoces do desenvolvimento. Um alelo raro do gene TSC2 (tuberous sclerosis complex) tem incidência significativamente maior em pacientes com gangliogliomas. Correlação entre parâmetros clínicos e neuropatológicos. Em pacientes com lesões positivas para CD34, o início da epilepsia foi mais precoce e a idade quando da cirurgia foi menor que nos CD34 negativos. Houve desaparecimento ou grande redução das crises em 80% dos pacientes com lesões positivas para CD34. Dos 14 pacientes que não melhoraram, 13 tinham lesões negativas para CD34. Uma alta percentagem de tumores de baixo grau associados com epilepsia focal tinha expressão de CD34, e estas células representavam um componente importante. Já tumores de arquitetura semelhante, mas localizados fora do lobo temporal e não associados a epilepsia, não tinham células positivas para CD34. Parece haver uma localização preferencial no lobo temporal de uma população celular CD34+ precursora destes tumores. Na esclerose
hipocampal, onde há intensa gliose, não há expressão
de CD34, reforçando a impressão de que CD34 não é
associado a astrócitos reativos. Quanto à expressão
de CD34 em raras células de fenótipo neuronal, parece mais
provável que seja devida a prolongamentos astrocitários tocando
os neurônios que por expressão endógena por parte dos
próprios neurônios.
|
| CD 34.
O antígeno CD 34 é uma proteína transmembrana densamente glicosilada de 110 kD e função desconhecida. Há alguma evidência de que CD 34 poderia ter papel na adesividade celular, particularmente a lectinas, devido à alta glicosilação. Desta forma, precursores de células hemopoiéticas que expressam CD 34 poderiam ligar-se a células do estroma da medula óssea que expressam lectinas. O antígeno CD 34 foi originalmente definido pelo anticorpo monoclonal MY10 obtido contra a linhagem de células KG1a (de leucemia mielóide humana). O gene para a proteína CD 34 foi localizado ao cromossomo 1q32, e não tem homologia com nenhum outro gene humano conhecido. O antígeno está presente em cerca de 1% das células mononucleares normais da medula óssea, inclusive precursores hemopoiéticos ou células tronco. Também ocorre em células precursoras mais maduras, já comprometidas com uma linhagem (eritróide, mielóide ou linfóide). Entre as células CD34+ estão as células estromais necessárias ao ambiente adequado para hemopoiese. A principal contribuição do CD 34 na patologia diagnóstica advém de sua demonstração em leucemias imaturas e em tumores vasculares. Além de sua positividade em células tronco da MO e em células endoteliais normais, o antígeno é encontrado em células da zona marginal esplênica e em células dendríticas intersticiais em torno de vasos, nervos, folículos pilosos, feixes musculares e glândulas sudoríparas. No endotélio vascular, o antígeno pode estar ausente de grandes veias e artérias, e nos seios da placenta e baço. É expressado na superfície luminal das células endoteliais e nos processos interdigitantes entre as células. Já em vasos neoformados, como em tumores, o antígeno pode também ser encontrado em microprocessos abluminais. CD 34 em neoplasias hemopoiéticas. CD 34 é visto em leucemias imaturas como a leucemia linfoblástica aguda (LLA) de linhagem T ou B, e na leucemia mieloblástica aguda (LMA). Em síndromes mielodisplásicas, expressão de CD 34 prognostica transformação maligna e baixa sobrevida. CD34 é um bom marcador de células mielóides imaturas e, portanto, marca o sarcoma granulocítico. CD 34 em neoplasias vasculares. CD 34 é um bom marcador para tumores vasculares, sendo expressado tanto por células endoteliais de vasos sanguíneos como linfáticos. Há marcação variável das células musculares lisas e seus tumores por CD 34. CD34 marca fortemente os tumores estromais do trato digestivo (GIST). Tumores epiteliais são geralmente negativos para CD34. O marcador é invariavelmente presente em tumor fibroso solitário e dermatofibrosarcoma protuberans. Fonte. Extraído de Leong A S-Y, Cooper K, Leong F J W-M. Manual of Diagnostic Antibodies for Immunohistology. Greenwich Medical Media Ltd, London, 1999. |
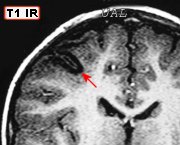
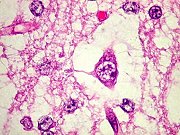
| Para mais imagens deste caso: | TC, RM | HE (DNT e ganglioglioma) |
 |
 |
|
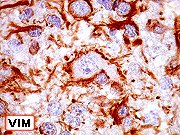
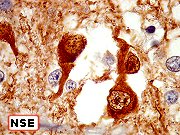
| IH, ganglioglioma | DNT, IH para neurônios | DNT, IH para glia e outros |
 |
 |
 |
| Sobre gangliogliomas | Características de imagem dos gangliogliomas | Neuroimagem e neuropatologia de outros casos de ganglioglioma |
| Sobre o DNT | Características de imagem dos DNTs | Neuroimagem e neuropatologia de outros casos de DNT |
| Neuropatologia
- Graduação |
Neuropatologia -
Casos Complementares |
Neuroimagem
- Graduação |
Neuroimagem -
Casos Complementares |
Correlação
Neuropatologia - Neuroimagem |
|
|
|
|