|
|
de hemisfério cerebral (padrão histológico predominante: gemistocítico) |
|
|
|
de hemisfério cerebral (padrão histológico predominante: gemistocítico) |
|
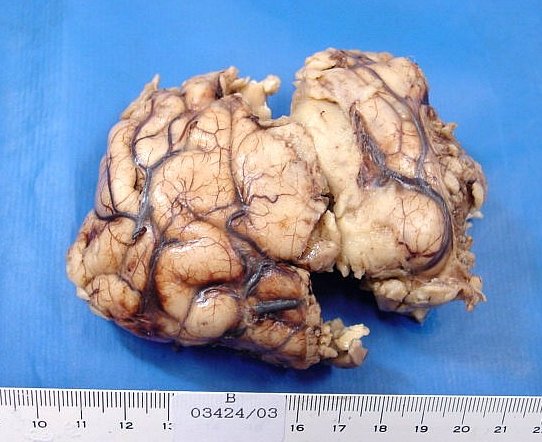
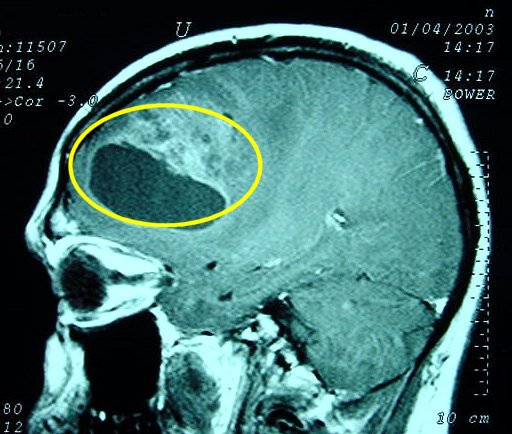
| Resumo da neuroimagem vs. Espécime cirúrgico |
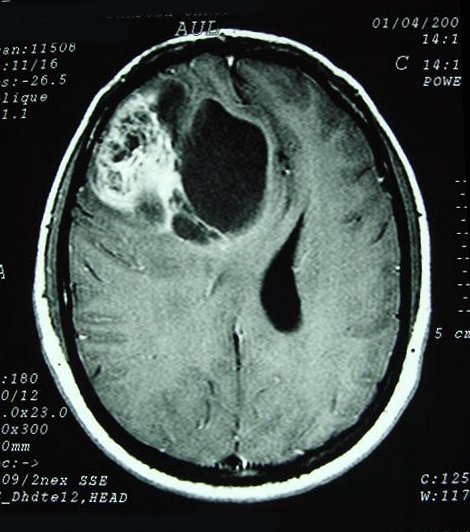 |
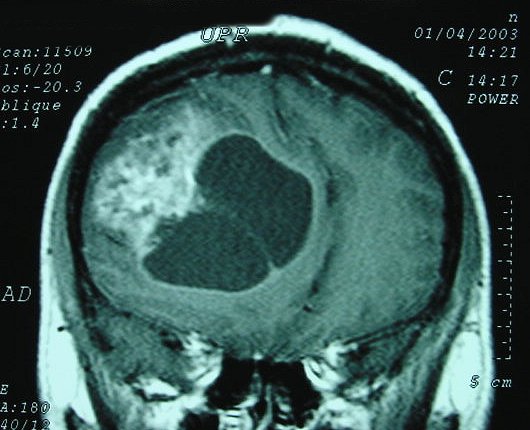 |
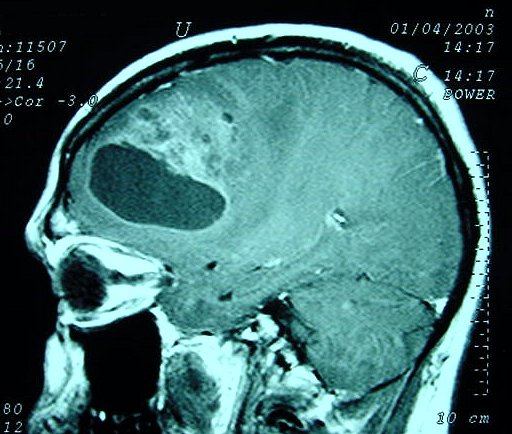 |
 |
 |
 |
 |
 |
 |
 |
|
 |
|
 |
|
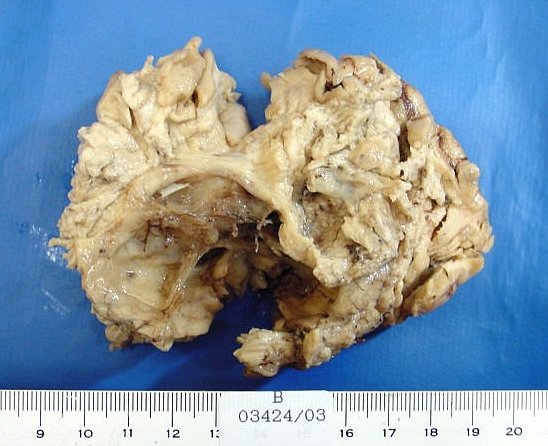
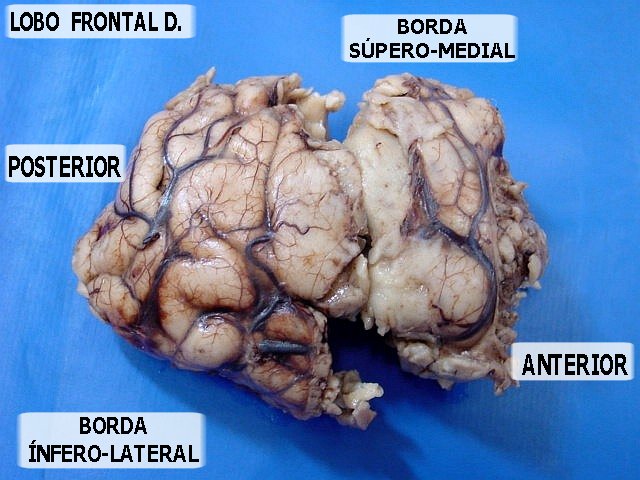
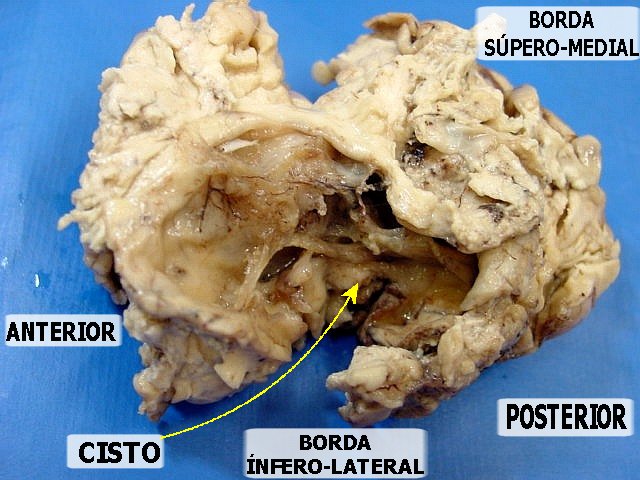
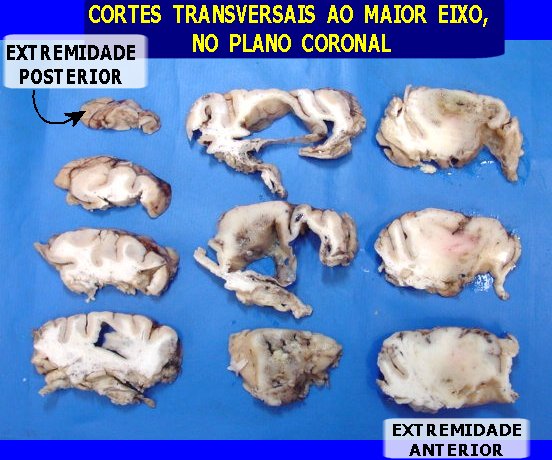
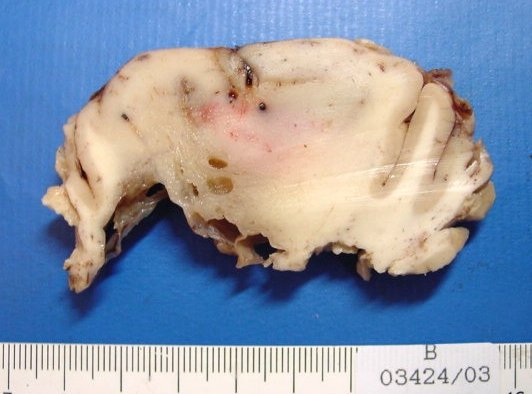
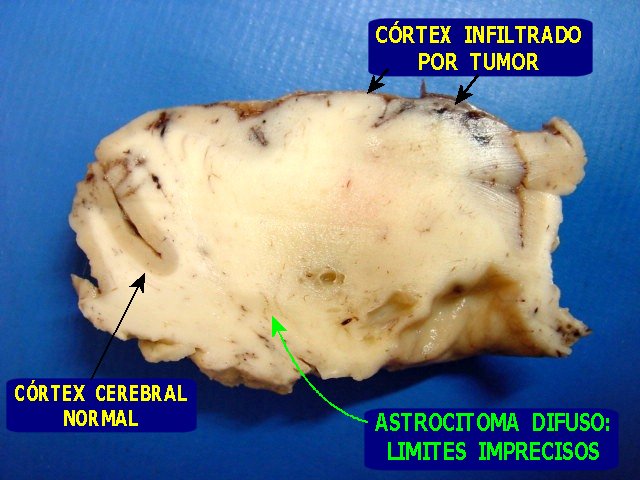
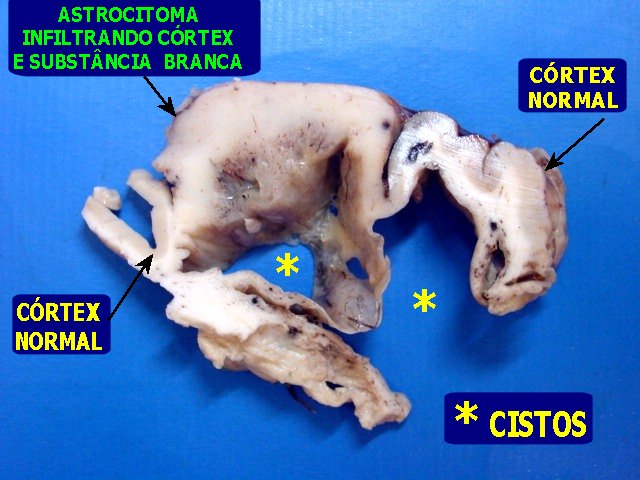
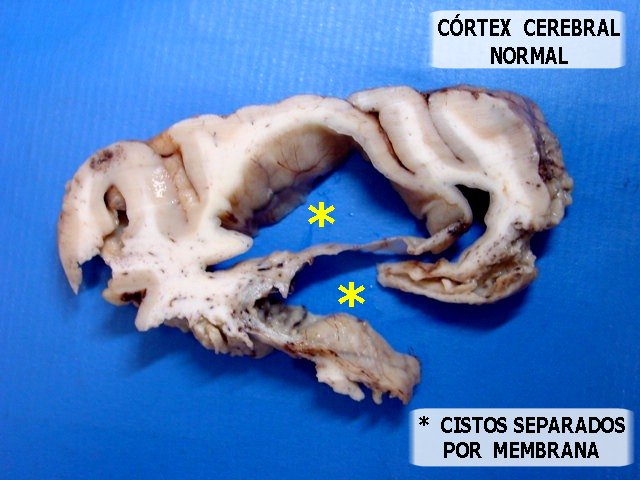
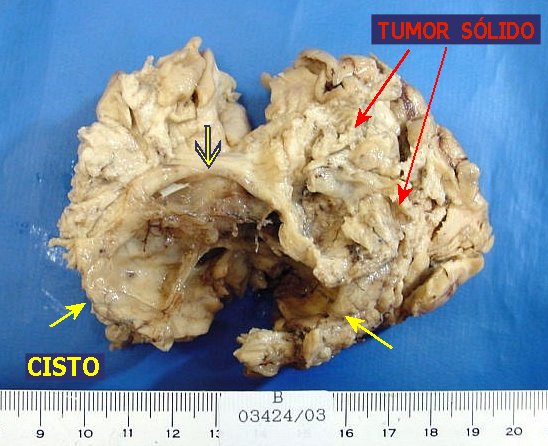
| Grande espécime de lobectomia parcial frontal D, pesando 155 g. e medindo 11 x 8 x 4 cm. Na parte profunda do espécime, cavidade com 5,5 x 4 cm., com paredes finas e lisas. Em cortes transversais, observou-se outra cavidade mais profunda, separada da primeira por fina membrana, e que atingia até a substância branca subcortical. Tumor com áreas microcísticas, acinzentado, mal delimitado, que invade o córtex e a substância branca. | |
 |
 |
|
|
|
|
|
| Área sólida do tumor. É constituída por áreas gemistocíticas (a maior parte), áreas fibrilares e áreas menos diferenciadas. | |
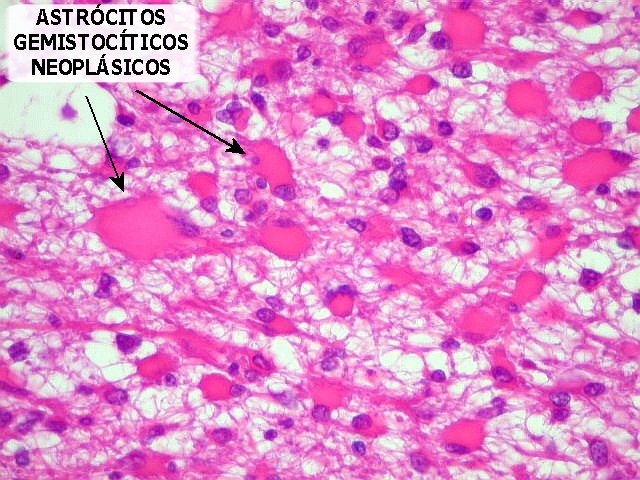
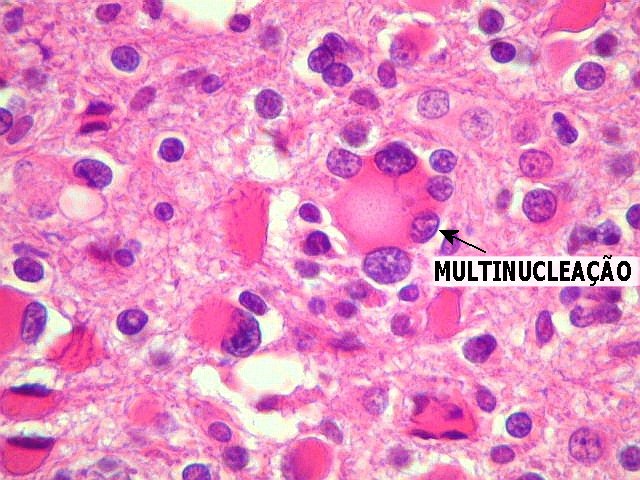
| Áreas
gemistocíticas. Os astrócitos neoplásicos
lembram astrócitos gemistocíticos reativos, que ocorrem em
lesão cerebral de qualquer natureza. Aqui, porém, são
muito numerosos, dando alta celularidade ao tecido, e apresentam atipias,
como variação da forma e tamanho dos núcleos, e das
células como um todo, multinucleação e perda da relação
núcleo-citoplasma. Não há, portanto, perigo
de confundir estas alterações com gliose.
Obs.: a presença de extensas áreas gemistocíticas em um astrocitoma difuso, como no presente caso, tem implicação prognóstica, e prenunciam comportamento agressivo do tumor, ou seja, evolução para grau mais alto no decorrer do tempo. |
|
 |
|
 |
|
| Áreas fibrilares. Nestas, predominam astrócitos neoplásicos com morfologia fibrilar, ou seja, abundantes prolongamentos que se entrelaçam dando uma trama fibrilar densa. Os corpos celulares são delicados, com pouco citoplasma, ao contrário das formas gemistocíticas. Os astrocitomas difusos variam consideravelmente de aspecto histológico com a área, sendo comum a coexistência de áreas fibrilares, protoplasmáticas, e gemistocíticas no mesmo tumor, e variam também em relação ao grau de anaplasia. | |
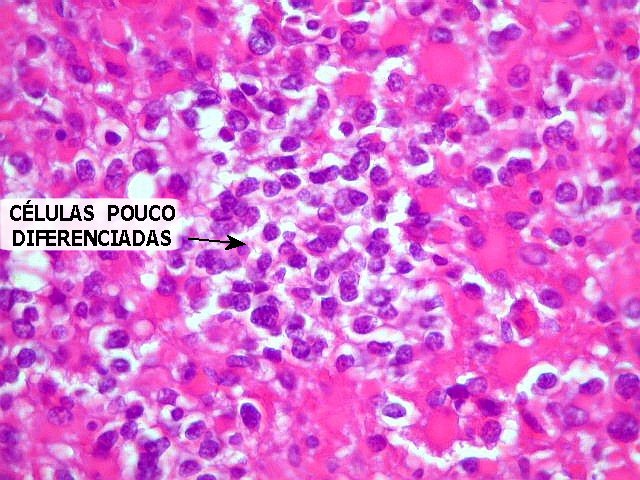
| Áreas menos diferenciadas. Nestas, ocorrem células menores, com pouco citoplasma, que não imitam a formas de astrócitos já exemplificadas acima. São, provavelmente, células com maior tendência a multiplicar-se, como demonstrado pela marcação nuclear para o antígeno Ki-67 (ou MIB-1), associado à proliferação celular. | |
 |
|
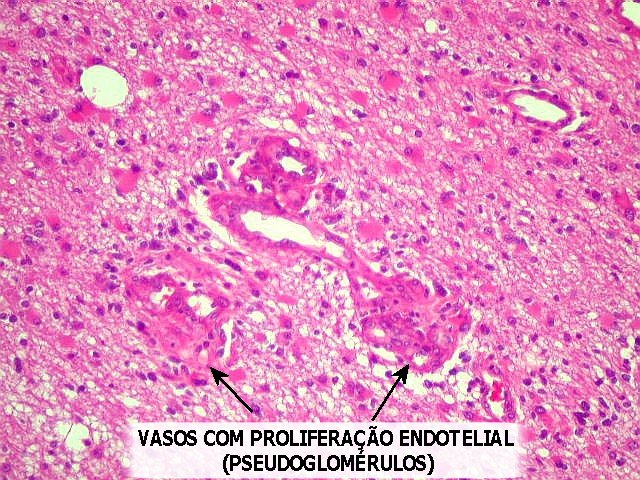
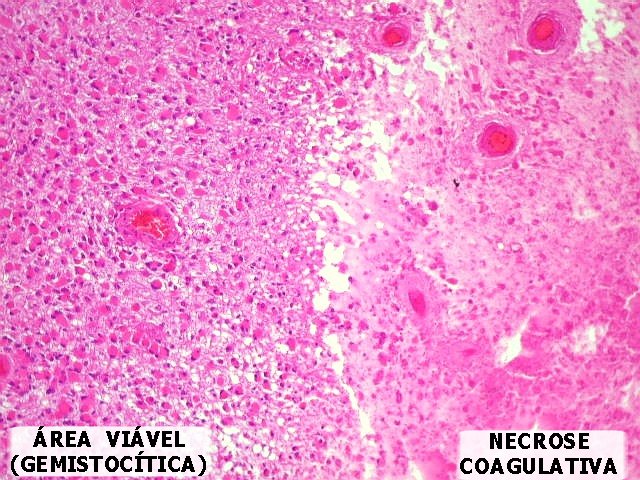
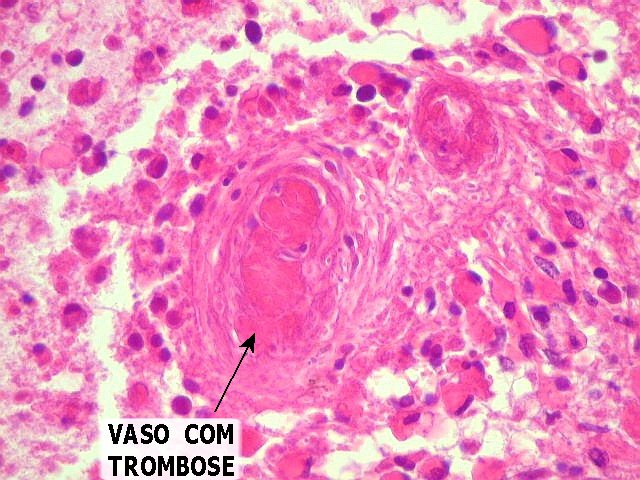
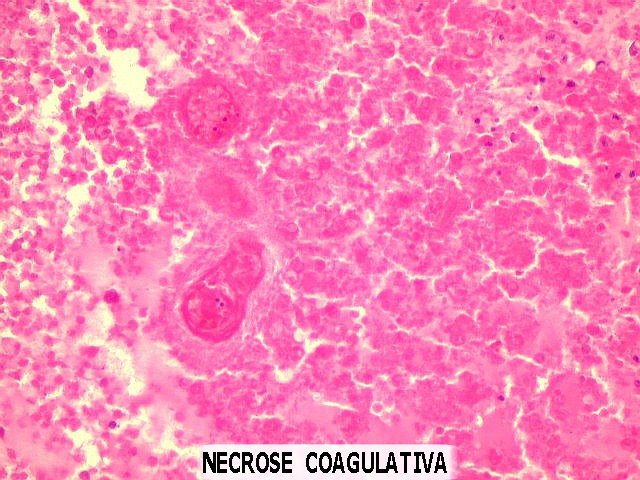
| Proliferação vascular, necrose. A proliferação vascular e a necrose valem juntas como um critério na classificação da OMS para os astrocitomas difusos. O encontro de uma ou da outra (ou de ambas conjuntamente) eleva um grau na escala de malignidade. A proliferação vascular é causada pela multiplicação das células endoteliais, levando a espessamento da parede vascular, estabelecimento de mais de uma luz, ou obliteração da luz existente. Freqüentemente, acompanha-se de trombose, que, por sua vez, leva à necrose coagulativa. A trombose ocorre por defeitos na superfície das células endoteliais proliferadas. Para mais detalhes sobre a classificação dos astrocitomas difusos segundo os critérios da Organização Mundial da Saúde, clique aqui. | |
 |
|
 |
|
 |
 |
| Parede do cisto. Aspecto semelhante ao das outras áreas do tumor. | |
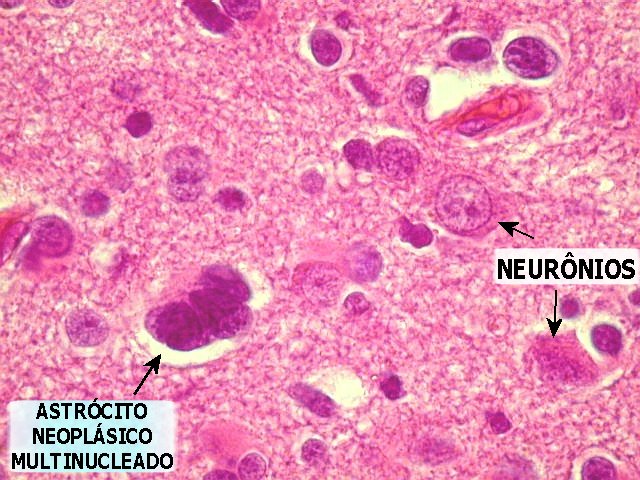
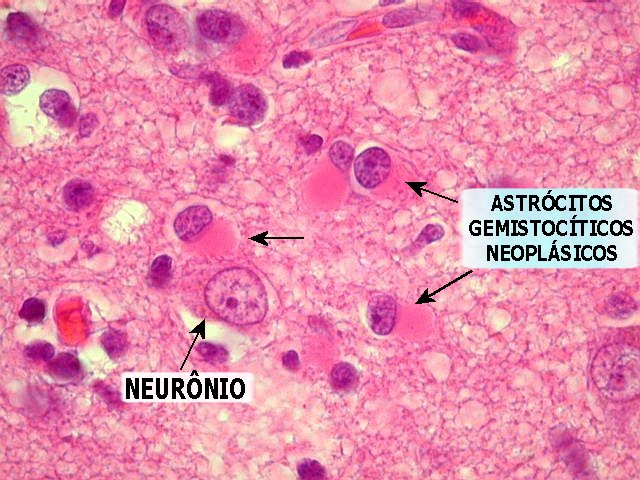
| Infiltração do córtex. O córtex cerebral está com celularidade aumentada e perde sua arquitetura normal, devido à infiltração por células neoplásicas, freqüente nos astrocitomas difusos. As células que infiltram são em sua maior parte astrócitos gemistocíticos, que chamam a atenção pelo citoplasma abundante e róseo. São encontradas lado a lado com neurônios, e no neurópilo. | |
 |
|
 |
|
| IMUNOHISTOQUÍMICA |
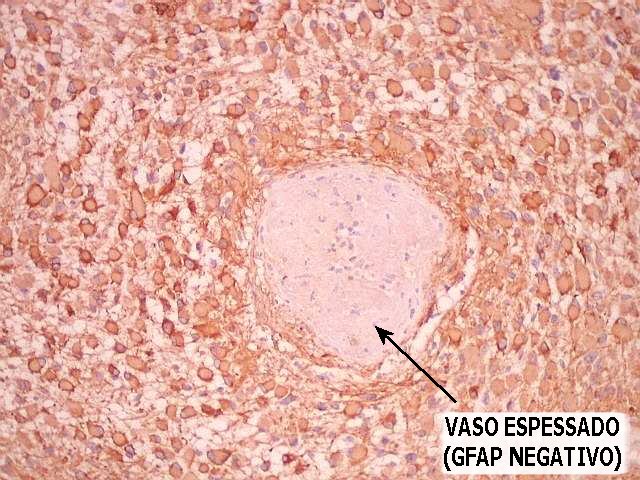
| GFAP. Difusamente positivo nos astrócitos neoplásicos, com certo reforço na periferia dos astrócitos gemistocíticos. Vasos proliferados são negativos. | |
 |
|
| S-100. Positivo em parte das células neoplásicas. Positividade pode ser nuclear, citoplasmática ou ambas. S-100 é um antígeno neuroectodérmico, presente também em células de Schwann (portanto em schwannomas) e em melanócitos (portanto, em melanomas). | |
| VIM. Distribuição e morfologia semelhantes às do GFAP. | |
| KI-67. A proporção de núcleos marcados varia de forma inversamente proporcional ao grau de diferenciação do tumor. Em áreas bem diferenciadas, ricas em astrócitos gemistocíticos, há poucos núcleos marcados. Onde as células são menores, com menos citoplasma, sugerindo maior grau de anaplasia, a marcação é vista em vários núcleos (neste caso, até cerca de 10%). | |
|
|
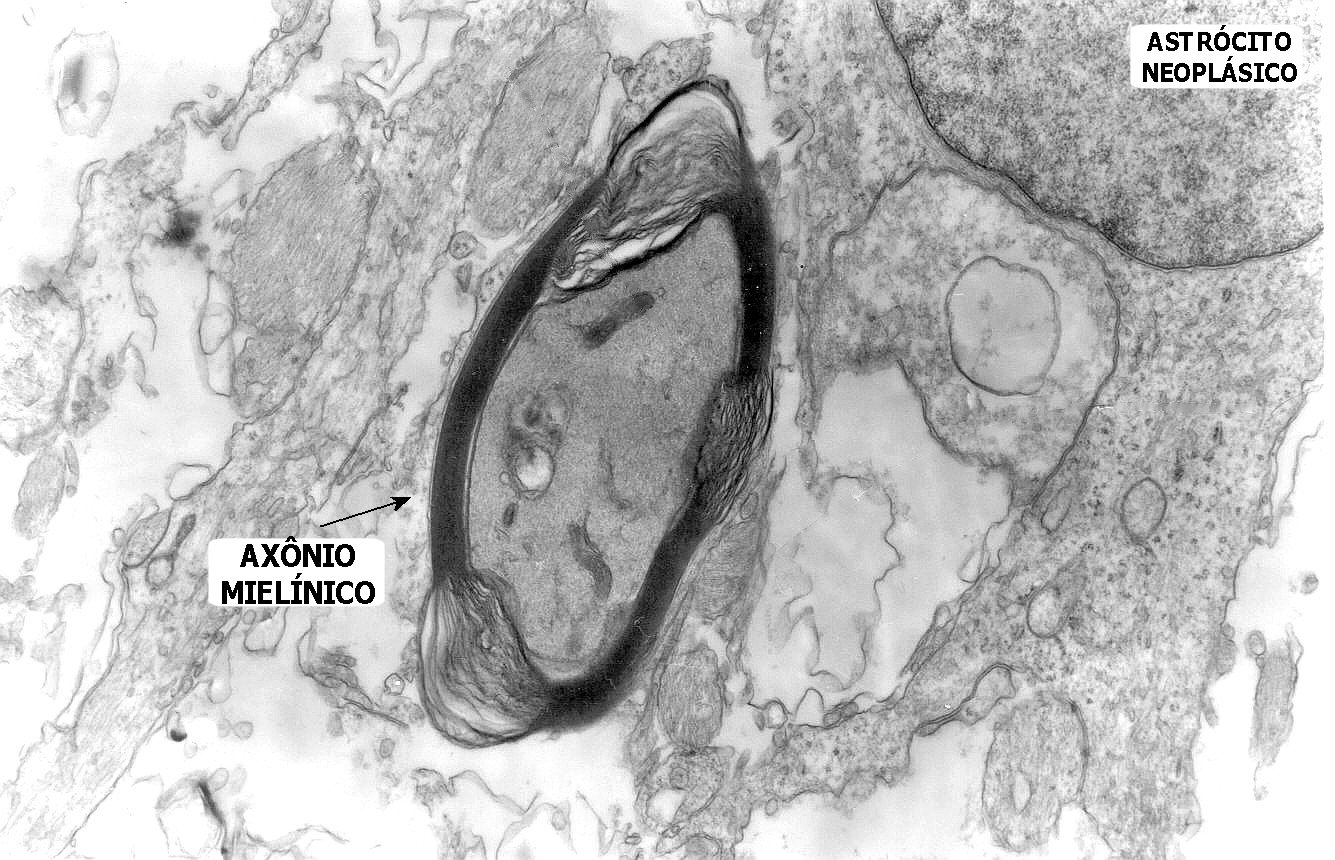
| A microscopia
eletrônica não contribui para o diagnóstico neste caso,
que é estabelecido já na HE. Foi feita a título
de curiosidade e de ganhar maior experiência com a técnica,
para uso em tumores de diagnóstico mais difícil. Os fragmentos
foram obtidos do espécime demonstrado no topo desta página,
já após várias horas de fixação em formol.
Apesar disso, o grau de conservação da ultraestrutura é
aceitável.
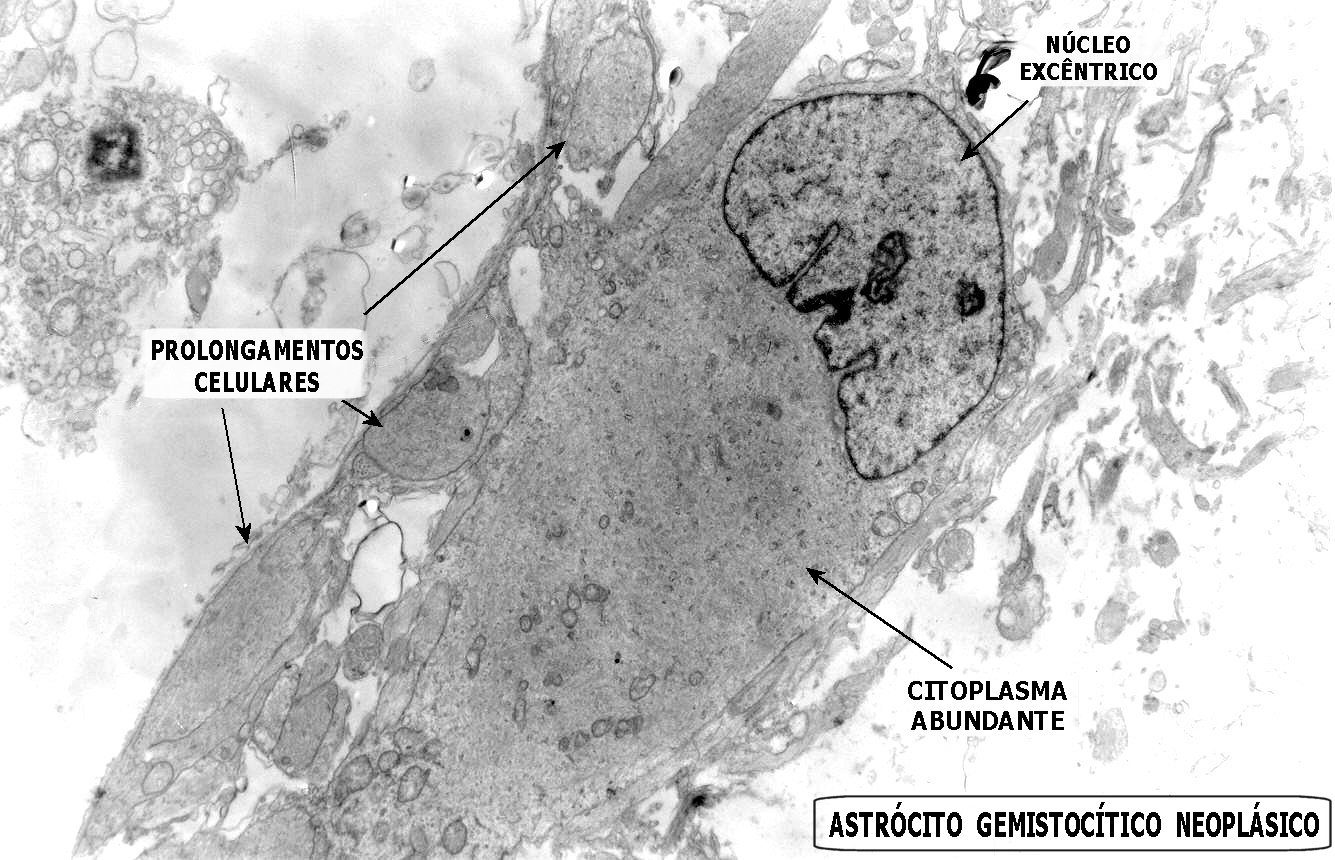
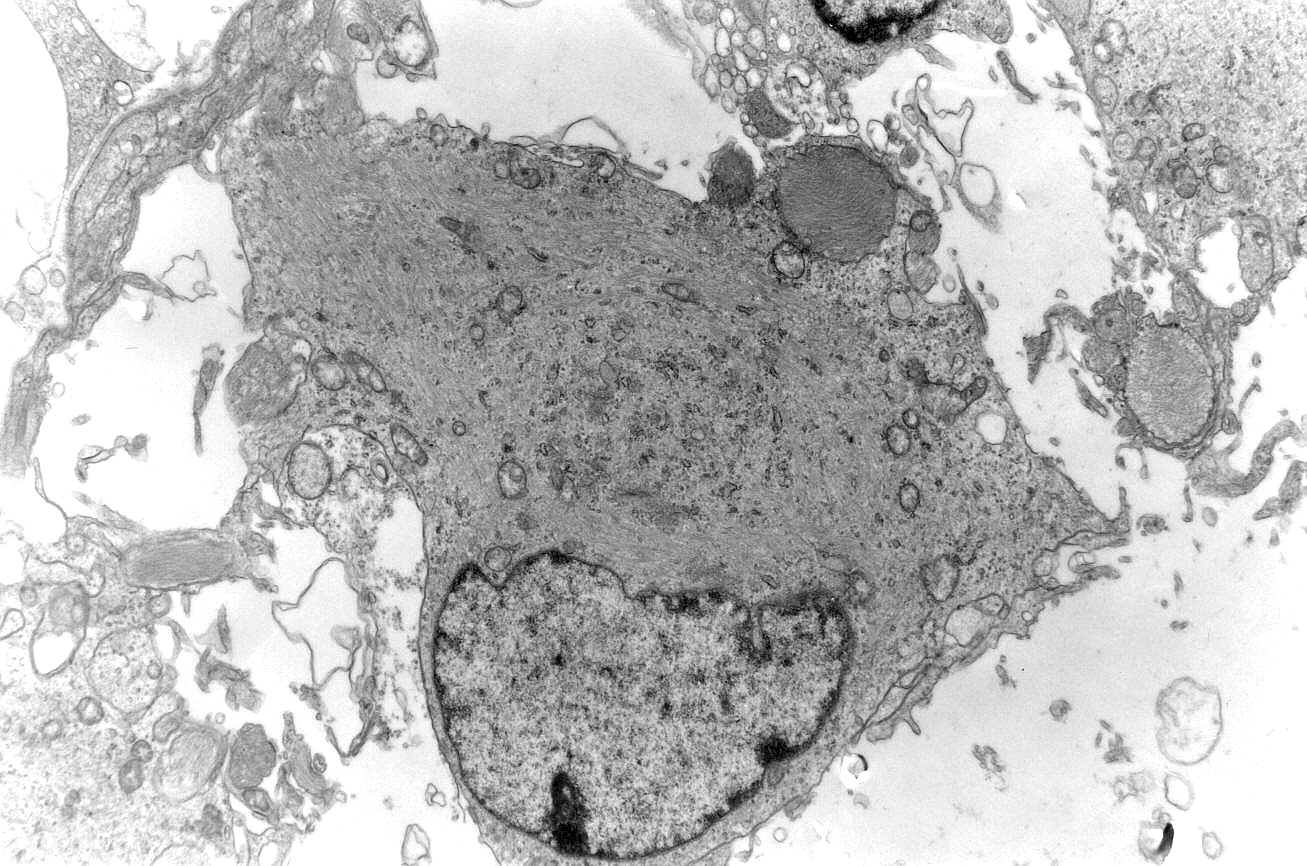
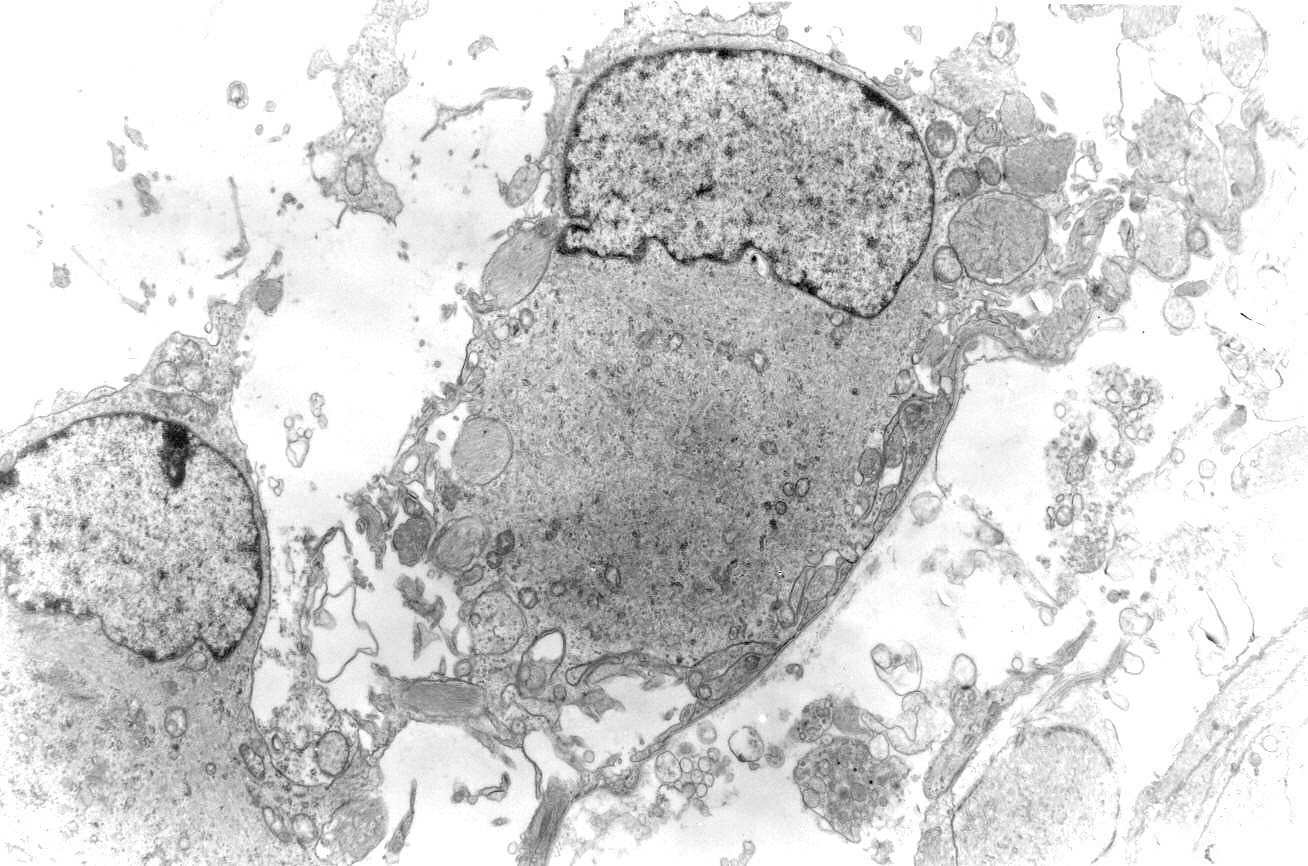
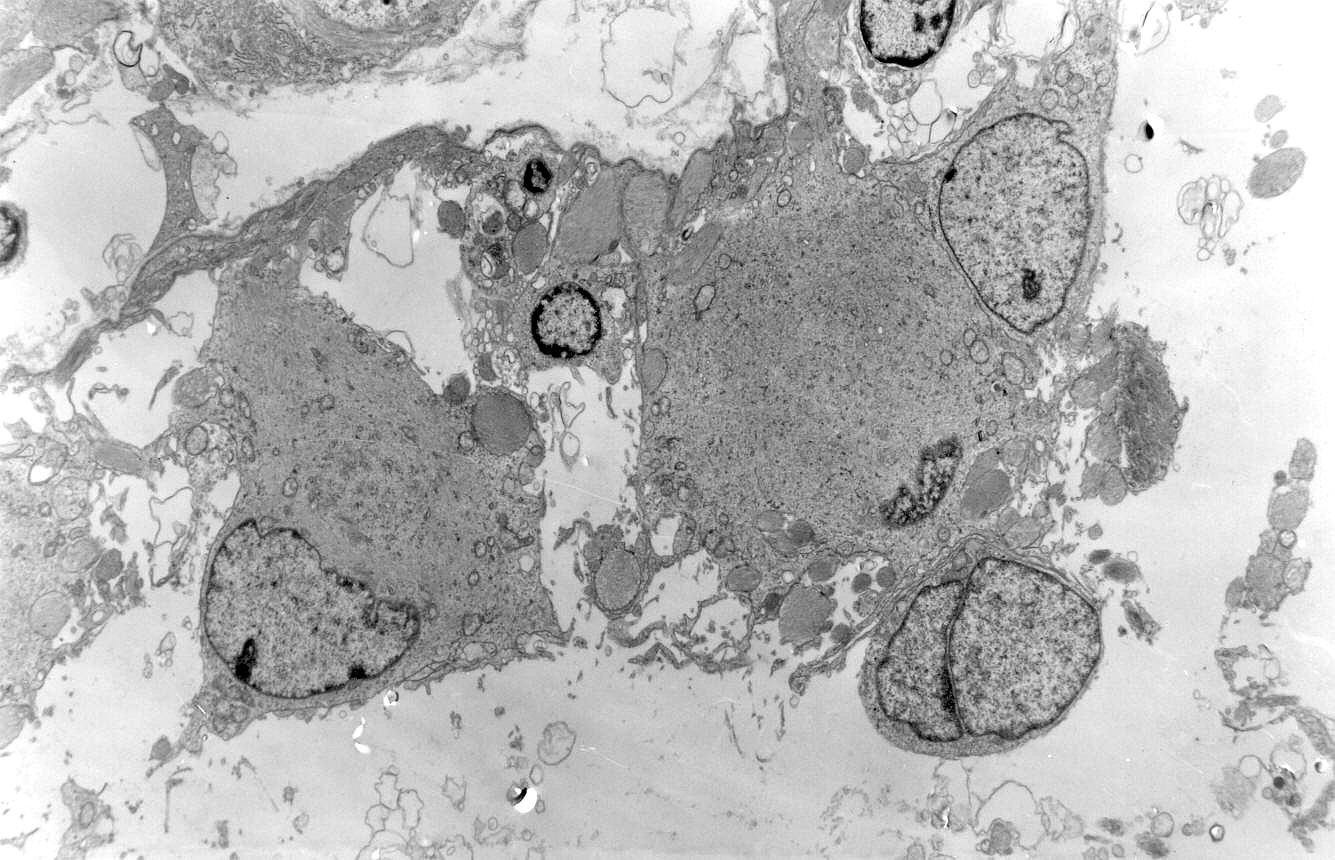
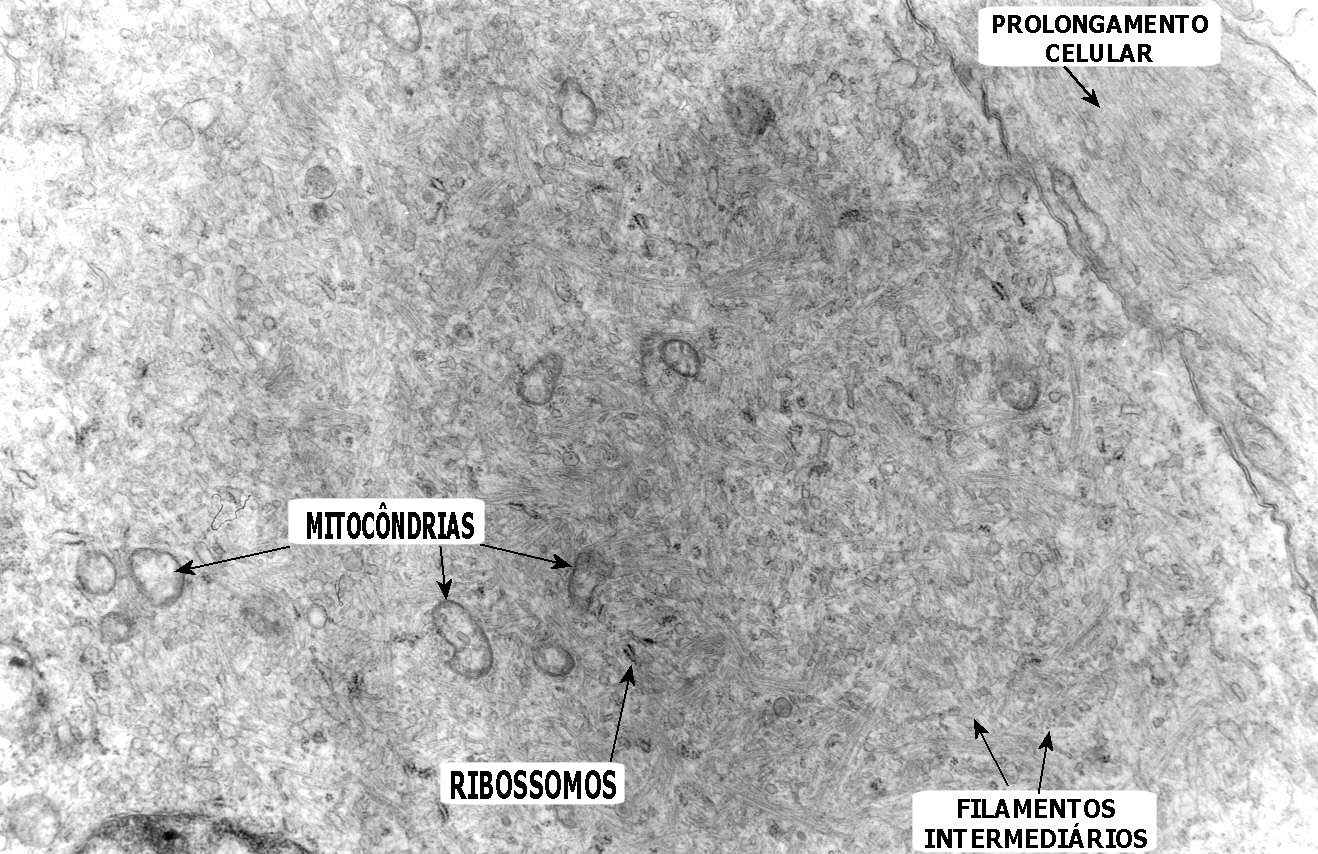
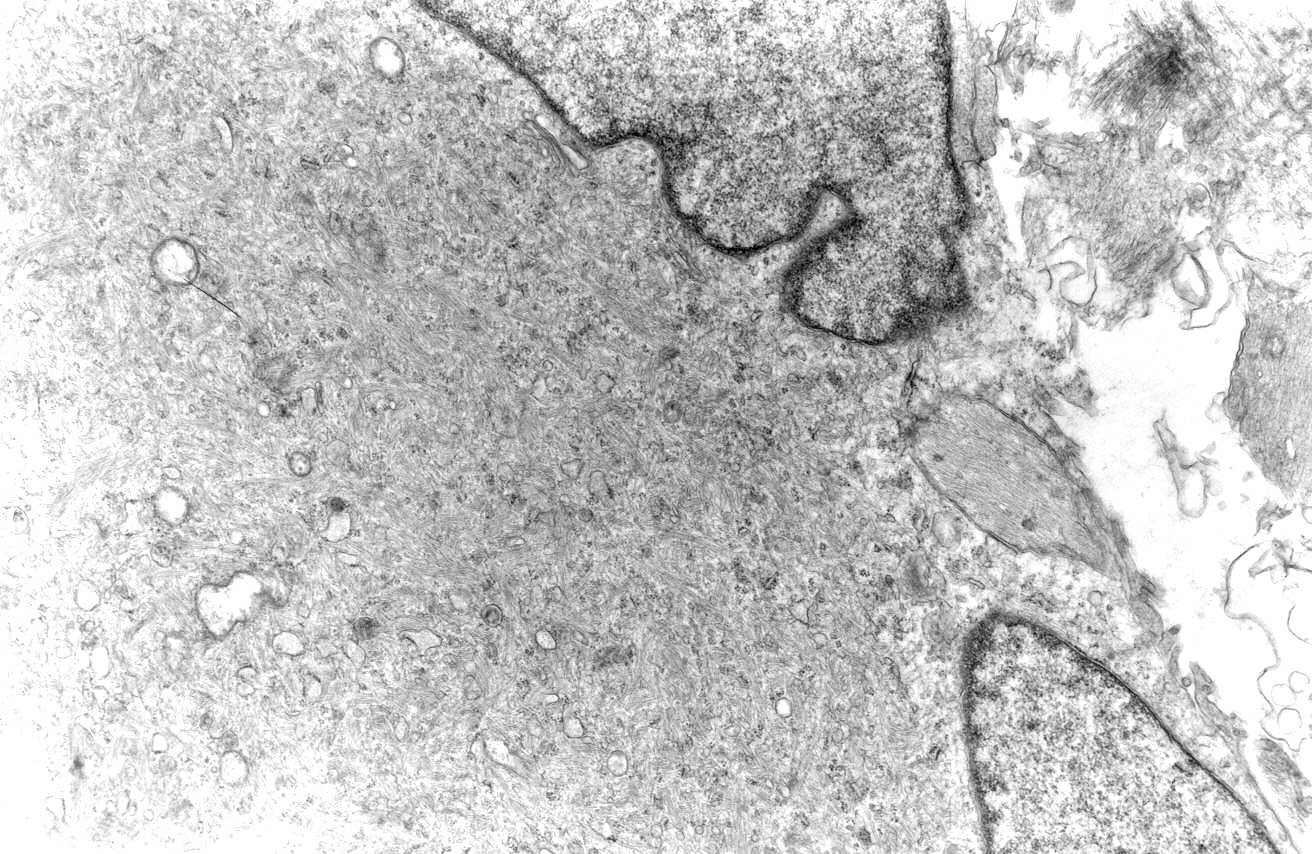
As fotos mostram astrócitos gemistocíticos neoplásicos, com núcleo excêntrico e abundante citoplasma. A cromatina nuclear é frouxa, formando fina orla mais densa na periferia, abaixo da carioteca. O citoplasma é preenchido por poucas organelas (mitocôndrias, rosetas de ribossomos), dispersas entre abundantes filamentos intermediários (que correspondem principalmente a GFAP e vimentina, como demonstrado na imunohistoquímica). |
 |
 |
 |
 |
 |
 |
 |
Astrocitomas são tumores originados em astrócitos. São classificados basicamente em difusos e pilocíticos. Os astrocitomas pilocíticos ocorrem em localizações especiais como no cerebelo e nervo óptico. Predominam em crianças e são considerados de grau de malignidade baixo (grau I da OMS). Os astrocitomas difusos ocorrem principalmente em hemisférios cerebrais de adultos e são os tumores mais comuns originados em células gliais (gliomas). São chamados difusos porque não têm boa delimitação e apresentam tendência infiltrativa. Além disso, tendem a progredir com o tempo a graus mais altos de malignidade. Assim, seu prognóstico a longo prazo é sombrio. |
Classificação dos astrocitomas difusos segundo a OMS.
| Critérios (feições) histológicas | Nome | Graduação | Sobrevida |
| 1 critério, geralmente atipias nucleares. | Astrocitoma difuso de baixo grau | Grau II | > 5 anos |
| 2 critérios, geralmente atipias nucleares e mitoses | Astrocitoma anaplásico | Grau III | 2 a 5 anos |
| 3 ou 4 critérios: atipias, mitoses, proliferação vascular e/ou necrose. | Glioblastoma multiforme | Grau IV | < 1 ano. |
| Para ver a ressonância magnética deste tumor, clique ao lado: | 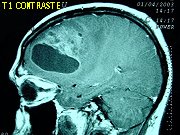 |
| Neuropatologia
- Graduação |
Neuropatologia -
Casos Complementares |
Neuroimagem
- Graduação |
Neuroimagem -
Casos Complementares |
Correlação
Neuropatologia - Neuroimagem |
|
|
|